Inleiding
Pulmonale embolie (PE) is een veel voorkomende aandoening met een jaarlijkse incidentie van 110 gevallen per 100.000 volwassenen,1 die de laatste jaren toeneemt.1,2 De symptomen kunnen variëren van asymptomatisch tot obstructieve shock na collaps van de bloedsomloop.3 Het totale sterftecijfer is niet alleen hoog, maar ook zeer variabel. In een recente studie bedroeg de totale mortaliteit 8,65% na drie maanden.4 De centrale slagaders zijn het meest betrokken,5,6 terwijl subsegmentale PE 4-7% van de gevallen uitmaakt.7-9 Een aantal studies meldt echter subsegmentale betrokkenheid bij tot 30% van de patiënten.9
De klinische relevantie van de omvang van PE is nog steeds discutabel, en de rol van antistolling bij patiënten met subsegmentale betrokkenheid is in een aantal studies betwist.10,11
Het doel van onze studie was de klinische bijzonderheden van patiënten met PE in ons ziekenhuis te beschrijven en hun prognose op basis van de uitgebreidheid van de ziekte te analyseren.
Methoden
We voerden een retrospectieve studie uit van alle patiënten ouder dan 18 jaar met een bevestigde CT thoraxscandiagnose van PE12 in het ziekenhuiscomplex van Pontevedra in Spanje tussen januari 2005 en december 2010. De follow-up eindigde op 31 januari 2012, de deadline voor overleving. De minimale follow-up was dus 14 maanden. Administratieve gegevens van gecodeerde ziekenhuisontslagen werden gebruikt voor de selectie van patiënten. Patiënten met onvolledige gegevens en/of een diagnose gesteld met andere methoden dan CT-scan van de borst werden uitgesloten van de oorspronkelijke steekproef van 470 patiënten. Aldus werden 313 gevallen in de studie opgenomen.
De volgende gegevens werden geanalyseerd:
-
Persoonlijke gegevens: leeftijd, geslacht, actief roken en zwaarlijvigheid (body mass index >30).
-
Clinische gegevens, lichamelijk onderzoek en aanvullende testgegevens: recente operatie, anesthesie, trauma, kanker, langdurig reizen en/of immobilisatie; verlamming van de onderste ledematen; inbrengen van een centrale katheter, trombofilie of antifosfolipidensyndroom; eerdere veneuze trombo-embolische ziekte (VTE); spataderen in de onderste ledematen; zwangerschap, anticonceptie of hormoontherapie. Tachypneu, crepitant rale, tekenen van DVT in de onderste ledematen; vitale functies, systolische hypotensie (SBP
100mmHg), diastolische hypotensie (DBP60mmHg) en tachycardie (hartslag>100).13,14 Arteriële bloedgas analyse, hemoglobine, hematocriet, aantal bloedplaatjes, leukocytose, neutrofilie, glucose, ureum, creatinine, natrium, kalium en fibrinogeen, gestratificeerd als normaal of abnormaal volgens de laboratorium referentiewaarden in ons ziekenhuis. D-dimeer niveaus werden bepaald met een hoog-gevoelige turbidimetrische immunoassay. D-dimeerwaarden boven 500ng/ml werden als pathologisch beschouwd. De nierfunctie werd als normaal beschouwd bij een glomerulaire filtratiesnelheid volgens de verkorte MDRD-vergelijking van meer dan 60 ml/min/1,73 m2.15 Elektrocardiografische en beeldvormingsbevindingen: gewone röntgenfoto van de borst; echo-Doppler van de onderste ledematen (volledig of distaal) werd uitgevoerd naar goeddunken van de radioloog, op basis van de klinische presentatie van de patiënt. PE’s werden verzameld en met CT-scan van de borstkas in drie groepen ingedeeld: centraal (hoofdstam, rechter- of linkerlongslagader, tussenliggende slagaders of lobaire slagaders), segmentaal en subsegmentaal. De locatie van de trombus werd bepaald aan de hand van de grootste betrokken slagader. Comorbiditeit gemeten aan de hand van de Charlson-index (CCI), ingedeeld in “0”, “1-2” en “≥3”.16
Klinische waarschijnlijkheid werd bepaald met de scores van Wells17 en Geneva18.
Oorzaak van overlijden werd toegekend door de hoofdonderzoeker op basis van beschikbare medische dossiers en ingedeeld in drie groepen: PE-gerelateerd, PE-ongerelateerd, en onbekend. Discrepantie tussen gegevens en onzekere einddiagnoses werd opgelost door bespreking met gegevensverzamelaars.
Statistische analyse
Categorische variabele gegevens worden gepresenteerd als frequenties (procenten); continue variabele gegevens worden gepresenteerd als medianen en interkwartielbereiken.
Fisher’s exact en Chi-kwadraat tests werden gebruikt om categorische variabelen te vergelijken. Tussen groepen werden continue variabelen vergeleken met behulp van ANOVA of de Kruskal-Wallis test bij niet-normale verdelingen.
Overlevingscurven en toenames in de kans op overlijden werden respectievelijk berekend met de Kaplan-Meier test en de Cox regressie. Verschillen werden als significant beschouwd bij p
0,05. De gegevens werden geanalyseerd met SPSS 15 voor Windows.Resultaten
De studie includeerde 313 PE-patiënten; 56% was vrouw en de mediane leeftijd was 70 jaar (interkwartielbereik 53-78 jaar). Centrale PE was goed voor 68% van de gevallen; segmentale en subsegmentale PE, voor 25% en 7%. Patiënten met subsegmentale PE waren jonger, hadden minder comorbiditeit en geen van hen presenteerde proximale DVT (tabel 1). Onder de patiënten in de subsegmentale PE groep bevonden zich 10 (45%) met enkelvoudige PE en 12 (55%) met meervoudige PE.
Wat de symptomen betreft, dyspneu komt het meest voor bij patiënten met centrale PE, en ook pijn komt vaak voor bij segmentale en subsegmentale PE (Tabel 1). Comorbiditeit gemeten door CCI was aanwezig in 78% van de gevallen, en kwam vaker voor bij centrale PE (Tabel 1). Bij 22% van de patiënten was voorafgaand aan de PE de diagnose kanker gesteld (gegevens niet weergegeven). Wat betreft de aanwezigheid van risicofactoren en de klinische waarschijnlijkheid van PE volgens de Wells en Geneva scores, werden geen verschillen gevonden in de uitgebreidheid van de ziekte (Tabel 1). Wat de aanvullende tests betreft, vertoonden patiënten met betrokkenheid van de centrale slagader significant hogere D-dimeerwaarden en presteerden zij slechter bij de bloedgasanalyse. Er werd geen significant verschil gevonden in de overige parameters (Tabel 2). Alle patiënten werden opgenomen in het ziekenhuis en behandeld met anticoagulantia.
De 30-dagen mortaliteit was 7%, toe te schrijven aan PE in 3,5% van de gevallen. Patiënten met subsegmentale PE vertoonden significant hogere overlevingspercentages, zowel na 30 dagen als aan het einde van de follow-up (Fig. 1). Er werd geen verschil waargenomen in de doodsoorzaak op basis van de uitgebreidheid van PE (afb. 2). Factoren die onafhankelijk verband hielden met een hogere waarschijnlijkheid van overlijden waren de diagnose kanker en een hogere comorbiditeit gemeten aan de hand van de Charlson-index (tabel 3).
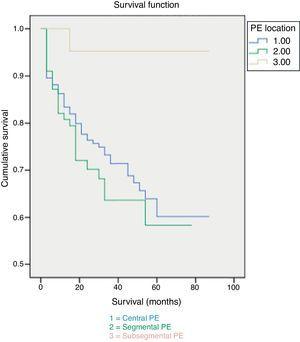
Alle overlevingskansen en omvang van PE.

Oorzaken van overlijden en uitbreiding van PE.
Predictoren van sterfte. Multivariate analyse.
| Factoren | OR | CI 95% |
|---|---|---|
| PE locatie | ||
| Centraal | 1 | |
| Segmentaal | 1.28 | 0.79-2.09 |
| Subsegmentaal | 0.29 | 0.03-2.23 |
| Kanker | ||
| Nee | 1 | |
| Ja | 3.72 | 2.30-6.03 |
| Charlson | ||
| 0 | 1 | |
| 1-2 | 2.81 | 0.82-9.59 |
| ≥3 | 8.61 | 2.58-28,69 |
Gecorrigeerd voor leeftijd, geslacht, nierfunctie en bloedgasparameters.
Discussie
Prevalentie van subsegmentale PE was 7%, vergelijkbaar met die gerapporteerd door andere auteurs.5 Er werd geen significant geslachtsverschil gevonden wat betreft de uitgebreidheid van de ziekte; het aandeel vrouwen is echter iets hoger in onze steekproef. De leeftijd van patiënten met subsegmentale PE was lager dan die van patiënten met centrale en segmentale PE. Het verschil zou verband kunnen houden met hypercoagulatie en de veranderingen in het vasculaire endotheel die optreden bij het ouder worden19 : deze zouden de omvang van trombi bij oudere patiënten kunnen vergemakkelijken, vooral gezien het feit dat er geen leeftijdsverschil werd gevonden in de prevalentie van risicofactoren voor PE.
Hoewel de symptomen van PE aspecifiek zijn en de presentatie gewoonlijk gelijkaardig is bij volwassenen, vonden we pijn op de borst bij jongere patiënten en een positieve associatie tussen leeftijd en dyspneu.19 In onze studie werd pijn op de borst bij jongere patiënten met perifere PE en dyspneu bij oudere patiënten met centrale PE en hogere niveaus van hypoxie het vaakst gemeld. In het algemeen kwam dyspneu minder vaak voor bij patiënten met subsegmentale PE.10 Deze presteerden beter bij bloedgasanalyse en hadden over het algemeen een minder ernstige klinische presentatie,20 waaronder minder proximale DVT.5,10
D-dimeerwaarden bij patiënten met PE lijken geassocieerd te zijn met trombusgrootte, zijn gerelateerd aan de PE-ernst en hebben waarde als prognostische marker.21 Wij vonden lagere serumwaarden bij patiënten met subsegmentale PE, die een meer goedaardige klinische presentatie hadden en een betere uitkomst op middellange termijn. D-dimeer testen werden echter slechts in 30% van de gevallen uitgevoerd. Onze resultaten zijn dus niet doorslaggevend.
In onze studie was de 30-dagen mortaliteit hoger dan in andere studies,22 hoewel het aandeel PE-gerelateerde sterfgevallen vergelijkbaar was.4 Geen van de patiënten overleed ten gevolge van subsegmentale PE. De verschillen in mortaliteit zouden verschillende oorzaken kunnen hebben: de gemiddelde leeftijd van onze patiënten is hoger, velen hebben begeleidende chronische ziekten die de slechte uitkomst van PE kunnen conditioneren, en het aantal sterfgevallen als gevolg van comorbiditeit is ook hoog. In feite is de belangrijkste bepalende factor voor sterfte comorbiditeit, met name kanker. Patiënten met kanker en PE hebben niet alleen een slechte prognose, maar ook een slechtere prognose dan patiënten met alleen kanker of PE.23 Symptomen van PE kunnen worden verward met die van exacerbaties van eerdere cardiopulmonale ziekten,24 wat leidt tot vertraagde diagnose en behandeling, slechtere prognose en hogere mortaliteit. Oudere patiënten zijn complexer en kunnen een hogere comorbiditeit en vertraagde diagnose hebben24; comorbiditeit is ook gesuggereerd als risicofactor voor PE bij deze patiënten.25,26
De klinische betekenis van subsegmentale PE is onbekend. Het kan echter klinische relevantie en gevolgen op lange termijn hebben bij patiënten met een lage cardiopulmonale reserve.2 Het heeft gewoonlijk een lage mortaliteit2,27 en een goede prognose.5,28 Daarom heeft een aantal auteurs gesuggereerd dat bepaalde patiënten geen anticoagulantiatherapie nodig zouden hebben.29,30
Onze gegevens suggereren dat patiënten met subsegmentale PE klinisch in grote mate verschillen van patiënten met meer proximale PE. De prognose wordt eerder beïnvloed door de aanwezigheid van begeleidende aandoeningen dan door de uitgebreidheid van de ziekte.
Ethische openbaarmakingenBescherming van menselijke en dierlijke proefpersonen
De auteurs verklaren dat de gevolgde procedures in overeenstemming waren met de voorschriften van de desbetreffende ethische commissie voor klinisch onderzoek en met die van de Code of Ethics van de World Medical Association (Verklaring van Helsinki).
Geheimhouding van gegevens
De auteurs verklaren dat zij de protocollen van hun werkcentrum inzake de publicatie van patiëntengegevens hebben gevolgd en dat alle in de studie opgenomen patiënten voldoende informatie hebben ontvangen en schriftelijk geïnformeerde toestemming hebben gegeven om aan de studie deel te nemen.
Recht op privacy en geïnformeerde toestemming
Geef een antwoord