schizofrenie
Kortetermijnonderzoeken – Volwassenen
De werkzaamheid van SEROQUEL XR bij de behandeling van schizofrenie werd aangetoond in 1 kortetermijn, 6 weken durende, placebogecontroleerde studie met vaste doses bij intramurale en extramurale patiënten met schizofrenie (n=573) die voldeden aan de DSM-IV-criteria voor schizofrenie. SEROQUEL XR (eenmaal daags) werd toegediend als 300 mg op dag 1, en de dosis werd verhoogd tot 400 mg of 600 mg op dag 2, of 800 mg op dag 3. Het primaire eindpunt was de verandering van de totale score van de Positive and Negative Syndrome Scale (PANSS) ten opzichte van de uitgangssituatie aan het einde van de behandeling (dag 42). SEROQUEL XR doses van 400 mg, 600 mg en 800 mg eenmaal daags waren superieur aan placebo wat betreft de PANSS-totaalscore op Dag 42 (studie 1 in Tabel 26).
Kortetermijnproeven -Adolescenten (leeftijd 13-17 jaar)
De werkzaamheid van SEROQUEL XR bij de behandeling van schizofrenie bij adolescenten (13-17 jaar) werd ondersteund door een 6 weken durend, dubbelblind, placebogecontroleerd onderzoek. Patiënten die voldeden aan de diagnostische criteria van de DSM-IV voor schizofrenie werden gerandomiseerd in een van de drie behandelingsgroepen: SEROQUEL 400 mg/dag (n=73), SEROQUEL 800 mg/dag (n=74), of placebo (n=75). De studiemedicatie werd gestart met 50 mg/dag en op dag 2 verhoogd tot 100 mg/dag (verdeeld en twee of drie keer per dag gegeven). Vervolgens werd de dosis getitreerd tot de beoogde dosis van 400 mg/dag of 800 mg/dag met stappen van 100 mg/dag, verdeeld en twee of drie keer per dag toegediend. De primaire variabele voor de werkzaamheid was de gemiddelde verandering ten opzichte van de uitgangswaarde in de totale Positieve en Negatieve Syndroom Schaal (PANSS). SEROQUEL met 400 mg/dag en 800 mg/dag was superieur aan placebo wat betreft de vermindering van de totale PANSS-score (studie 2 in tabel 26).
|
Studie Nummer |
Behandelingsgroep |
Primair werkzaamheidseindpunt: PANSS Totaal |
||
|
Gemiddelde Baseline Score (SD) |
LS Gemiddelde Verandering vanaf Baseline (SE) |
Placebo-afgetrokken Verschil Verschil (geneesmiddel min placebo) in kleinste-kwadraten gemiddelde verandering vanaf baseline.
(95% CI) |
||
|
Studie 1 |
SEROQUEL XR (400 mg/dag) Doses die statistisch significant beter zijn dan placebo
|
95.8 (13.9) |
-24.8 (2,5) |
-6,1 (-11,5, -0,6) |
|
SEROQUEL XR (600 mg/dag) |
96.8 (14.1) |
-30.9 (2.5) |
-12.1 (-17.6, -6.7) |
|
|
SEROQUEL XR (800 mg/dag) |
97,3 (14,7) |
-31,3 (2,5) |
-12.5 (-17,9, -7,1) |
|
|
SEROQUEL (400 mg/dag) , In de proef opgenomen voor gevoeligheid van de test
|
96.5 (16.0) |
-26.6 (2.4) |
-7.8 (-13.1, -2.4) |
|
|
Placebo |
96,2 (13,3) |
-18,8 (2.5) |
||
|
Studie 2 (adolescenten) |
SEROQUEL (400 mg/dag) |
96.2 (17.7) |
-27.3 (2.6) |
-8.2 (-16.1, -0.3) |
|
SEROQUEL (800 mg/dag) |
96,9 (15,3) |
-28,4 (1.8) |
-9,3 (-16,2, -2,4) |
|
|
Placebo |
96,2 (17,7) |
-19,2 (3.0) |
||
|
SD: standaardafwijking; SE: standaardfout; LS Mean: kleinste kwadraten gemiddelde; CI: ongecorrigeerd betrouwbaarheidsinterval. |
||||
Onderhoudstests
In een langere-termijnstudie (studie 3), klinisch stabiele volwassen poliklinische patiënten (n=171) die voldeden aan de DSM-IV-criteria voor schizofrenie en stabiel bleven na 16 weken open-label behandeling met flexibele doses SEROQUEL XR (400 mg/dag-800 mg/dag) gerandomiseerd naar placebo of voortzetting van hun huidige SEROQUEL XR (400 mg/dag-800 mg/dag) voor observatie op mogelijke terugval tijdens de dubbelblinde voortzettingsfase (onderhoudsfase). Stabilisatie tijdens de open-label fase werd gedefinieerd als het ontvangen van een stabiele dosis SEROQUEL XR en het hebben van een CGI-S≤4 en een PANSS score ≤60 van begin tot einde van deze open-label fase (zonder toename van ≥10 punten in PANSS totale score). Terugval tijdens de dubbelblinde fase werd gedefinieerd als een ≥30% toename van de PANSS-totaalscore, of een CGI-verbeterscore van ≥6, of ziekenhuisopname wegens verslechtering van de schizofrenie, of behoefte aan een ander antipsychoticum. Patiënten op SEROQUEL XR ervoeren een statistisch significante langere tijd tot terugval dan patiënten op placebo (figuur 1).
Figuur 1: Kaplan-Meier Curves van Tijd tot Terugval van Schizofrenie (studie 3)
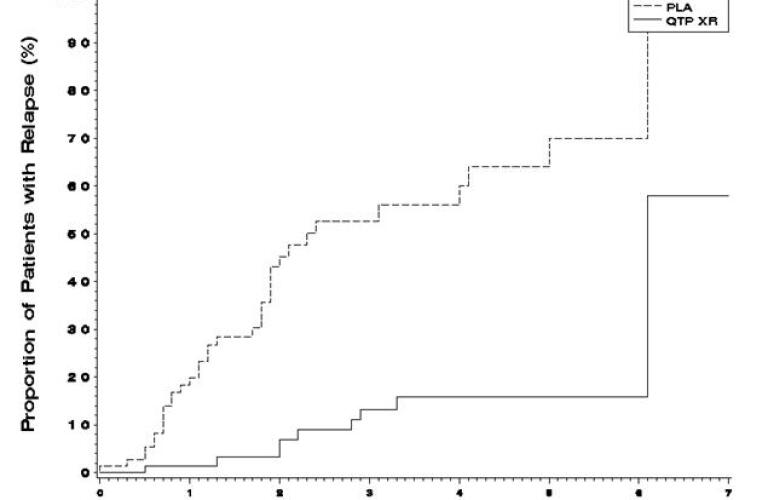
PLA Placebo. QTP Quetiapine. XR Extended-release.
Noot: resultaten zijn van de tussentijdse analyse.
bipolaire stoornis
Bipolaire stoornis type I, manische of gemengde episoden
Volwassenen
De werkzaamheid van SEROQUEL XR bij de acute behandeling van manische episoden werd vastgesteld in één 3 weken durende, placebogecontroleerd onderzoek (Studie 1 in Tabel 27) bij patiënten die voldeden aan de DSM-IV-criteria voor bipolaire stoornis type I met manische of gemengde episoden met of zonder psychotische kenmerken (N=316). De patiënten werden ten tijde van de randomisatie minimaal 4 dagen in het ziekenhuis opgenomen. Patiënten gerandomiseerd naar SEROQUEL XR kregen 300 mg op dag 1 en 600 mg op dag 2. Daarna kon de dosis worden aangepast tussen 400 mg en 800 mg per dag.
Het primaire beoordelingsinstrument dat werd gebruikt voor het beoordelen van manische symptomen in deze onderzoeken was de Young Mania Rating Scale (YMRS), een 11-item clinicus-gerelateerde schaal die traditioneel wordt gebruikt om de mate van manische symptomen te beoordelen in een bereik van 0 (geen manische kenmerken) tot 60 (maximale score). SEROQUEL XR was superieur aan placebo wat betreft de vermindering van de YMRS-totaalscore in week 3.
De werkzaamheid van SEROQUEL bij de behandeling van acute manische episoden werd ook vastgesteld in 3 placebogecontroleerde onderzoeken bij patiënten die voldeden aan de DSM-IV-criteria voor bipolaire stoornis type I met manische episoden. Deze onderzoeken includeerden patiënten met of zonder psychotische kenmerken en sloten patiënten met rapid cycling en gemengde episoden uit. Van deze onderzoeken waren er 2 monotherapie (12 weken) en 1 adjunctietherapie (3 weken) met lithium of divalproex. De belangrijkste uitkomsten van deze onderzoeken waren de verandering in de YMRS-score ten opzichte van de uitgangswaarde na 3 en 12 weken voor monotherapie en na 3 weken voor aanvullende therapie. Adjunct therapie wordt gedefinieerd als de gelijktijdige start of daaropvolgende toediening van SEROQUEL met lithium of divalproex.
De resultaten van de proeven volgen:
Monotherapie
In twee 12 weken durende proeven (n=300, n=299) waarin SEROQUEL werd vergeleken met placebo, was SEROQUEL superieur aan placebo wat betreft de vermindering van de YMRS-totaalscore op week 3 en 12. De meerderheid van de patiënten in deze onderzoeken die SEROQUEL innamen, werd gedoseerd in een bereik tussen 400 mg/dag en 800 mg/dag (onderzoeken 2 en 3 in tabel 27).
Aanvullende therapie
In een placebogecontroleerde studie van 3 weken werden 170 patiënten met bipolaire manie (YMRS ≥20) gerandomiseerd om SEROQUEL of placebo te ontvangen als aanvullende behandeling bij lithium of divalproex. Patiënten kunnen al dan niet een adequate behandelingskuur van lithium of divalproex hebben gekregen voorafgaand aan de randomisatie. SEROQUEL was superieur aan placebo wanneer het werd toegevoegd aan lithium of divalproex alleen voor de vermindering van de YMRS-totaalscore. De meerderheid van de patiënten in deze proef die SEROQUEL innamen, werd gedoseerd tussen 400 mg/dag en 800 mg/dag (studie 4 in tabel 27).
Kinderen en adolescenten (leeftijd 10-17)
De werkzaamheid van SEROQUEL XR bij de acute behandeling van manische episoden geassocieerd met bipolaire stoornis type I bij kinderen en adolescenten (10 – 17 jaar) werd geëxtrapoleerd uit een 3-weeks, dubbelblind, placebogecontroleerd, multicenteronderzoek. Patiënten die voldeden aan de DSM-IV diagnostische criteria voor een manische episode werden gerandomiseerd naar een van de drie behandelingsgroepen: SEROQUEL 400 mg/dag (n=95), SEROQUEL 600 mg/dag (n=98), of placebo (n=91). De studiemedicatie werd gestart met 50 mg/dag en op dag 2 verhoogd tot 100 mg/dag (verdeelde doses, twee- of driemaal daags). Vervolgens werd de dosis getitreerd tot een streefdosis van 400 mg/dag of 600 mg/dag met stappen van 100 mg/dag, in verdeelde doses twee- of driemaal daags. De primaire variabele voor de werkzaamheid was de gemiddelde verandering ten opzichte van de uitgangswaarde in de totale YMRS-score. SEROQUEL 400 mg/dag en 600 mg/dag waren superieur aan placebo wat betreft de vermindering van de totale YMRS-score (studie 5 in tabel 27).
|
Study Number |
Treatment Group |
Primary Efficacy Measure: YMRS Totaal |
|||
|
Gemiddelde uitgangsscore (SD) Gemiddelde uitgangsscore van gegevens over volwassenen is gebaseerd op patiënten die in de primaire analyse zijn opgenomen; gemiddelde uitgangsscore bij kinderen is gebaseerd op alle patiënten in de ITT-populatie.
|
LS Gemiddelde verandering vanaf uitgangswaarde (SE) |
Placebo-subtracted Difference In de studie opgenomen als een actieve comparator.
(95% CI) |
|||
|
Studie 1 |
SEROQUEL XR (400-800 mg/dag) Doses die statistisch significant beter zijn dan placebo.
|
28,8 (5,4) |
-14,3 (0,9) |
-3,8 (-5,7, -2,0) |
|
|
Placebo |
28.4 (5,1) |
-10,5 (0,9) |
|||
|
Studie 2 |
SEROQUEL (200-800 mg/dag) |
34.0 (6,1) |
-12,3 (1,3) |
-4,0 (-7,0, -1,0) |
|
|
Haloperidol |
32.3 (6,0) |
-15,7 (1,3) |
-7,4 (-10,4, -4,4) |
||
|
Placebo |
33,1 (6.6) |
-8,3 (1,3) |
|||
|
Studie 3 |
SEROQUEL (200-800 mg/dag) |
32,7 (6.5) |
-14.6 (1.5) |
-7.9 (-10.9, -5.0) |
|
|
Lithium |
33,3 (7,1) |
-15.2 (1,6) |
-8,5 (-11,5, -5,5) |
||
|
Placebo + stemmingsstabilisator |
34,0 (6,9) |
-6.7 (1,6) |
|||
|
Studie 4 |
SEROQUEL (200-800 mg/dag) + stemmingsstabilisator |
31.5 (5.8) |
-13.8 (1.6) |
-3.8 (-7.1, -0.6) |
|
|
Placebo + stemmingsstabilisator |
31.1 (5.5) |
-10 (1.5) |
|||
|
Studie 5 (kinderen en adolescenten) |
SEROQUEL (400 mg/dag) |
29.4 (5.9) |
-14.3 (0.96) |
-5.2 (-8.1, -2.3) |
|
|
SEROQUEL (600 mg/dag) |
29,6 (6,4) |
-15,6 (0,97) |
-6,6 (-9,5, -3.7) |
||
|
Placebo |
30,7 (5,9) |
-9,0 (1., 1,97) |
-9,0 (1., 1,97) |
.1) |
|
|
Stemmingsstabilisator: lithium of divalproex; SD: standaardafwijking; SE: standaardafwijking; LS Mean: kleinste kwadraten gemiddelde; CI: ongecorrigeerd betrouwbaarheidsinterval. |
|||||
Bipolaire stoornis, depressieve episoden
Volwassenen
De werkzaamheid van SEROQUEL XR voor de acute behandeling van depressieve episoden die gepaard gaan met bipolaire stoornis bij patiënten die voldeden aan de DSM-IV-criteria voor bipolaire stoornis werd vastgesteld in één 8 weken durende, gerandomiseerd, dubbelblind, placebogecontroleerd onderzoek (N=280 poliklinische patiënten). Deze studie omvatte patiënten met bipolaire stoornissen van het type I en II, en patiënten met en zonder een “rapid cycling”-verloop. Patiënten gerandomiseerd naar SEROQUEL XR kregen 50 mg toegediend op dag 1, 100 mg op dag 2, 200 mg op dag 3, en 300 mg op dag 4 en daarna.
Het primaire beoordelingsinstrument dat werd gebruikt om depressieve symptomen te beoordelen, was de Montgomery-Asberg Depression Rating Scale (MADRS), een 10-item schaal beoordeeld door een clinicus met scores variërend van 0 (geen depressieve kenmerken) tot 60 (maximale score). Het primaire eindpunt was de verandering ten opzichte van de uitgangsscore in MADRS-score op week 8. SEROQUEL XR was superieur aan placebo wat betreft de vermindering van de MADRS-score op week 8 (studie 6 in tabel 28).
De werkzaamheid van SEROQUEL voor de behandeling van depressieve episoden geassocieerd met bipolaire stoornis werd vastgesteld in 2 identieke 8 weken durende, gerandomiseerde, dubbelblinde, placebogecontroleerde studies (N=1045). Deze studies omvatten patiënten met bipolaire stoornis type I of II en patiënten met of zonder een “rapid cycling”-verloop. Patiënten die werden gerandomiseerd naar SEROQUEL kregen eenmaal daags een vaste dosis van hetzij 300 mg of 600 mg toegediend.
Het primaire beoordelingsinstrument dat in deze studies werd gebruikt om depressieve symptomen te beoordelen, was de MADRS. Het primaire eindpunt in beide studies was de verandering ten opzichte van de uitgangswaarde in MADRS-score op week 8. In beide studies was SEROQUEL superieur aan placebo wat betreft de vermindering van de MADRS-score op week 8 (studies 7 en 8 in tabel 28). In deze onderzoeken werd geen extra voordeel gezien met de dosis van 600 mg. Voor de 300 mg dosisgroep werden statistisch significante verbeteringen ten opzichte van placebo gezien in de algehele kwaliteit van leven en tevredenheid met betrekking tot verschillende gebieden van functioneren, zoals gemeten met de Q-LES-Q(SF).
|
Studie Nummer |
Behandelingsgroep |
Primaire Doeltreffendheidsmeting: MADRS Totaal |
||||
|
Gemiddelde Baseline Score (SD) |
LS Gemiddelde Verandering vanaf Baseline (SE) |
Placebo-afgetrokken Verschil Verschil (geneesmiddel min placebo) in kleinste kwadraten gemiddelde verandering vanaf baseline.
(95% CI) |
||||
|
Studie 6 |
SEROQUEL XR (300 mg/dag) Doses die statistisch significant beter zijn dan placebo.
|
29.8 (5.2) |
-17.4 (1.2) |
-5.5 (-7.9, -3.2) |
||
|
Placebo |
30.1 (5.5) |
-11.9 (1,2) |
||||
|
Studie 7 |
SEROQUEL (300 mg/dag) |
30.3 (5.0) |
-16.4 (0.9) |
-6.1 (-8.3, -3,9) |
||
|
SEROQUEL (600 mg/dag) |
30.3 (5.3) |
-16.7 (0.9) |
-6.5 (-8.7, -4.3) |
|||
|
Placebo |
30,6 (5,3) |
-10,3 (0.9) |
||||
|
Studie 8 |
SEROQUEL (300 mg/dag) |
31.1 (5,7) |
-16,9 (1,0) |
-5,0 (-7,3, -2,7) |
||
|
SEROQUEL (600 mg/dag) |
29,9 (5.6) |
-16.0 (1.0) |
-4.1 (-6.4, -1.8) |
|||
|
Placebo |
29.6 (5.4) |
-11.9 (1.0, 1.0) |
-11.9 (1.0, 1.0) |
-16.0 (1.0).0) |
||
|
SD: standaardafwijking; SE: standaardfout; LS Mean: kleinste kwadraten gemiddelde; CI: ongecorrigeerd betrouwbaarheidsinterval. |
||||||
Maintenance Treatment as an Adjunct to Lithium or Divalproex
De werkzaamheid van SEROQUEL bij de onderhoudsbehandeling van bipolaire stoornis type I werd vastgesteld in 2 placebogecontroleerde onderzoeken bij patiënten (n=1326) die voldeden aan de DSM-IV-criteria voor bipolaire stoornis type I (onderzoeken 9 en 10). De onderzoeken omvatten patiënten bij wie de meest recente episode manisch, depressief of gemengd was, met of zonder psychotische kenmerken. In de open-label fase moesten de patiënten stabiel zijn op SEROQUEL plus lithium of divalproex gedurende ten minste 12 weken om te kunnen worden gerandomiseerd. Gemiddeld waren de patiënten 15 weken gestabiliseerd. In de randomisatiefase werden de patiënten verder behandeld met lithium of divalproex en werden zij gerandomiseerd naar SEROQUEL (tweemaal daags toegediend met een totaal van 400 mg/dag tot 800 mg/dag) of placebo. Ongeveer 50% van de patiënten was gestopt met de SEROQUEL-groep tegen dag 280 en 50% van de placebogroep was gestopt tegen dag 117 van de dubbelblinde behandeling. Het primaire eindpunt in deze studies was de tijd tot het opnieuw optreden van een “mood event” (manische, gemengde of depressieve episode). Een stemmingsstoornis werd gedefinieerd als medicatie-initiatie of ziekenhuisopname voor een stemmingsepisode; YMRS-score ≥20 of MADRS-score ≥20 bij 2 opeenvolgende beoordelingen; of stopzetting van de studie als gevolg van een stemmingsstoornis.
In beide studies was SEROQUEL superieur aan placebo wat betreft het verhogen van de tijd tot het terugkeren van een stemmingsevenement (Figuur 2 en Figuur 3). Het behandelingseffect was aanwezig voor het verhogen van de tijd tot herval van zowel manische als depressieve episoden. Het effect van SEROQUEL was onafhankelijk van enige specifieke subgroep (toegewezen stemmingsstabilisator, geslacht, leeftijd, ras, meest recente bipolaire episode, of rapid cycling beloop).
Figuur 2: Kaplan-Meier Curves van de tijd tot het opnieuw optreden van een stemmingsgebeurtenis (Studie 9)
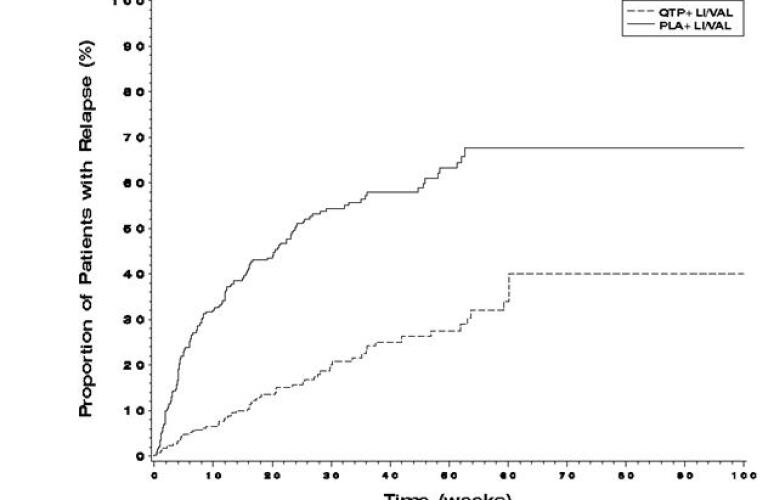
Figuur 3: Kaplan-Meier Curves van de tijd tot het opnieuw optreden van een stemmingsgebeurtenis (Studie 10)
major depressive disorder, adjunctive therapy to antidepressants
De werkzaamheid van SEROQUEL XR als adjunctieve therapie naast antidepressiva bij de behandeling van MDD werd aangetoond in twee placebogecontroleerde, vast gedoseerde onderzoeken van 6 weken (n=936). SEROQUEL XR 150 mg/dag of 300 mg/dag werd gegeven als aanvullende therapie bij een bestaande antidepressivumtherapie bij patiënten die eerder een inadequate respons op ten minste één antidepressivum hadden vertoond. SEROQUEL XR werd toegediend als 50 mg/dag op dag 1 en 2, en verhoogd tot 150 mg/dag op dag 3 voor beide dosisgroepen. Op dag 5 werd de dosis verhoogd tot 300 mg/dag in de 300 mg/dag vast gedoseerde groep. Inadequate respons werd gedefinieerd als het hebben van aanhoudende depressieve symptomen voor de huidige episode ondanks het gebruik van een antidepressivum gedurende 6 weken op of boven de minimaal effectieve op het etiket vermelde dosis. De gemiddelde HAM-D totaalscore bij binnenkomst was 24, en 17% van de patiënten scoorde 28 of hoger. Patiënten gebruikten verschillende antidepressiva voordat ze aan de studie deelnamen, waaronder SSRI’s (paroxetine, fluoxetine, sertraline, escitalopram, of citalopram), SNRI’s, (duloxetine en venlafaxine,) TCA’s (amitriptyline), en andere (bupropion).
Het primaire eindpunt in deze onderzoeken was verandering van uitgangswaarde tot week 6 in de Montgomery-Asberg Depression Rating Scale (MADRS.), SEROQUEL XR 300 mg eenmaal daags als aanvullende behandeling bij een andere antidepressivumtherapie was superieur aan het antidepressivum alleen in vermindering van de MADRS-totaalscore in beide onderzoeken. SEROQUEL XR 150 mg eenmaal daags als aanvullende behandeling was superieur aan antidepressivum alleen wat betreft vermindering van de MADRS-totaalscore in één onderzoek (onderzoek 1 en 2 in tabel 29).
|
Study Number |
Treatment Group |
Primary Efficacy Measure: MADRS Totaal |
||||
|
Gemiddelde Baseline Score (SD) |
LS Gemiddelde Verandering vanaf Baseline (SE) |
Placebo-afgetrokken Verschil Verschil (geneesmiddel min placebo) in kleinste kwadraten gemiddelde verandering vanaf baseline.
(95% CI) |
||||
|
Studie 1 |
SEROQUEL XR (150 mg/dag) + AD |
27,2 (5,2) |
-13,6 (0.8) |
-1,9 (-3,9, 0,1) |
||
|
SEROQUEL XR (300 mg/dag) Doses die statistisch significant beter zijn dan placebo.
+ AD |
27,6 (5,0) |
-14,7 (0,8) |
-3,0 (-5,0, -1.0) |
|||
|
Placebo + AD |
27.6 (5.5) |
-11.7 (0.8) |
-14.7 (0.8) |
-14.7 (0.8).7 (0,8) |
||
|
Studie 2 |
SEROQUEL XR (150 mg/dag) + AD |
28.6 (5.4) |
-15.3 (0.7) |
-3.1 (-4.9, -1.2) |
||
|
SEROQUEL XR (300 mg/dag) + AD |
28,4 (5,5) |
-14.9 (0,7) |
-2,7 (-4,6, -0,8) |
|||
|
Placebo |
28.2 (5.6) |
-12.2 (0.7) |
||||
|
AD: Antidepressivum; SD: standaarddeviatie; SE: standaardafwijking; LS Mean: kleinste kwadraten gemiddelde; CI: ongecorrigeerd betrouwbaarheidsinterval. |
||||||
Geef een antwoord