このシリーズのPart I、Part II、Part III、Part IVでは、以下の6つのコンセプトを取り上げました:
#1 – コレステロールとは何ですか?
#2 – 私たちが食べるコレステロールと体内のコレステロールの関係は?
#3 – コレステロールは悪者?
#4 – コレステロールはどのように体内を移動するか?
#6 – コレステロールは実際にどのような問題を引き起こすのか?
必要に応じて、以前の記事から得られるポイントを簡単に復習しましょう:
- コレステロールは体内の「単なる」有機分子ですが、興味深い違いがあります:食べる、作る、貯蔵する、排出するなど、すべて異なる量になっています。
- 私たちの体内にあるコレステロールのプールは、生命維持に不可欠です。
- コレステロールには、未エステル化または「遊離」(UC)とエステル化(CE)の2つの形態があり、その形態によって、吸収できるかどうか、貯蔵できるかどうか(他の要因も含めて)が決まります。 これは吸収されず、私たちの腸から排泄される(つまり、便として体外に排出される)。
- 体内で合成されたコレステロール(すなわち、内因性産生コレステロール)の再吸収が、体内のコレステロールの主な供給源となっているのです。 つまり、体内のコレステロールのほとんどは、私たちの体内でつくられたものなのです。
- コレステロールを調節するプロセスは非常に複雑で、何重にもコントロールされています。 今回は吸収のほうにしか触れていませんが、合成のほうも複雑で、高度な制御が行われています。 合成と吸収が非常に相互に関連していることがわかります。
- コレステロールを食べても、体内のコレステロール値にはほとんど影響がありません。 これは事実であり、私の意見ではありません。 これと異なることを言う人は、せいぜいこのトピックについて無知なのです。 最悪の場合、彼らは意図的な詐欺師です。 数年前、カナダのガイドラインは食事性コレステロールの制限を撤廃しました。 他の国々、特にアメリカはこれに追いつく必要がある。 このトピックに関する重要な参考文献は、こちらをご覧ください。
- コレステロールとトリグリセリドは血漿に溶けない(つまり
- 私たちの体のどこにでも、たとえば肝臓から冠動脈に運ばれるためには、リポタンパク質と呼ばれる特別なタンパク質に包まれた輸送体によって運ばれる必要があります。
- リポタンパク質という「船」が肝臓を出るとき、成熟プロセスを経て、遊離脂肪酸という形でトリグリセリドの「荷物」の多くを捨て、より小さく、より豊富なコレステロールを含むようになるのです。 その中で最も重要なのは、VLDL、IDL、LDL粒子に存在するアポBクラスと、ほとんどの場合HDL粒子に存在するアポA-Iクラスである。
- 血漿中のコレステロールの輸送は、肝臓と小腸から末梢に向かって、そして肝臓と小腸(「腸」)に戻るという両方向に起こります。
- アポBを含む粒子の主な機能は、筋肉にエネルギー(トリグリセリド)を、すべての細胞にリン脂質を輸送することです。 そのコレステロールは肝臓に輸送される。 アポA-Iを含む粒子は、コレステロールをステロイド生成組織、脂肪細胞(コレステロールエステルの貯蔵器官)へ輸送し、最終的には肝臓、腸、ステロイド生成組織へ戻ります。
- すべてのリポタンパク質は、ヒト脂質輸送システムの一部で、脂質を効率よく輸送するために調和して働いています。
- 現在、米国では(そして世界でも)ほとんどの人が、TC、TG、HDL-Cのみを直接測定する「標準」リピッド パネルを受けています。
- LDL-Cを直接測定する、より高度なコレステロール測定検査も存在します(ただし、標準化されたものはありません)。
- LDL粒子の数を数えることができる最も頻繁に使用され、ガイドラインで推奨されている検査は、NMR LipoProfileの一部であるアポリポ蛋白BまたはLDL-P NMRのいずれかである。 NMRは、LDLやその他のリポタンパク質粒子のサイズも測定できるため、グルコースやインスリン値に変化が見られる前に、薬剤未使用の患者におけるインスリン抵抗性を予測するのに有効である。
- このプロセスでは炎症が重要な役割を果たしますが、内皮への侵入と内皮内での保持がプロセスを推進するのです。 しかし、Lp(a)やapoB含有リポタンパク質も、特にインスリン抵抗性の人では役割を果たしています。
- 動脈硬化を止めたければ、LDL粒子数を下げなければなりません。
コンセプト#7 – LDL粒子の大きさは重要か
脂質学でこれほど混乱と議論を生む話題はそうそうないと思います。 私は今月ずっとこの問題に取り組んできましたので、この問題を正面から取り上げる時が来たのだと思います。 私はこのテーマについて多くの論文を読み、多くの講演を見てきましたが、中でも私の心を捉えたのは、ワシントンDCで開催されたADA第66回学術集会でのJim Otvosの講演でした。 この投稿で使用している図のいくつかは、彼の講演やその後の議論から直接、または改変して引用しています。
この議論の冒頭で、心に留めておくべき 2 つの臨床シナリオを指摘したいと思います。 このような患者は皆LDL粒子が大きいのですが、粒子数を減らす薬で治療しないと、ほとんどが小児期か成人期早期に死亡します。
共通点は(1)と(2)の患者のセットは両方とも高いLDL-Pを持っているということです。 今日お見せしようとするのは、粒子数を調整すると、粒子径は心血管リスクと統計的に有意な関係を持たないということです。
「パターンA」対「パターンB」LDL
約30年前にグラジエントゲル電気泳動法が登場したことが、人々がLDL粒子の大きさに関心を持つきっかけとなりました。 次の2つのシナリオのうち、他の条件がすべて同じであれば、一方がより高いリスクを持つことを実証した過去25年間の研究には事欠かない。 .
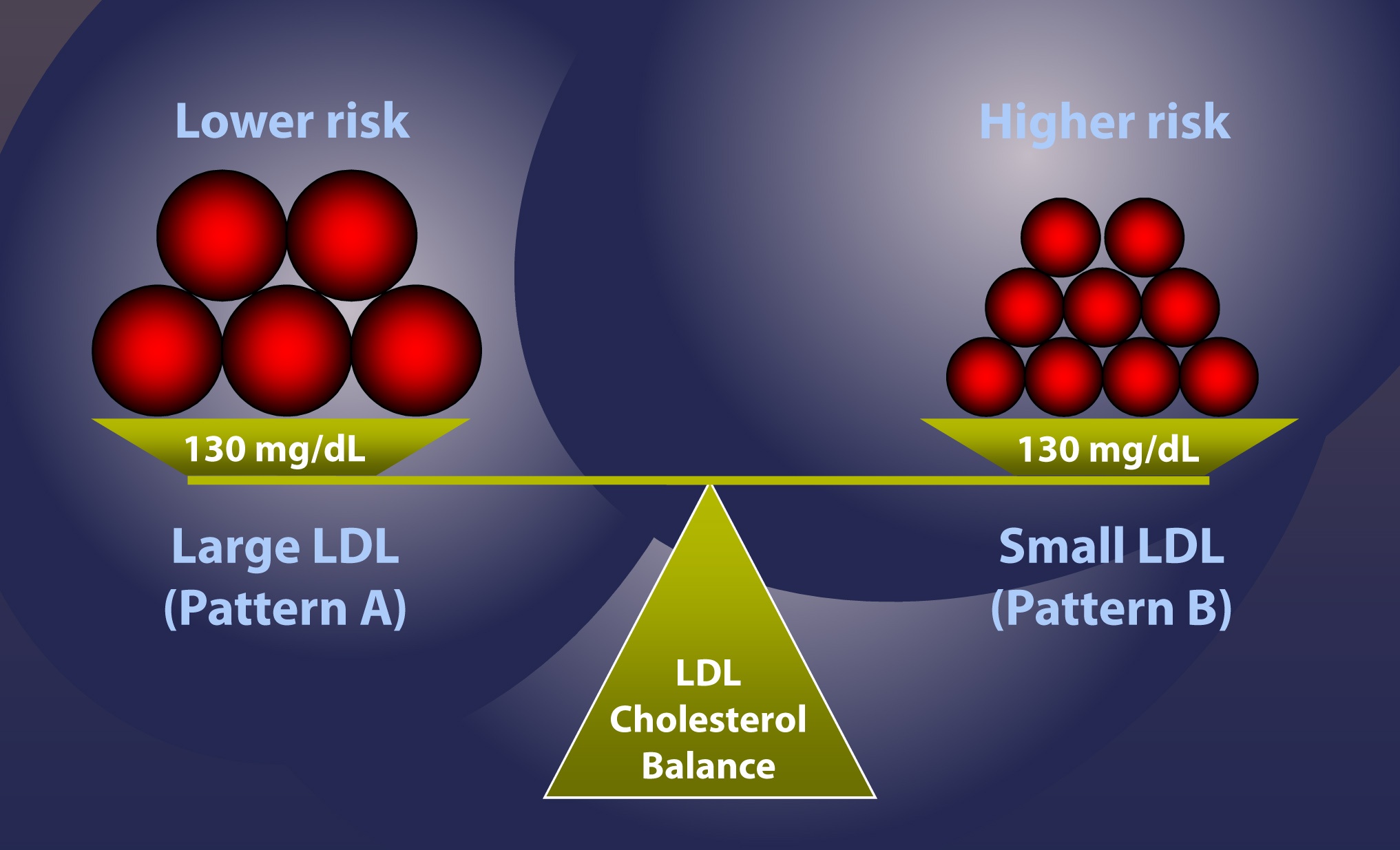
ここで例を挙げよう。 2人の患者を考えてみましょう。どちらもLDL粒子内のコレステロールの総量は同じで、たとえば130 mg/dLです。 さらに、それぞれが中核となるコレステロールエステルとトリグリセリドの比率が「理想的」であるとします(このシリーズの第1回と第3回を思い出してください、この比率は4:1です)。 この仮定がおそらく正しいのと同じくらい間違っている理由は、この後の記事で説明するつもりですが、簡単にするために、幾何学的な点を挙げたいと思います。
- LDL-C=130mg/dL、パターンA(大粒子)-下図左の人
- LDL-C=130mg/dL、パターンB(小粒子)-下図右の人
これまで並べてきた一連の仮定では、2のケースがよりリスクが高いと言えるでしょう。 つまり、LDL粒子内のコレステロール濃度が同じで、CEとTGの比率が同じだと仮定すると、右の人、ケース2の方が粒子が多く、したがってリスクも高いことが数学的に必要なのです。 本当に知らなければならないのは、LDL粒子1つにつき、いくつのコレステロール分子があるかということです。 血漿中のコレステロールを輸送するためには、コレステロールの多いLDL粒子よりも、コレステロールの少ないLDL粒子が常に必要であり、コレステロール分子の数は、サイズとコアTG含有量の両方に依存します。 粒子内のTGが多いほど、粒子内のコレステロールは少なくなります。
では、なぜ右側の人の方がリスクが高いのでしょうか? 粒子が多いからでしょうか? それとも、粒子が小さいからでしょうか。
これが、今日私が取り上げたい頸動脈の質問です。
- 小さいLDL粒子は、数に関係なく、大きいLDL粒子よりもアテローム性である。
- 粒子の大きさとは関係なく、粒子の数がアテローム性リスクを高めるものである。
- 大きさと数の両方が重要なので、右の人は「二重に」リスクがある。
- どちらの特徴も重要ではなく、これらの属性(つまり大きさと数)は、重要な他の何かの目印になるものだ。 これはそうするのに良い場所です。
私がまだLDL粒子が動脈硬化の原因物質であると納得していないのであれば、私が言うことは何も重要ではありませんから、今すぐ理由4の除外をするつもりです。 試験データは議論の余地のないものであり、現在、世界中でリスク評価のための粒子数測定を提唱する7つのガイドラインが存在します。 LDL粒子が多いほど、動脈硬化のリスクは高くなります。
しかし、理由1、2、3のどれが正しいか、どうすればわかるのでしょうか。
この図(この論争で最も有名なのひとつ)は、1997年にCirculationに掲載されたQuebec Cardiovascular Studyからのものです。 5033>
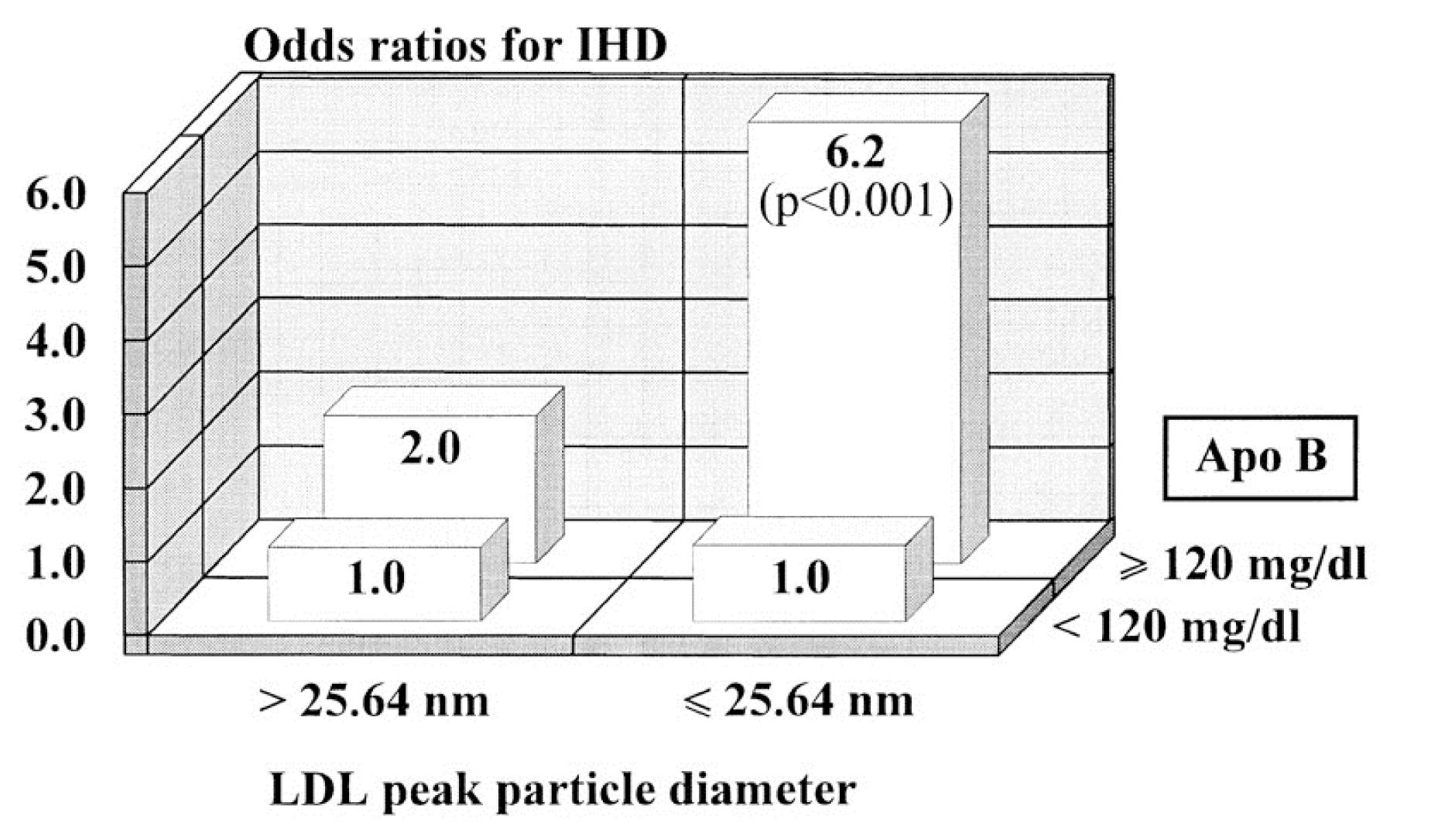

このグラフは、見慣れないとちょっと複雑なんですね。 これは相対リスクを示していますが、2次元のものです。 LDLサイズとapoB(LDL-Pの代理)の役割を見ているのです。 明らかなことは、LDL-Pが低い(すなわち、apoB < 120 mg/dl)患者では、サイズは重要でないことである。 ピークLDLの大きさに関係なく、いずれの場合も相対リスクは1.0である。 しかし、LDL粒子が多い患者(すなわち、apoB > 120 mg/dl)では、ピークLDLサイズが小さいほどリスクが高く、6.2倍になるようです。
この図だけを見ていると、サイズと数が独立してリスクを予測するという結論になりそうです(すなわち、上記の理由3)。 非論理的な結論ではありませんが…
しかし、あまり言及されていないのは、論文の本文です:
「脂質、リポ蛋白、アポリポ蛋白の変数の中で、アポBが多変量のステップワイズロジスティック分析で虚血性心疾患(IHD)リスクの最高かつ唯一の有意な予測因子として出てきた(P=.IHD)。002)。”
「IHDリスクに対するアポBレベルの寄与を考慮した後、連続変数としてのLDL-PDはIHDリスクに寄与しなかった」
連続変数とは何でしょう? 身長や体重のように、ある範囲の中で取り得る値が無限大にあるものです。 これに対して、「背が高い」「背が低い」のような、2つのカテゴリしかない離散的な変数です。 例えば、「身長が高い」を180cm以上と定義すると、世界の全人口は2つのバケツに分けられる。 背が低い人」(つまり身長6フィート未満の人)と「背が高い人」(つまり身長6フィート以上の人)である。 この図は、LDLの大きさを「大きい」「小さい」という離散的な変数のように示していますが、明らかにそうではありません。 これは連続変数であり、「大きい」「小さい」だけでなく、どのような値も取り得るということです。 この同じ分析をLDLの大きさを連続変数として行うと、大きさの影響はなくなり、アポB(つまりLDL-P)だけが問題になります。
この効果はその後も観察されており、有名なMESA (Multi-Ethnic Study of Atherosclerosis) 試験があります(こちらをご覧ください)。 MESA試験では、約5500人の男女を対象に、LDL-P、LDL-C、LDLサイズ、IMT(内膜中膜厚、動脈硬化の非侵襲的マーカー)、その他多くのパラメータ間の関連を数年間にわたって調査しました。
この研究では、上記の研究と同じような統計分析を使って、LDL-Pと粒子径の本当の役割を解析し、下の表にまとめました。 この表は、LDL-Pを考慮しない場合(すなわち「未調整」分析)、粒子径が1標準偏差増加すると、動脈硬化が20.9ミクロン減少することを示しており、粒子径が重要だと考える人なら予想されることです。 粒子が大きければ動脈硬化は少ない」
しかし、ここが重要なのですが、著者らがLDL粒子の数(黄色)で調整したところ、同じ現象は見られませんでした。 LDL粒子径が1標準偏差増加すると、ほとんど有意ではないものの、14.5ミクロンの動脈硬化が追加されました(p=0.05)
この点を繰り返しましょう。 LDL-Pを考慮すると、粒子径とアテローム性動脈硬化の関係はなくなってしまいます(そして、「間違った」方向、つまり、より大きな粒子、より多くのアテローム性動脈硬化に向かう傾向さえあるのです)。 年齢と性別を調整し、LDL-Pを調整しない場合、LDL粒子の数の変化(五分位で表示されるので、各グループは20%の割合で変化を示す)はIMT(すなわち動脈硬化)と関係がないようです。
しかしながら、小さいLDL-Pを調整すると、大きいLDL粒子の数が増えるとリスクが有意に増加することが明らかになります。
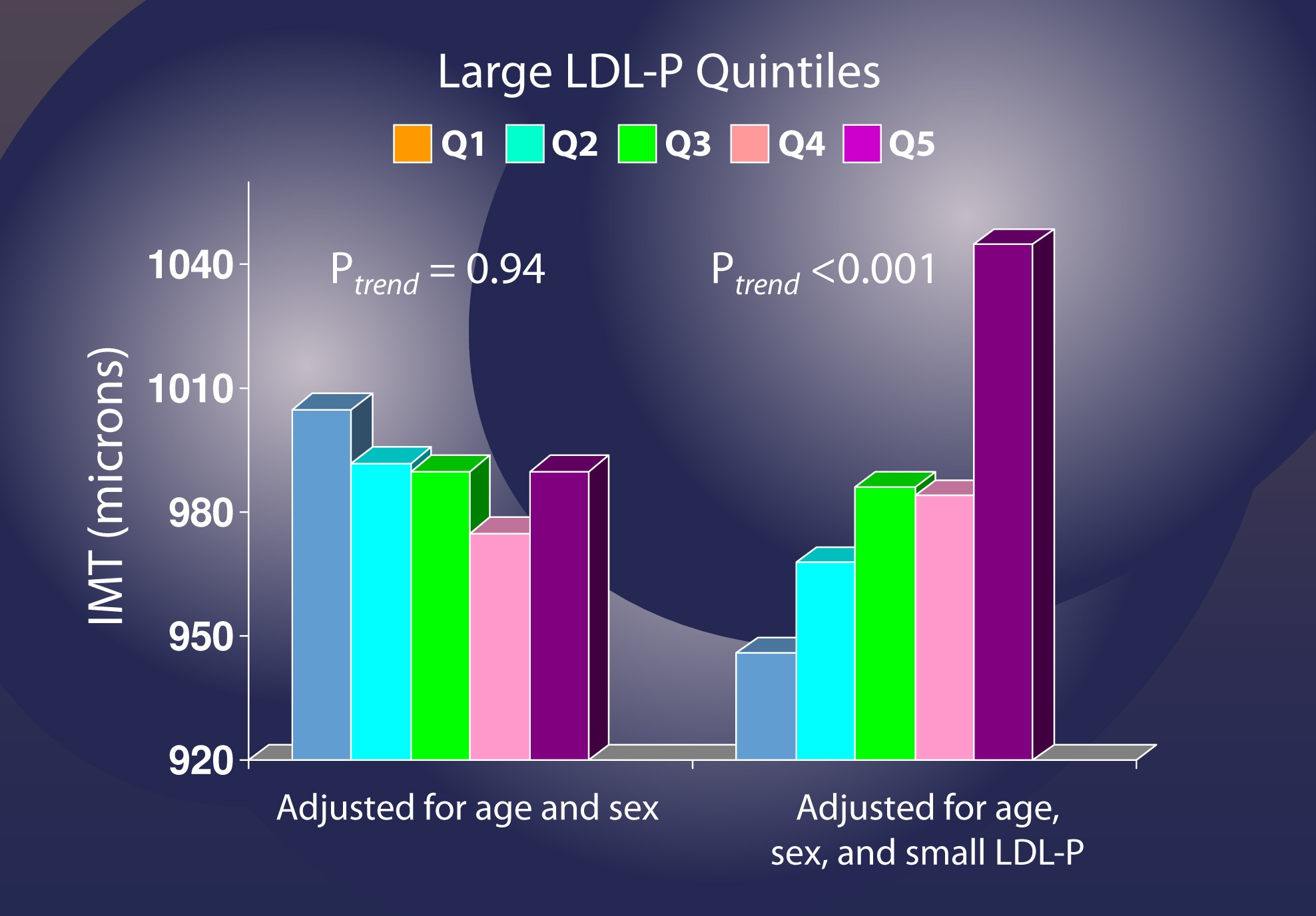

この問題に取り組む研究のほんの一部しかカバーしていませんが、この問題は今やかなり明確になっています。 小さなLDL粒子は大きなLDL粒子よりもアテローム性ではないのですが、交絡因子を除去することによってのみ、これが明らかになります。 つまり、この問題を取り上げたときに使った図を見返せば、理由2が正しいことがわかるはずです。
このことは、小さな粒子で歩いている「平均的な」人にはリスクがないことを意味しているわけではありません。
- 彼らの粒子の小ささは、おそらく他の何か(たとえば、LDL粒子内のトリグリセリドの高い輸送による代謝の狂い)のマーカーです。 来週は、皆さんが気になっているであろう、もう一つの疑問について取り上げます。 なぜLDL-PやapoBを測定する必要があるのでしょうか? なぜLDL-PやapoBを測定する必要があるのでしょうか。
まとめ
- 一見すると、LDL粒子が小さい患者は、LDL粒子の大きい患者よりも動脈硬化のリスクが高いように見えますが、すべての要素が同じです。 それゆえ、パターンAは「良い」、パターンBは「悪い」というこの考え方は、かなり普及しています。
- しかし、この疑問に答えるには、LDL-Pを一定に保ち、さらにLDLサイズを一定に保ちながら、心血管イベントまたは動脈硬化の直接のマーカー(IMTなど)の変化を見る必要があります。 そうして初めて、サイズとイベントの関係が消失していることがわかるのです。 重要なのはLDL粒子の数だけで、大きいか小さいか、あるいは混合しているかです。
- “A particle is a particle is a particle.”(粒子は粒子)。 数がわからなければリスクもわからない
。
- 彼らの粒子の小ささは、おそらく他の何か(たとえば、LDL粒子内のトリグリセリドの高い輸送による代謝の狂い)のマーカーです。 来週は、皆さんが気になっているであろう、もう一つの疑問について取り上げます。 なぜLDL-PやapoBを測定する必要があるのでしょうか? なぜLDL-PやapoBを測定する必要があるのでしょうか。
コメントを残す