Ben Valsler
Alles wat blinkt is geen goud,
maar al te vaak heb je dat horen zeggen.
Brian Clegg laat een andere kant zien,
van dwaas goud – ijzersulfide.
Brian Clegg
‘There’s gold in them thar hills!’ Of toch niet? Zoals de bijnaam ‘goud voor dwazen’ suggereert, vertoont het pyrietmineraal van ijzer-II-disulfide meer dan een terloopse gelijkenis met het edelmetaal. Met de eenvoudige formule FeS2, kan de kubische structuur van de verbinding resulteren in de productie van opmerkelijk effectief uitziende platonische vormen, zowel in scherp omrande kubussen als in dodecaëders die eruit zien alsof ze zijn vervaardigd, hoewel vaker de natuurlijke vorming resulteert in een minder duidelijk afgebakende structuur.

Bron: ©
In de kristallen van ijzerdisulfide komen zwavelatomen in paren voor, waarbij een van de vier zwavelbindingen verbonden is met een ander zwavelatoom. Deze bindingen worden bij verhitting verbroken, waardoor ijzer-II-sulfide – FeS – en zwavel ontstaan. Dit proces wordt gebruikt bij de productie van zwaveldioxide, zowel om het gas te gebruiken, bijvoorbeeld als bleekmiddel voor papier, als als de eerste stap voor de productie van zwavelzuur. Meer recent heeft de verbinding, die een halfgeleider is, een toepassing gevonden in lithium-ijzerbatterijen, waarbij de kathode is gemaakt van ijzerdisulfide: deze batterijen zijn spanningscompatibel met traditionele 1,5 volt cellen, maar gaan aanzienlijk langer mee dan alkaline equivalenten.

Bron: ©
Waarschijnlijk de vroegste toepassing van ijzerdisulfide was als alternatief voor vuursteen bij het slaan van vonken – vandaar de naam pyriet – en werd vaak op deze manier gebruikt in vroege pistolen. Het werd ook lange tijd gebruikt voor de productie van ijzersulfaat, van oudsher bekend als groene vitriool. IJzerdisulfide wordt soms nog steeds op deze manier gebruikt, zij het met meer gesofisticeerde mechanismen dan de traditionele aanpak waarbij een hoopje pyriet in de regen wordt achtergelaten en de vloeistof die ervan afdruipt wordt opgevangen.
Als het mineraal oxideert, geeft het een behoorlijke hoeveelheid warmte af, wat kan leiden tot explosies in kolenmijnen met een hoog zwavelgehalte. Deze neiging tot oxideren betekent echter niet dat ijzer II disulfide altijd opgesloten zit. Gepolijst pyriet wordt sinds de oudheid in juwelen gebruikt en de vrij donkere kristallen ervan (ze hebben zelden de glans van goud) waren bijzonder in de mode tussen het einde van de jaren 1700 en het begin van de twintigste eeuw.

Bron: ©
Marcasiet broche
Verwarrend genoeg worden juwelen van pyriet marcasietjuwelen genoemd – verwarrend omdat er een alternatief ijzer II disulfide mineraal bestaat dat marcasiet heet, waarbij de kubische structuur is uitgerekt tot wat bekend staat als een orthorhombische vorm. Deze vorm is minder geschikt voor het maken van edelstenen omdat hij brozer is en waarschijnlijk zal afbrokkelen. De naam van het juweel (in het Verenigd Koninkrijk vaak uitgesproken als ‘marca-seet’) stamt uit een tijd dat alle vormen van het mineraal bekend stonden als marcasiet.

Bron: ©
Marcasiet mineraal
Het ijzer II disulfide is echter lang niet de enige manier om ijzer en zwavel te combineren. Het veel minder fraai ogende ijzer II sulfide is een zwart gevlekte stof met een structuur die octahedraal is rond het ijzer. De verbinding ontstaat vrij vaak bij de afbraak van organisch materiaal, als zwart slib in moerassen of de donkere verkleuring van een overgekookte eierdooier.
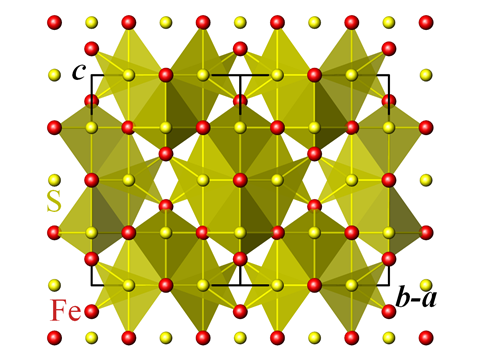
Bron: Perditax
Kristalstructuur van greigiet
Dit is nog maar het begin voor subtiele varianten van ijzersulfide. Mineralen bekend als greigiet, mackinawiet en pyrrhotiet hebben varianten van de structuur, terwijl het zwarte poeder van ijzer III sulfide – Fe2S3 – alleen ooit kunstmatig is geproduceerd. Greigiet komt voor in de eigenschappen van een pas in 1975 ontdekte groep zeebacteriën die het opmerkelijke vermogen bezitten zich te oriënteren naar het magnetisch veld van de aarde. Deze organismen, die “magnetotactische” bacteriën worden genoemd, hebben in hun cellen kristallen die grotendeels bestaan uit greigiet, het ijzersulfide-equivalent van het bekendste in de natuur voorkomende magnetische materiaal, het ijzeroxide magnetiet.

Bron: Raymond T. Downward, NASA
Geëtst oppervlak van de Mundrabilla-meteoriet, met rechtsonder, linksonder en linksboven een metallische ijzer-nikkel-legeringsfase van kamciet (38% Ni) en taeniet (6% Ni). Het donkere materiaal is een ijzersulfide (FeS of troiliet) met een parallel neerslag van duabreeliet (ijzer-chroom sulfide (FeCr2S4).
Van de alternatieve structuren is troiliet misschien wel het interessantst, een andere vorm van ijzersulfide met een hexagonale structuur. Hoewel dit af en toe wordt gevonden inheemse op aarde, het meest vaak opduikt in meteorieten – in het bijzonder de relatief zeldzame rassen die zijn ontstaan op de Maan en Mars voordat ze werden weggeblazen van het oppervlak in een impact uit de ruimte.

De naam troiliet werd gegeven ter ere van de Italiaanse priester Domenico Troili die in 1766 de eerste geregistreerde waarneming deed van een meteoor die resulteerde in een voorwerp dat de grond raakte. Troili dacht dat het belangrijkste materiaal van de meteoriet marcasiet was (wat waarschijnlijk pyriet betekent), maar bijna 100 jaar later identificeerde de Duitse mineraloog Gustav Rose de samenstelling van de meteoriet als een ander ijzersulfide en vernoemde het naar Troili.
Ironsulfide kan een last zijn. Het kan zich ophopen, bijvoorbeeld in olie- en gasbronnen, waardoor de buizen dichtslibben. Maar elders heeft het zijn waarde bewezen. Het mag dan een eenvoudige verbinding zijn van twee eenvoudige chemische elementen, en als pyriet een bedrieglijk nepgoud, maar in zijn gevarieerde vormen vertoont het een diversiteit en aanpassingsvermogen die zijn gebruikers allesbehalve gek maakt.
Ben Valsler
Dat was Brian Clegg in zijn verdediging van ijzersulfide. Volgende week, Mike Freemantle met kerosine, en een onconventionele vorm van oorlogsvoering.
Michael Freemantle
Op ongeveer een maand na de Japanse aanval op Pearl Harbor in december 1941, bedacht een Amerikaanse tandarts een plan om Japanse steden te verwoesten door kleine brandbommen aan vleermuizen te binden.
Ben Valsler
Zoek volgende keer uit wat er gebeurde in Project x-ray. Tot die tijd kun je [email protected] mailen of @chemistryworld tweeten als je verzoeken hebt voor verbindingen die we in de podcast moeten opnemen. Ik ben Ben Valsler, bedankt voor uw komst.
Geef een antwoord