14.8 Ethers
Leerdoelen
- Beschrijf het structuurverschil tussen een alcohol en een ether dat van invloed is op de fysische eigenschappen en de reactiviteit van elk.
- Noem eenvoudige ethers.
- Beschrijf de structuur en het gebruik van sommige ethers.
Met de algemene formule ROR′, een etherEen organische verbinding die een zuurstofatoom tussen twee koolwaterstofgroepen heeft. kan worden beschouwd als een derivaat van water waarin beide waterstofatomen zijn vervangen door alkyl- of arylgroepen. Het kan ook worden beschouwd als een derivaat van een alcohol (ROH) waarin het waterstofatoom van de OH-groep is vervangen door een tweede alkyl- of arylgroep:
HOH→H atomenreplace bothROR′←of OH groupreplace H atomROH
Eenvoudige ethers hebben eenvoudige algemene namen, gevormd uit de namen van de groepen die aan het zuurstofatoom vastzitten, gevolgd door de generieke naam ether. Bijvoorbeeld, CH3-O-CH2CH2CH3 is methyl propyl ether. Als beide groepen hetzelfde zijn, moet de groepsnaam worden voorafgegaan door het voorvoegsel di-, zoals in dimethylether (CH3-O-CH3) en diëthylether CH3CH2-O-CH2CH3.
Ethermoleculen hebben geen waterstofatoom op het zuurstofatoom (dat wil zeggen, geen OH-groep). Daarom is er geen intermoleculaire waterstofbinding tussen ethermoleculen, en daarom hebben ethers vrij lage kookpunten voor een gegeven molaire massa. Sterker nog, ethers hebben kookpunten die ongeveer gelijk zijn aan die van alkanen met vergelijkbare molaire massa en veel lager dan die van de overeenkomstige alcoholen (Tabel 14.4 “Vergelijking van kookpunten van alkanen, alcoholen en ethers”).
Tabel 14.4 “Vergelijking van kookpunten van alkanen, alcoholen en ethers”).4 Vergelijking van kookpunten van alkanen, alcoholen en ethers
| Gesamengevoegde structuurformule | Naam | Molaire massa | Kookpunt (°C) | Intermoleculaire waterstofbinding in zuivere vloeistof? |
|---|---|---|---|---|
| CH3CH2CH3 | propaan | 44 | -42 | geen |
| CH3OCH3 | dimethyl ether | 46 | -25 | geen |
| CH3CH2OH | ethylalcohol | 46 | 78 | ja |
| CH3CH2CH2CH3 | pentaan | 72 | 36 | geen |
| CH3CH2OCH2CH3 | diethylether | 74 | 35 | geen |
| CH3CH2CH2CH2OH | butylalcohol | 74 | 117 | ja |
Ethermoleculen hebben wel een zuurstofatoom, echter, en gaan waterstofbruggen aan met watermoleculen. Dientengevolge heeft een ether ongeveer dezelfde oplosbaarheid in water als de alcohol die er isomerisch mee is. Zo zijn dimethylether en ethanol (beide met de molecuulformule C2H6O) volledig oplosbaar in water, terwijl diëthylether en 1-butanol (beide C4H10O) nauwelijks oplosbaar zijn in water (8 g/100 mL water).
Voorbeeld 5
Wat is de gangbare naam voor elke ether?
- CH3CH2CH2OCH2CH2CH3
-
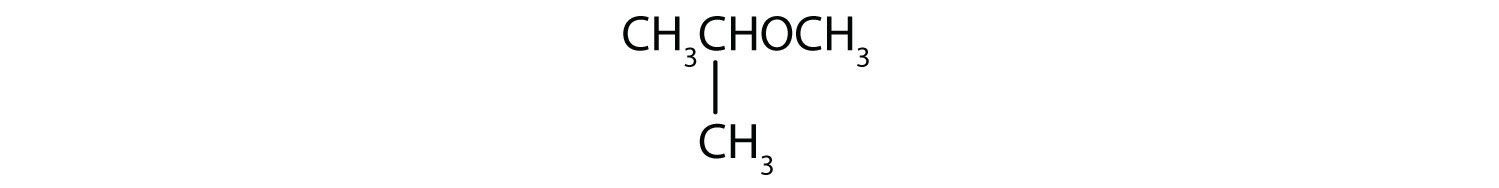
Oplossing
- De koolstofgroepen aan weerszijden van het zuurstofatoom zijn propylgroepen (CH3CH2CH2), dus de verbinding is dipropylether.
- De drie-koolstofgroepen zitten vast aan het middelste koolstofatoom, dus het is een isopropylgroep. De één-koolstofgroep is een methylgroep. De verbinding is isopropylmethylether.
Vaardigheids-oefening
-
CH3CH2CH2CH2OCH2CH2CH2CH3
-
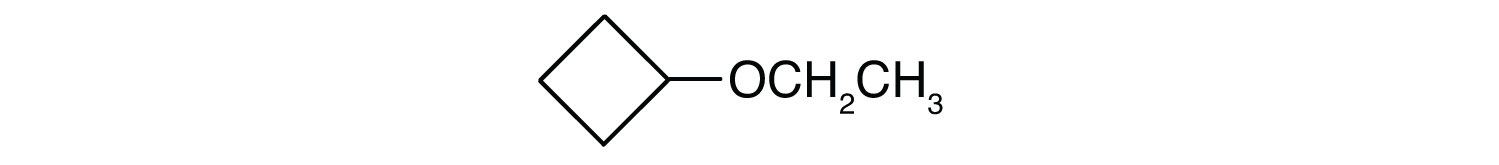
Wat is de gewone naam voor elke ether?
Voor uw gezondheid: Ethers as General Anesthetics
Een algemeen verdovingsmiddel werkt in op de hersenen en veroorzaakt bewusteloosheid en een algemene ongevoeligheid voor gevoel of pijn. Diethylether (CH3CH2OCH2CH3) was het eerste algemene verdovingsmiddel dat werd gebruikt.
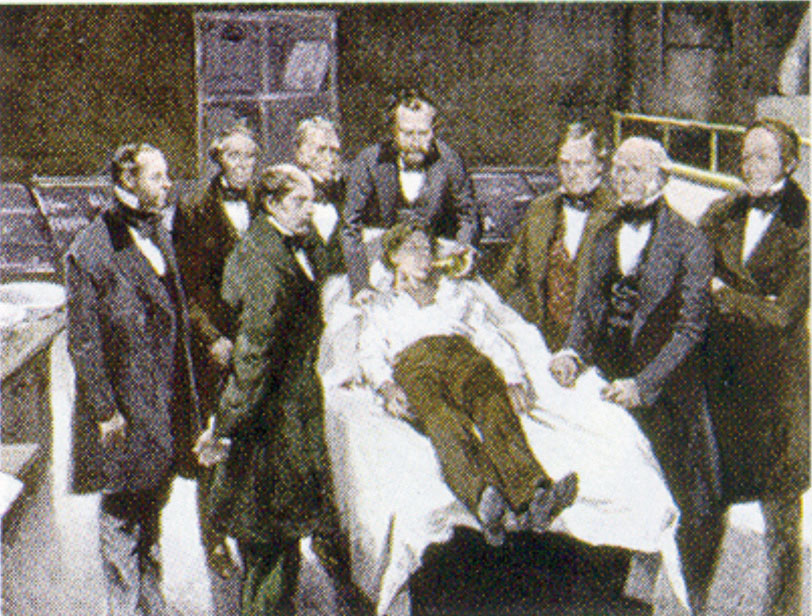
William Morton, een tandarts uit Boston, introduceerde diethylether in de chirurgische praktijk in 1846. Dit schilderij toont een operatie in Boston in 1846 waarbij diethylether als verdovingsmiddel werd gebruikt. Het inademen van etherdamp veroorzaakt bewusteloosheid door de activiteit van het centrale zenuwstelsel te onderdrukken.
Bron: Schilderij van William Morton door Ernest Board, uit http://commons.wikimedia.org/wiki/File:Morton_Ether_1846.jpg.
Diethylether is relatief veilig omdat er een vrij groot verschil is tussen de dosis die een effectief niveau van verdoving teweegbrengt en de dodelijke dosis. Omdat het echter zeer ontvlambaar is en bovendien het nadeel heeft dat het misselijkheid veroorzaakt, is het vervangen door nieuwere inhalatie-anesthetica, waaronder de fluorhoudende verbindingen halothaan, enfluraan en isofluraan. Helaas zijn er vraagtekens geplaatst bij de veiligheid van deze verbindingen voor operatiekamerpersoneel. Vrouwelijk operatiepersoneel dat aan halothaan wordt blootgesteld, krijgt bijvoorbeeld vaker een miskraam dan vrouwen in de algemene bevolking.
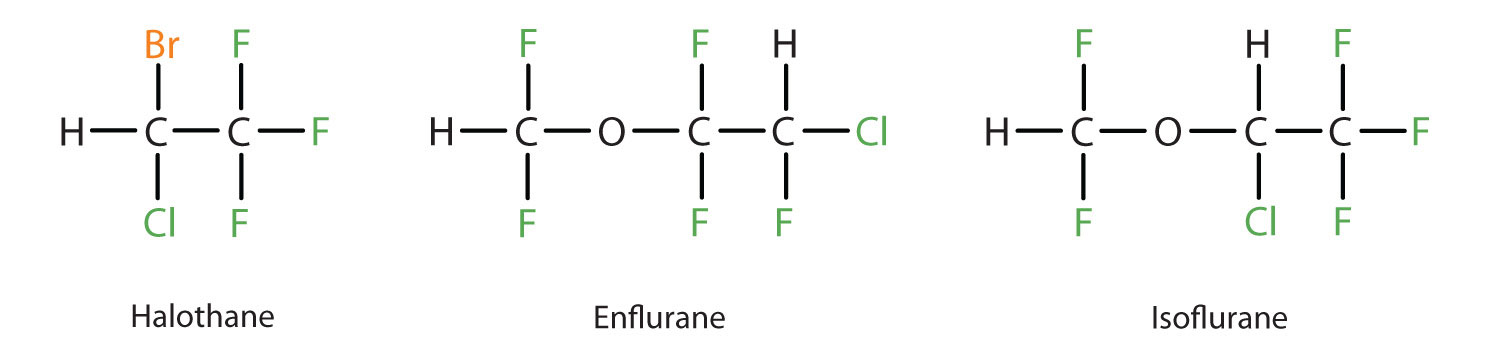
Deze drie moderne, inhalerende, halogeenhoudende, verdovingsmiddelen zijn minder ontvlambaar dan diethylether.
Oefeningen voor begripsherziening
-
Waarom heeft diethylether (CH3CH2OCH2CH3) een veel lager kookpunt dan 1-butanol (CH3CH2CH2CH2OH)?
-
Welke stof is beter oplosbaar in water-ethylmethylether (CH3CH2OCH3) of 1-butanol (CH3CH2CH2CH2OH)? Leg uit.
Antwoorden
-
Diethylether heeft geen intermoleculaire waterstofbruggen omdat er geen OH groep is; 1-butanol heeft een OH en gaat intermoleculaire waterstofbruggen aan.
-
Ethylmethylether (drie koolstofatomen, één zuurstofatoom) is beter oplosbaar in water dan 1-butanol (vier koolstofatomen, één zuurstofatoom), ook al kunnen beide een waterstofbrug aangaan met water.
Key Takeaways
- Om ethers gewone namen te geven, geef je gewoon de groepen die aan het zuurstofatoom vastzitten, gevolgd door de algemene naam ether. Als beide groepen hetzelfde zijn, moet de groepsnaam worden voorafgegaan door het voorvoegsel di-.
- Ethermoleculen hebben geen OH groep en dus geen intermoleculaire waterstofbinding. Ethers hebben daarom bij een gegeven molaire massa een vrij laag kookpunt.
- Ethermoleculen hebben een zuurstofatoom en kunnen waterstofbruggen aangaan met watermoleculen. Een ethermolecuul heeft ongeveer dezelfde oplosbaarheid in water als de alcohol die er isomerisch mee is.
Oefeningen
-
Hoe kan ethanol twee verschillende producten geven bij verhitting met zwavelzuur? Noem deze producten.
-
Welke van deze ethers is isomerisch met ethanol-CH3CH2OCH2CH3, CH3OCH2CH3, of CH3OCH3?
-
Noem elke verbinding.
- CH3OCH2CH2CH3
-
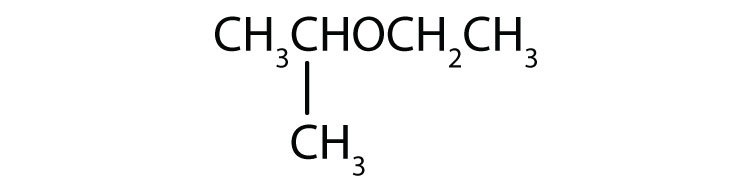
-
Noem elke verbinding.
- CH3CH2CH2CH2OCH3
- CH3CH2OCH2CH2CH3
-
Teken de structuur voor elke verbinding.
- methylether
- tert-butylether
-
Teken voor elke verbinding de structuur.
- diisopropylether
- cyclopropylpropylether
Antwoorden
-
Intramoleculaire (zowel de H als de OH komen van hetzelfde molecuul) dehydratie geeft ethyleen; intermoleculair (de H komt van één molecuul en de OH komt van een ander molecuul) dehydratie geeft diethylether.
-
- methylpropylether
- ethylisopropylether
-
- CH3OCH2CH3
-
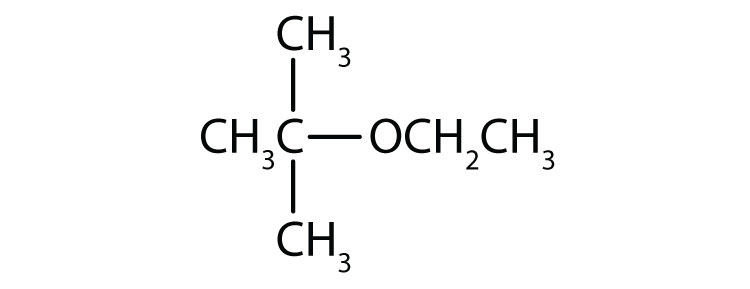
Geef een antwoord