Was haben DNA-Mini-Preps und Protein-Immunpräzipitationsexperimente gemeinsam? Sie beginnen unterschiedlich, aber sie enden mit demselben kritischen Schritt – der Elution. Aber was genau ist eine Elution, und wozu dient sie?
Die Terminologie
Zunächst ein paar grundlegende Begriffe:
Elution – Extraktion eines Materials aus einem anderen durch Waschen mit einem Lösungsmittel.
Das Adsorptionsmittel – eine feste Phase, die im Falle von Mini-Prep-Säulen ein Kieselgel sein kann, in der Regel aber Perlen, die kovalent an Antikörper oder andere Ligandenmoleküle gebunden werden können. „Feste Phase“ bedeutet nicht notwendigerweise eine Standsäule; es können auch Beads in einem Eppendorf sein, die leicht zu waschen sind.
Affinität – ein Maß für die Fähigkeit des Absorptionsmittels, das gewünschte Molekül zu binden (das, was eluiert werden soll). Je höher die Affinität der festen Phase für das Biomolekül der Wahl (BOC) ist, desto fester bindet das Molekül an sie. Die Bindung sollte jedoch nicht irreversibel sein, da dies die Elution unmöglich macht.
Eluent – ein Lösungsmittel, das BOC vom Adsorptionsmittel entfernt.
Eluat – das Lösungsmittel, das BOC enthält und vom Adsorptionsmittel entfernt wurde.
Materialvorbereitung
Vor der Elution muss das Molekül der Wahl absorbiert und gleichzeitig von Verunreinigungen befreit werden. Dies ist ein wesentlicher Schritt, denn die herkömmliche Weisheit besagt: „Garbage in, garbage out“. Auch wenn Sie ausgezeichnete Reagenzien für die Elution haben, wenn Ihre Probe jedoch zu viel von dem nicht verwandten Personal enthält (der wissenschaftliche Begriff ist „Gunk“), wird es das Adsorptionsmaterial verstopfen. Die Sättigung der festen Phase verhindert, dass Ihr BOC absorbiert wird, und verunreinigt das Eluat. Effektive Lyse- und Reinigungsschritte sind für den Erfolg Ihres Elutionsexperiments unerlässlich.
Es ist wichtig, das Volumen Ihres Vorabsorptionsmaterials zu bestimmen. Das Volumen des Lysats, das durch das Absorptionsmedium fließt, sollte 3 – 5 Volumina der Säule nicht überschreiten. Ein großes Lysatvolumen, das durch das Absorptionsmittel fließt, verlängert die Versuchsdauer und erhöht die Wahrscheinlichkeit, dass Gunk absorbiert wird. In vielen Fällen lohnt es sich, das anfängliche Lysatvolumen durch Filtration oder Fraktionierung zu verringern. Das Lysatvolumen bestimmt also die Größe der Säule.
Die Wahl des Adsorptionsmaterials hängt von der chemischen Zusammensetzung des Moleküls ab, das Sie interessiert. Bei der Absorption von Biomolekülen kommt es in der Regel zu mehr oder weniger spezifischen Wechselwirkungen zwischen dem Substrat und dem Molekül. So wird z. B. DNA auf Minisäulen aufgrund der ionischen Wechselwirkung zwischen negativ geladenen DNA-Phosphatgruppen und positiv geladenen Silikapartikeln absorbiert.
Proteine werden in der Regel auf Sepharose oder mit IgG beschichteten Magnetbeads adsorbiert.
Nach einer ersten Lysatanwendung darf Ihre Säule zu keinem Zeitpunkt austrocknen. Dies würde Ihr Molekül an das Absorptionsmittel „backen“ und die Integrität der Säule beeinträchtigen. Wenn Sie keine Zeit haben, das Experiment fortzusetzen, füllen Sie die Säule mit einem kompatiblen Puffer auf und stoppen Sie den Fluss.
Waschen
Das Waschen der festen Phase dient dazu, ein nicht verwandtes Material zu entfernen, während das Molekül von Interesse auf der Säule verbleibt. Die selektive Trennung wird häufig durch die Verwendung eines Puffers mit geringer Ionenstärke (z. B. mit niedriger Salzkonzentration) erreicht. Das Volumen des Waschpuffers sollte in etwa der Menge des Ausgangsmaterials entsprechen und mindestens 3-5 Volumina der Säule betragen.
Nachdem jedoch mehrere Volumina des Waschpuffers durch die Säule geflossen sind, werden die Verunreinigungen weggewaschen, und zusätzliches Waschen wird die Qualität Ihrer Präparation nicht verbessern. Außerdem verlieren Sie Ihr Zielmaterial.
Elution
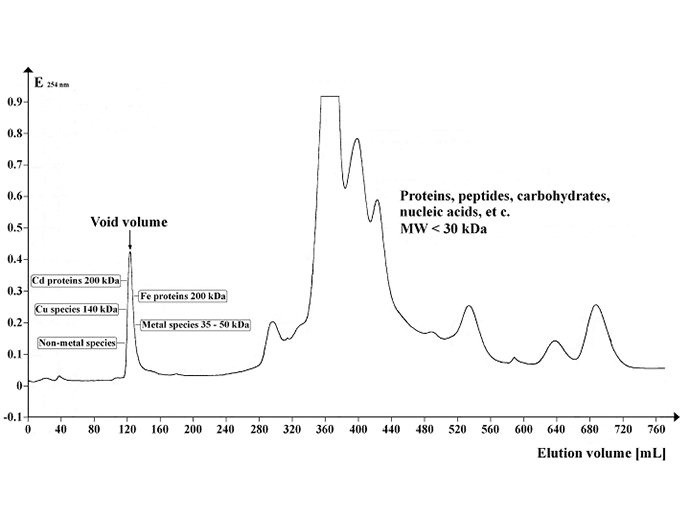
Bild: Chromatogramm des UV-Absorptionsprofils des Arabidopsis-Überstandes, getrennt auf Sephadex G-50 Superfine. Gelvolumen: 500 mL; Säulenlänge: 700 mm; Säulendurchmesser: 30 mm; Eluentenflussrate: 12 mL / Std.; Fraktionsvolumen: 8,0 mL; Anzahl der Fraktionen: 95; Probenvolumen: 5 mL; Trennungstemperatur: 4 °C; Elutionspuffer: 20 mM Tris-HCl, 1 mM NaN3; pH 8,0. Bildnachweis: https://commons.wikimedia.org/wiki/File:Chrom_SephG-50.tif
Die Elution selbst funktioniert, weil Sie die Bindungen zwischen der Säule und dem Substrat aufbrechen (z. B. durch Verwendung eines hohen Salzgehalts oder einer hohen Temperatur des Elutionsmittels). Die Elution erfolgt in der Regel in einem kleinen Puffervolumen, das mit der Probenlagerung und weiteren Anwendungen kompatibel ist.
Die Elution der DNA von der Mini-Prep-Säule ist der einfachste Fall: ein Volumen Puffer entfernt fast die gesamte DNA. Die DNA-Konzentration im Eluat ist umgekehrt proportional zum verwendeten Elutionspuffer: Je mehr Puffer verwendet wird, desto geringer ist die endgültige DNA-Konzentration. Aber selbst in diesem Fall empfehlen die meisten Hersteller, ein zusätzliches Volumen zu verwenden, um die gesamte DNA zu entfernen.
Für die Säulen ist die Elutionsgeschwindigkeit entscheidend. Eine zu langsame Geschwindigkeit erhöht das Risiko des Molekülabbaus; eine zu schnelle Geschwindigkeit führt dazu, dass keine Fraktionen aufgelöst werden.
Bei großvolumigen Säulen müssen Sie Eluatfraktionen sammeln, da Ihr Molekül auf diese verteilt wird. Die erste Fraktion enthält eine Mischung aus Wasch- und Elutionspuffer sowie mögliche Verunreinigungen, die nicht durch den Waschpuffer entfernt wurden.
Sie können die OD für Ihren Molekültyp überwachen (260nm/280nm für DNA) und einen Blot für Ihre spezifische Molekülkonzentration in jeder Fraktion durchführen. Im einfachsten Fall folgt die Verteilung der Moleküle einer einfachen Glockenkurve, sie kann aber auch einen oder mehrere scharfe Peaks aufweisen.
Zusammenfassend lässt sich sagen, dass die Kenntnis der grundlegenden Parameter Ihres Experiments (Absorptionsmittel, Größe der Säule, Waschpuffer, Elutionspuffer, Durchflussrate, Anzahl der Fraktionen) und der allgemeinen Elutionsprinzipien es Ihnen ermöglichen wird, Ihre Elution erfolgreich zu gestalten.
Für weitere Details suchen Sie einen Artikel, in dem andere Wissenschaftler etwas Ähnliches gemacht haben – idealerweise das gleiche Molekül, aber ein ähnliches genügt – und passen Sie es an Ihre Bedingungen an.
Schreibe einen Kommentar