14.8 Ether
Lernziele
- Beschreiben Sie den strukturellen Unterschied zwischen einem Alkohol und einem Ether, der die physikalischen Eigenschaften und die Reaktivität beider beeinflusst.
- Nennen Sie einfache Ether.
- Beschreibe die Struktur und die Verwendung einiger Ether.
Ein Ether mit der allgemeinen Formel ROR′ ist eine organische Verbindung, die ein Sauerstoffatom zwischen zwei Kohlenwasserstoffgruppen enthält. kann als ein Derivat von Wasser betrachtet werden, bei dem beide Wasserstoffatome durch Alkyl- oder Arylgruppen ersetzt sind. Er kann auch als Derivat eines Alkohols (ROH) betrachtet werden, bei dem das Wasserstoffatom der OH-Gruppe durch eine zweite Alkyl- oder Arylgruppe ersetzt ist:
HOH→H-Atomeersetzen beideROR′←der OH-Gruppeersetzen H-AtomROH
Einfache Ether haben einfache gebräuchliche Namen, die aus den Namen der an das Sauerstoffatom gebundenen Gruppen gebildet werden, gefolgt von der allgemeinen Bezeichnung Ether. Zum Beispiel ist CH3-O-CH2CH2CH3 Methylpropylether. Wenn beide Gruppen gleich sind, sollte dem Gruppennamen die Vorsilbe di- vorangestellt werden, wie in Dimethylether (CH3-O-CH3) und Diethylether CH3CH2-O-CH2CH3.
Ether-Moleküle haben kein Wasserstoffatom am Sauerstoffatom (d.h. keine OH-Gruppe). Daher gibt es keine intermolekulare Wasserstoffbindung zwischen Ether-Molekülen, und Ether haben daher recht niedrige Siedepunkte für eine gegebene molare Masse. Tatsächlich haben Ether etwa die gleichen Siedepunkte wie Alkane mit vergleichbarer Molmasse und viel niedrigere als die der entsprechenden Alkohole (Tabelle 14.4 „Vergleich der Siedepunkte von Alkanen, Alkoholen und Ethern“).
Tabelle 14.4 Vergleich der Siedepunkte von Alkanen, Alkoholen und Ethern
| Kondensierte Strukturformel | Name | Molare Masse | Siedepunkt (°C) | Intermolekulare Wasserstoffbrückenbindungen in reiner Flüssigkeit? |
|---|---|---|---|---|
| CH3CH2CH3 | Propan | 44 | -42 | nein |
| CH3OCH3 | Dimethylether | 46 | -25 | nein |
| CH3CH2OH | Ethylalkohol | 46 | 78 | ja |
| CH3CH2CH2CH2CH3 | Pentan | 72 | 36 | nein |
| CH3CH2OCH2CH3 | diethylether | 74 | 35 | nein |
| CH3CH2CH2CH2OH | Butylalkohol | 74 | 117 | ja |
Ether-Moleküle haben zwar ein Sauerstoffatom, und gehen mit Wassermolekülen Wasserstoffbrückenbindungen ein. Folglich hat ein Ether etwa die gleiche Löslichkeit in Wasser wie der Alkohol, der mit ihm isomerisch ist. So sind z. B. Dimethylether und Ethanol (beide mit der Summenformel C2H6O) vollständig in Wasser löslich, während Diethylether und 1-Butanol (beide C4H10O) kaum in Wasser löslich sind (8 g/100 ml Wasser).
Beispiel 5
Wie lautet die gebräuchliche Bezeichnung für jeden Ether?
- CH3CH2CH2OCH2CH2CH3
-
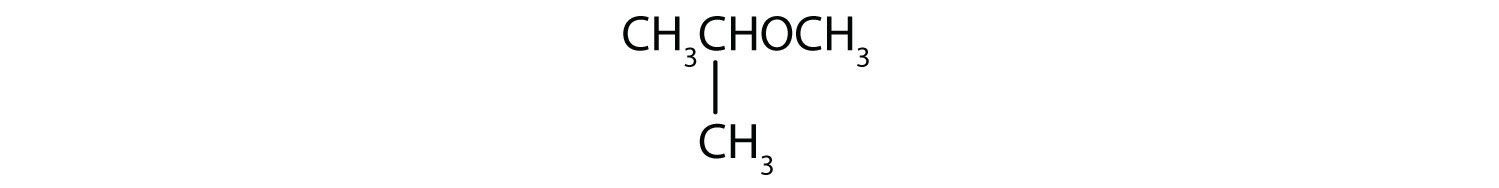
Lösung
- Die Kohlenstoffgruppen auf beiden Seiten des Sauerstoffatoms sind Propylgruppen (CH3CH2CH2), also ist die Verbindung Dipropylether.
- Die Dreikohlenstoffgruppe ist über das mittlere Kohlenstoffatom gebunden, es handelt sich also um eine Isopropylgruppe. Die Ein-Kohlenstoff-Gruppe ist eine Methylgruppe. Die Verbindung ist Isopropylmethylether.
Skill-Building Exercise
-
CH3CH2CH2CH2OCH2CH2CH2CH3
-
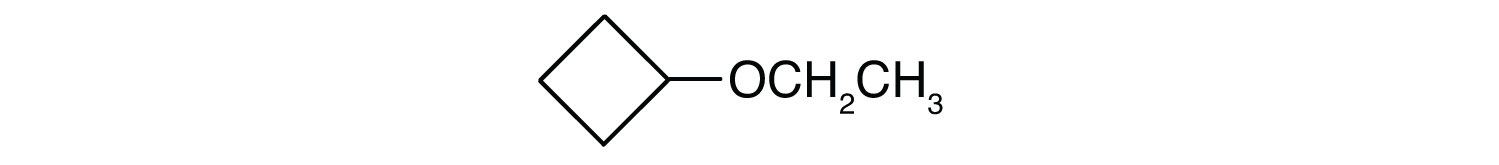
Wie lautet der gebräuchliche Name für jeden Ether?
Zu Ihrer Gesundheit: Ether als allgemeine Anästhetika
Ein allgemeines Anästhetikum wirkt auf das Gehirn, um Bewusstlosigkeit und eine allgemeine Gefühls- und Schmerzunempfindlichkeit zu erzeugen. Diethylether (CH3CH2OCH2CH3) war das erste Allgemeinanästhetikum, das verwendet wurde.
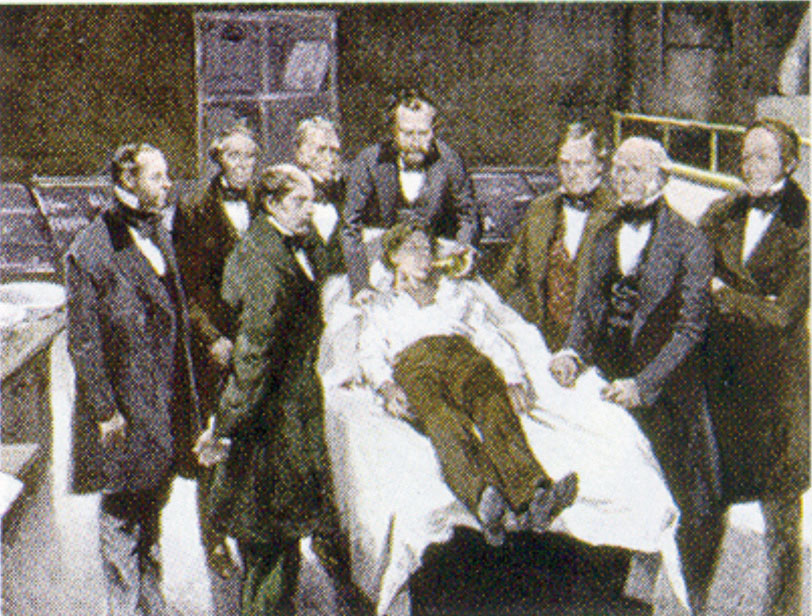
William Morton, ein Bostoner Zahnarzt, führte Diethylether 1846 in die chirurgische Praxis ein. Dieses Bild zeigt eine Operation in Boston im Jahr 1846, bei der Diethylether als Anästhetikum verwendet wurde. Das Einatmen von Ätherdampf führt zur Bewusstlosigkeit, indem die Aktivität des zentralen Nervensystems unterdrückt wird.
Quelle: Gemälde von William Morton von Ernest Board, aus http://commons.wikimedia.org/wiki/File:Morton_Ether_1846.jpg.
Diethylether ist relativ sicher, da zwischen der Dosis, die eine wirksame Betäubung bewirkt, und der tödlichen Dosis ein ziemlich großer Abstand besteht. Da es jedoch leicht entflammbar ist und den zusätzlichen Nachteil hat, dass es Übelkeit verursacht, wurde es durch neuere Inhalationsanästhetika ersetzt, darunter die fluorhaltigen Verbindungen Halothan, Enfluran und Isofluran. Leider wurde die Sicherheit dieser Verbindungen für das Personal im Operationssaal in Frage gestellt. So sind beispielsweise Frauen, die im Operationssaal mit Halothan in Berührung kommen, häufiger von Fehlgeburten betroffen als Frauen in der Allgemeinbevölkerung.
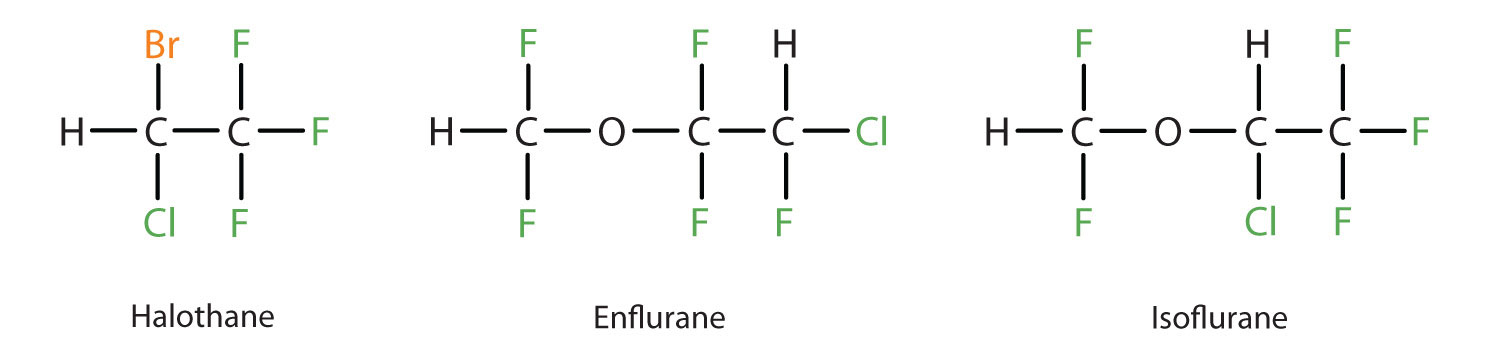
Diese drei modernen, inhalativen, halogenhaltigen Anästhetika sind weniger brennbar als Diethylether.
Konzeptüberprüfungsübungen
-
Warum hat Diethylether (CH3CH2OCH2CH3) einen viel niedrigeren Siedepunkt als 1-Butanol (CH3CH2CH2CH2OH)?
-
Welcher Stoff ist besser in Wasser löslich – Methylethyläther (CH3CH2OCH3) oder 1-Butanol (CH3CH2CH2CH2OH)? Erkläre.
Antworten
-
Diethylether hat keine intermolekulare Wasserstoffbindung, weil es keine OH-Gruppe gibt; 1-Butanol hat eine OH-Gruppe und geht eine intermolekulare Wasserstoffbindung ein.
-
Ethylmethylether (drei Kohlenstoffatome, ein Sauerstoffatom) ist besser in Wasser löslich als 1-Butanol (vier Kohlenstoffatome, ein Sauerstoffatom), obwohl beide mit Wasser Wasserstoffbrückenbindungen eingehen können.
Key Takeaways
- Um Ether zu benennen, benennt man einfach die Gruppen, die an das Sauerstoffatom gebunden sind, gefolgt von der allgemeinen Bezeichnung Ether. Wenn beide Gruppen gleich sind, sollte dem Gruppennamen die Vorsilbe di- vorangestellt werden.
- Ether-Moleküle haben keine OH-Gruppe und somit keine intermolekulare Wasserstoffbindung. Ether haben daher recht niedrige Siedepunkte für eine gegebene molare Masse.
- Ether-Moleküle haben ein Sauerstoffatom und können mit Wassermolekülen Wasserstoffbrückenbindungen eingehen. Ein Ethermolekül hat etwa die gleiche Löslichkeit in Wasser wie der zu ihm isomere Alkohol.
Übungen
-
Wie kann Ethanol beim Erhitzen mit Schwefelsäure zwei verschiedene Produkte ergeben? Nennen Sie diese Produkte.
-
Welcher dieser Ether ist isomer mit Ethanol – CH3CH2OCH2CH3, CH3OCH2CH3 oder CH3OCH3?
-
Nenne jede Verbindung.
- CH3OCH2CH2CH3
-
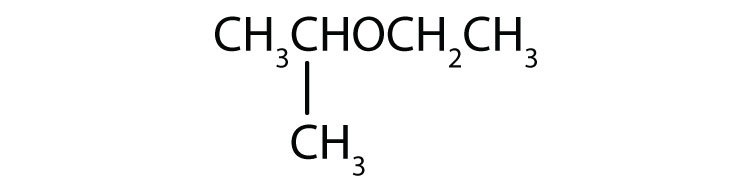
-
Nenne jede Verbindung.
- CH3CH2CH2CH2OCH3
- CH3CH2OCH2CH2CH3
-
Zeichne die Struktur für jede Verbindung.
- Methylethylether
- tert-Butylethylether
-
Zeichne die Struktur für jede Verbindung.
- Diisopropylether
- Cyclopropylpropylether
Antworten
-
Intramolekulare (sowohl das H als auch das OH stammen aus demselben Molekül) Dehydratisierung ergibt Ethylen; intermolekulare Dehydratisierung (das H stammt von einem Molekül und das OH von einem anderen Molekül) ergibt Diethylether.
-
- Methylpropylether
- Ethylisopropylether
-
- CH3OCH2CH3
-
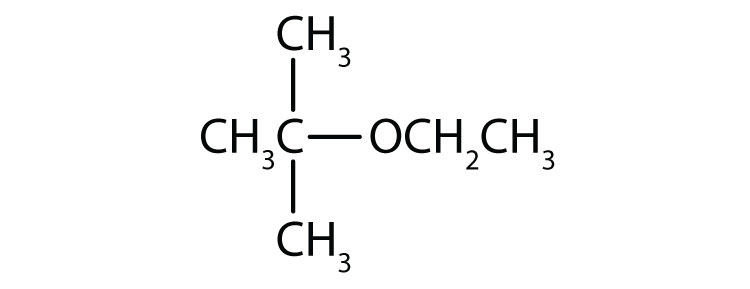
Schreibe einen Kommentar