- Was ist Eisen
- Wo ist Eisen zu finden
- Geschichte
- Identifikation
- Klassifikation, Eigenschaften und Merkmale von Eisen
- Allgemeine Eigenschaften
- Physikalische Eigenschaften
- Chemische Eigenschaften
- Atomdaten von Eisen (Element 26)
- Was sind die allgemeinen Verwendungszwecke von Eisen
- Hat das Element toxische Wirkungen
- Interessante Fakten
- Eisenmetallpreis
Was ist Eisen
Eisen (sprich: EYE-ren) ist ein Hartmetall mit einem hohen Handelswert, das zur Familie der Übergangsmetalle gehört. Es wird durch das chemische Symbol Fe dargestellt und ist chemisch reaktionsfreudig. Es neigt dazu, an der Luft leicht zu korrodieren und bildet eine rötliche Schicht, die Rost genannt wird, wenn es feuchter Luft ausgesetzt ist.

Eisensymbol
Wo ist Eisen zu finden
Es ist das vierthäufigste Metall in der Erdkruste und wird häufig mit anderen Mineralerzen wie Hämatit, Takonit und Magnetit in den Bergbaureserven der Ukraine, Brasiliens, Russlands, Australiens und Chinas gefunden. Seine kommerzielle Herstellung erfolgt in einem Hochofen durch Erhitzen der Erze mit Koks und Kalkstein.
Geschichte
Herkunft des Namens: Der Name des Elements stammt von dem angelsächsischen Wort „Eisen“.
Wer entdeckte es: Unbekannt
Wann, wo und wie wurde es entdeckt
Um 3500 v. Chr. sollen die Ägypter Gegenstände aus Eisen verwendet haben. Die kleinasiatischen Hethiter verhütteten das Metall bereits 1500 v. Chr. aus seinen Erzen. Im Jahr 1722 veröffentlichte René Antoine Ferchault de Réaumur, ein französischer Entomologe, ein Buch, in dem er die Bedeutung der verschiedenen Eisenlegierungen beschrieb.

Eisenmetall
Identifikation |
|||
| Atomzahl | 26 | ||
| CAS-Nummer | 7439-89-6 | ||
| Stellung im Periodensystem | Gruppe | Periode | Block |
| 8 | 4 | d | |
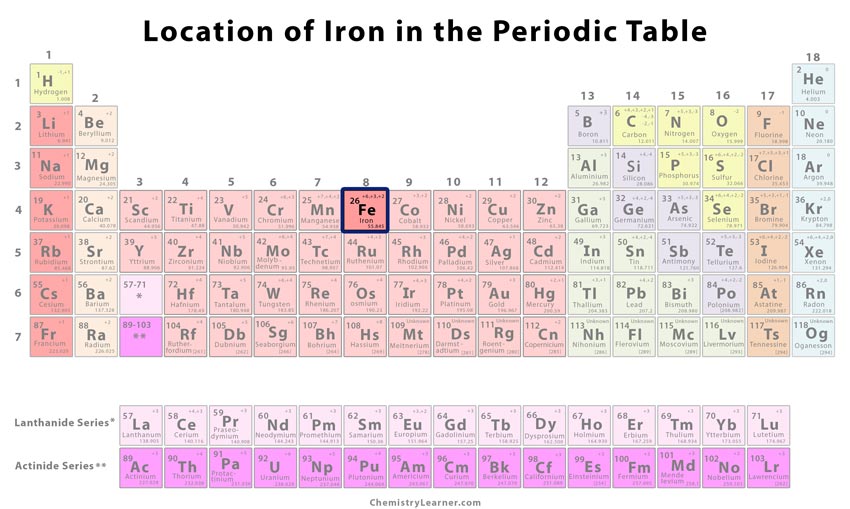
Wo liegt Eisen im Periodensystem
Klassifikation, Eigenschaften und Merkmale von Eisen
Allgemeine Eigenschaften |
||
| Relative Atommasse | 55.845 | |
| Atommasse/Gewicht | 55.845 Atommasseneinheiten | |
| Molare Masse/Molekulargewicht | 55.845 g/Mol | |
| Massenzahl | 56 | |
Physikalische Eigenschaften |
||
| Farbe/physikalisches Aussehen | Silbergrau | |
| Schmelzpunkt/Gefrierpunkt | 1538°C (2800°F) | |
| Siedepunkt | 2861°C (5182°F) | |
| Dichte | 7.87 g/cm3 | |
| Normalzustand/Naturzustand bei Raumtemperatur (fest/flüssig/gasförmig) | Fest | |
| Mischbarkeit | Ja | |
| Duktilität | Ja | |
| Härte | 4-5 Mohs | |
| Spezifische Wärmekapazität | 0.444 J g-1 oC | |
| Wärmeleitfähigkeit | 80.4 Wm-1K-1 | |
Chemische Eigenschaften |
||
| Entflammbarkeit | Nicht entflammbar | |
| Oxidationsstufen (Zahlen) | 6, 3, 2, 0,-2 | |
Atomdaten von Eisen (Element 26)
| Elektronenkonfiguration (Edelgaskonfiguration) | 3d64s2 | ||||||
| Atomstruktur | |||||||
| – Anzahl der Elektronen | 26 | ||||||
| – Anzahl der Neutronen | 30 | ||||||
| – Anzahl der Protonen | 26 | ||||||
| Atomradius | |||||||
| – Atomradius | 2.04 Å | ||||||
| – Kovalenter Radius | 1.24 Å | ||||||
| Ionisierungsenergie
(kJmol-1) |
1. | 2. | 3. | 4. | 5. | 6. | 7. |
| 762.466 | 1561.876 | 2957.469 | 5287.4 | 7236 | 9561.7 | 12058.74 | |
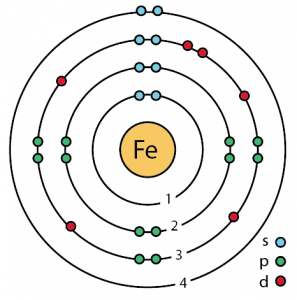
Atomstruktur von Eisen (Bohr-Modell)
Was sind die allgemeinen Verwendungszwecke von Eisen
- Eisen wird bei der Herstellung von verschiedenen Stahlsorten durch Legierung mit anderen Elementen wie Kohlenstoff, Nickel, Chrom und Wolfram zur Herstellung von Schneidegeräten, Fahrradketten, Gewehrläufen, Übertragungsmasten, Brückenträgern und Stahlbeton.
- Edelstahl mit einem hohen Anteil an Eisen und anderen Metallen hat eine enorme Festigkeit und eine bessere Funktion, die bei der Herstellung von chirurgischen Instrumenten, Büroklammern, Besteck, Kugellagern und Schmuck nützlich ist.
- Eine andere Form von Eisen, Schmiedeeisen genannt, das durch Schmelzen gewonnen wird, wird zur Herstellung von Tischlerwerkzeugen, Hebehaken, Ketten, Zäunen und Toren verwendet.
- Eisenfüllungen werden in Experimenten der Elektromagnetismuswissenschaft verwendet, um die Stärke von Magneten zu bestimmen, sowie in der Energiemetallurgie, in Kunstwerken, in Feuerwerkskörpern und beim Sandstrahlen.
- Fe wirkt als effizienter Katalysator in einigen industriellen chemischen Prozessen wie dem Haber-Prozess und Fischer-Tropsch.

Eisenbarren
Hat das Element toxische Wirkungen
Die versehentliche Einnahme von Fe wurde mit Erbrechen, Durchfall und anderen gastrointestinalen Problemen in Verbindung gebracht, einer häufigen Art von Metallvergiftung. Eine längere Anreicherung im Körper kann zu Atemwegs- und Herzproblemen führen. Das Einatmen von Metallstaub oder -dämpfen kann zu schweren Lungenreaktionen führen.
Interessante Fakten
- Meteoriten haben vermutlich einen hohen Eisengehalt.
- Eisen wurde von den alten Seefahrern als magnetisches Metall in Form von lodestones für die Herstellung von Kompassen verwendet.
- In einem durchschnittlichen menschlichen Körper sind 4 Gramm Fe vorhanden, das mit Hämoglobin verbunden ist, das wiederum hilft, Sauerstoff in die Lungen zu transportieren.
-

Eisenpulver
Eisenmetallpreis
Die Kosten für reines Eisen können zwischen $0,24 und $0,30 pro Pfund schwanken.
- http://www.rsc.org/periodic-table/element/26/iron
- https://education.jlab.org/itselemental/ele026.html
- https://www.chemicool.com/elements/iron.html
- https://www.radiochemistry.org/periodictable/elements/26.html
- https://www.thoughtco.com/iron-facts-606548
- https://www.tedpella.com/company_html/hardness.htm
- https://www.tedpella.com/company_html/hardness.htm
- http://www2.ucdsb.on.ca/tiss/stretton/database/specific_heat_capacity_table.html
- https://www.angelo.edu/faculty/kboudrea/demos/burning_iron/burning_iron.htm
- https://extrudesign.com/wrought-iron-properties-applications/
- http://www.iron-filing.com/
- https://www.clinicaladvisor.com/labmed/toxicity-associated-with-iron/article/614895/
- https://www.ncbi.nlm.nih.gov/pubmed/1592301
Schreibe einen Kommentar