Bindung in Acetylen
Schließlich lässt sich das Konzept der Hybridorbitale auch auf dreifach gebundene Gruppen wie Alkine und Nitrile anwenden. Betrachten wir zum Beispiel die Struktur von Ethin (allgemeiner Name Acetylen), dem einfachsten Alkin.
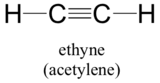
Dieses Molekül ist linear: alle vier Atome liegen in einer geraden Linie. Die Kohlenstoff-Kohlenstoff-Dreifachbindung ist nur 1,20 Å lang. Im Hybridorbitalbild von Acetylen sind beide Kohlenstoffe sp-hybridisiert. In einem sp-hybridisierten Kohlenstoff verbindet sich das 2s-Orbital mit dem 2px-Orbital zu zwei sp-Hybridorbitalen, die in einem Winkel von 180° zueinander ausgerichtet sind (z. B. entlang der x-Achse). Die 2py- und 2pz-Orbitale bleiben unhybridisiert und sind senkrecht entlang der y- bzw. z-Achse ausgerichtet.


Die C-C-Sigma-Bindung wird also durch die Überlappung eines sp-Orbitals von jedem der Kohlenstoffatome gebildet, während die beiden C-H-Sigma-Bindungen durch die Überlappung des zweiten sp-Orbitals an jedem Kohlenstoff mit einem 1s-Orbital an einem Wasserstoffatom gebildet werden. Jedes Kohlenstoffatom hat noch zwei halbgefüllte 2py- und 2pz-Orbitale, die sowohl zueinander als auch zu der durch die Sigma-Bindungen gebildeten Linie senkrecht stehen. Diese beiden senkrecht zueinander stehenden Paare von p-Orbitalen bilden zwei pi-Bindungen zwischen den Kohlenstoffen, was insgesamt zu einer Dreifachbindung führt (eine Sigma-Bindung plus zwei pi-Bindungen).

Das Konzept der Hybridorbitale erklärt sehr gut eine andere experimentelle Beobachtung: Einfachbindungen, die an Doppel- und Dreifachbindungen angrenzen, sind zunehmend kürzer und stärker als „normale“ Einfachbindungen, wie die in einem einfachen Alkan. Die Kohlenstoff-Kohlenstoff-Bindung in Ethan (Struktur A unten) entsteht durch die Überlappung zweier sp3-Orbitale.

Im Alken B ist die Kohlenstoff-Kohlenstoff-Einfachbindung jedoch das Ergebnis der Überlappung eines sp2-Orbitals und eines sp3-Orbitals, während im Alkin C die Kohlenstoff-Kohlenstoff-Einfachbindung das Ergebnis der Überlappung eines sp-Orbitals und eines sp3-Orbitals ist. Dies sind alles Einfachbindungen, aber die Bindung in Molekül C ist kürzer und stärker als die in B, die wiederum kürzer und stärker ist als die in A.
Die Erklärung dafür ist relativ einfach. Ein sp-Orbital setzt sich aus einem s-Orbital und einem p-Orbital zusammen und hat somit 50 % s-Charakter und 50 % p-Charakter. sp2-Orbitale haben im Vergleich dazu 33 % s-Charakter und 67 % p-Charakter, während sp3-Orbitale 25 % s-Charakter und 75 % p-Charakter haben. Aufgrund ihrer kugelförmigen Form sind 2s-Orbitale kleiner und halten die Elektronen im Vergleich zu 2p-Orbitalen näher und „dichter“ am Kern. Folglich sind Bindungen mit sp + sp3-Überlappung (wie in Alken C) kürzer und stärker als Bindungen mit sp2 + sp3-Überlappung (wie in Alken B). Bindungen mit sp3-sp3-Überlappung (wie in Alkan A) sind die längsten und schwächsten der Gruppe, da die Hybride zu 75 % p-Charakter haben.
Schreibe einen Kommentar