- What is Iron
- W Where is Iron Found
- Geschiedenis
- Identificatie
- Classificatie, Eigenschappen en kenmerken van ijzer
- Algemene eigenschappen
- Fysische Eigenschappen
- Chemische eigenschappen
- Atomische gegevens van ijzer (element 26)
- Wat zijn de Gemeenschappelijke Toepassingen van IJzer
- Heeft het element toxische effecten
- Belangrijke feiten
- Iron Metal Price
What is Iron
Iron (uitgesproken als EYE-ren) is een hard metaal met een hoge handelswaarde, behorend tot de familie van overgangsmetalen. Vertegenwoordigd door het chemische symbool Fe, is het chemisch reactief met een tendens om gemakkelijk te corroderen in lucht die een roodachtige laag genoemd roest wanneer blootgesteld aan vochtige lucht vormt.

Iron Symbol
W Where is Iron Found
Het is het op drie na meest voorkomende metaal in de aardkorst, gewoonlijk geassocieerd met andere minerale ertsen zoals hematiet, taconiet en magnetiet, die voorkomen in mijnreserves van Oekraïne, Brazilië, Rusland, Australië en China. De commerciële productie ervan vindt plaats in een hoogoven door de ertsen te verhitten met cokes en kalksteen.
Geschiedenis
Oorsprong van de naam: De naam van het element komt van een Angelsaksisch woord ‘ijzer’.
Wie heeft het ontdekt: Onbekend
Wanneer, waar en hoe werd het ontdekt
Omstreeks 3500 v. Chr. werd aangenomen dat de Egyptenaren ijzeren voorwerpen gebruikten. Van de Hettieten uit Klein-Azië was bekend dat zij het metaal in 1500 v. Chr. uit ertsen smolten. In 1722 publiceerde René Antoine Ferchault de Réaumur, een Franse entomoloog, een boek waarin hij de betekenis van verschillende ijzerlegeringen beschreef.

Iron Metaal
Identificatie |
|||
| Atoomnummer | 26 | ||
| CAS nummer | 7439-89-6 | ||
| Positie in het periodiek systeem | Groep | Periode | Blok |
| 8 | 4 | d | |
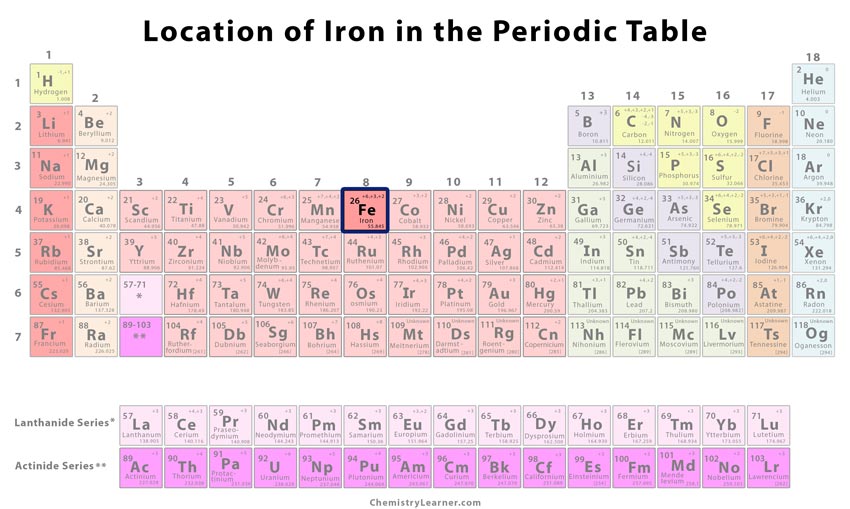
Waar staat ijzer in het Periodiek Systeem
Classificatie, Eigenschappen en kenmerken van ijzer
Algemene eigenschappen |
||
| Relatieve atoommassa | 55.845 | |
| Atomaire massa/gewicht | 55.845 atomaire massaeenheden | |
| Molaire massa/Moleculair gewicht | 55.845 g/mole | |
| Massa Aantal | 56 | |
Fysische Eigenschappen |
||
| Kleur/fysische verschijning | Zilvergrijs | |
| Smeltpunt/vriespunt | 1538°C (2800°F) | |
| kookpunt | 2861°C (5182°F) | |
| Dichtheid | 7.87 g/cm3 | |
| Standaard/Natuurlijke toestand bij kamertemperatuur (vast/vloeibaar/gas) | Vast | |
| Smeedbaarheid | Ja | |
| Verminderbaarheid | Ja | |
| Hardheid | 4-5 Mohs | |
| Specifieke warmtecapaciteit | 0.444 J g-1 oC | |
| Thermische geleidbaarheid | 80.4 Wm-1K-1 | |
Chemische eigenschappen |
||
| Brandbaarheid | Niet brandbaar | |
| Oxidatietoestanden (getallen) | 6, 3, 2, 0,-2 | |
Atomische gegevens van ijzer (element 26)
| Elektronenconfiguratie (edelgasconfiguratie) | 3d64s2 | ||||||
| Atoomstructuur | |||||||
| – Aantal elektronen | 26 | ||||||
| – Aantal neutronen | 30 | ||||||
| – Aantal Protonen | 26 | ||||||
| Radius van atoom | |||||||
| – Atoomstraal | 2.04 Å | ||||||
| – Covalente Straal | 1.24 Å | ||||||
| Ionisatie-energie
(kJmol-1) |
1e | 2e | 3e | 4e | 5e | 6e | 7e |
| 762.466 | 1561.876 | 2957.469 | 5287.4 | 7236 | 9561.7 | 12058.74 | |
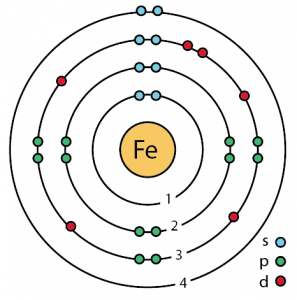
Iron Atomic Structure (Bohr Model)
Wat zijn de Gemeenschappelijke Toepassingen van IJzer
- Iron wordt gebruikt bij de vervaardiging van verschillende soorten staal door legering met andere elementen zoals koolstof, nikkel, chroom en wolfraam voor het maken van snijgereedschap, fietskettingen, geweerlopen, transmissietorens, brugliggers, en gewapend beton.
- Roestvast staal dat een hoog percentage ijzer bevat samen met andere metalen heeft een enorme sterkte en een betere functie die nuttig is bij het maken van chirurgische instrumenten, paperclips, bestek, kogellagers, en sieraden.
- Een andere vorm van Fe genoemd smeedijzer verkregen door smelten wordt gebruikt om timmermansgereedschap, hijshaken, kettingen, hekwerk, en poorten te maken.
- ijzervullingen zijn van toepassing in elektromagnetisme wetenschapsexperimenten om de sterkte van magneten te beoordelen, alsmede in energiemetallurgie, kunstwerken, vuurwerk, en zandstralen.
- Fe fungeert als een efficiënte katalysator is een aantal industriële chemische processen zoals Haber proces en Fischer-Tropsch .

Iron Bar
Heeft het element toxische effecten
Een toevallige inname van Fe is in verband gebracht met braken, diarree en andere gastro-intestinale problemen, een veel voorkomende vorm van metaalvergiftiging. Langdurige accumulatie in het lichaam kan resulteren in ademhalingsproblemen en hartstoornissen. Het inademen van metaalstof of dampen kan een ernstige longreactie veroorzaken.
Belangrijke feiten
- Meteorieten zouden een hoog ijzergehalte hebben.
- Iron werd gebruikt als een magnetisch metaal door oude navigators in de vorm van lodestones voor het maken van kompassen.
- In een gemiddeld menselijk lichaam is 4 gram Fe aanwezig, geassocieerd met hemoglobine dat op zijn beurt helpt bij het transporteren van zuurstof naar de longen.
-

Iron Powder
Iron Metal Price
De kosten van zuiver ijzer kunnen variëren tussen $ 0,24 en $ 0,30 per pond.
- http://www.rsc.org/periodic-table/element/26/iron
- https://education.jlab.org/itselemental/ele026.html
- https://www.chemicool.com/elements/iron.html
- https://www.radiochemistry.org/periodictable/elements/26.html
- https://www.thoughtco.com/iron-facts-606548
- https://www.tedpella.com/company_html/hardness.htm
- https://www.tedpella.com/company_html/hardness.htm
- http://www2.ucdsb.on.ca/tiss/stretton/database/specific_heat_capacity_table.html
- https://www.angelo.edu/faculty/kboudrea/demos/burning_iron/burning_iron.htm
- https://extrudesign.com/wrought-iron-properties-applications/
- http://www.iron-filing.com/
- https://www.clinicaladvisor.com/labmed/toxicity-associated-with-iron/article/614895/
- https://www.ncbi.nlm.nih.gov/pubmed/1592301
Geef een antwoord