14.8 Eteri
Obiective de învățare
- Descrieți diferența structurală dintre un alcool și un eter care afectează caracteristicile fizice și reactivitatea fiecăruia.
- Numiți eteri simpli.
- Descrieți structura și utilizările unor eteri.
Cu formula generală ROR′, un eterCompus organic care are un atom de oxigen între două grupe hidrocarbonate. poate fi considerat un derivat al apei în care ambii atomi de hidrogen sunt înlocuiți cu grupe alchil sau aril. Poate fi considerat, de asemenea, un derivat al unui alcool (ROH) în care atomul de hidrogen al grupei OH este înlocuit cu o a doua grupă alchil sau aril:
HOH→Atomii de Hînlocuiți ambiiROR′←din grupa OHînlocuiți atomul de HROH
Eterii simpli au denumiri comune simple, formate din denumirile grupărilor atașate la atomul de oxigen, urmate de denumirea generică de eter. De exemplu, CH3-O-CH2-CH2CH2CH3 este metil propil eter. În cazul în care ambele grupe sunt identice, numele grupei trebuie precedat de prefixul di-, ca în eterul dimetilic (CH3-O-CH3) și eterul dietilic CH3CH2-O-CH2CH3.
Molculele de eter nu au nici un atom de hidrogen pe atomul de oxigen (adică nu au grupa OH). Prin urmare, nu există legături de hidrogen intermoleculare între moleculele de eter și, prin urmare, eterii au puncte de fierbere destul de scăzute pentru o masă molară dată. Într-adevăr, eterii au puncte de fierbere aproximativ identice cu cele ale alcanilor de masă molară comparabilă și mult mai mici decât cele ale alcoolilor corespunzători (tabelul 14.4 „Compararea punctelor de fierbere ale alcanilor, alcoolilor și eteriilor”).
Tabel 14.4 „Compararea punctelor de fierbere ale alcanilor, alcoolilor și esterilor”).4 Compararea punctelor de fierbere ale alcanilor, alcoolilor și eteriilor
| Formula structurală condensată | Numele | Masa molară | Punctul de fierbere (°C) | Legătura intermoleculară a hidrogenului în lichidul pur? | |
|---|---|---|---|---|---|
| CH3CH2CH3 | propan | 44 | -42 | nu | |
| CH3OCH3 | eter dimetilic | 46 | -25 | nu | |
| CH3CH2OH | alcool etilic | 46 | 78 | da | |
| CH3CH2CH2CH2CH2CH3 | pentan | 72 | 36 | nu | |
| CH3CHCH2OCH2CH3 | eter dietilic | 74 | 35 | nu | nu |
| CH3CH2CH2CH2CH2OH | alcool butilic | 74 | 117 | da |
Molculele de eter au un atom de oxigen, totuși, și se angajează în legături de hidrogen cu moleculele de apă. În consecință, un eter are aproximativ aceeași solubilitate în apă ca și alcoolul care este izomer cu el. De exemplu, eterul dimetilic și etanolul (ambele având formula moleculară C2H6O) sunt complet solubile în apă, în timp ce eterul dietilic și 1-butanolul (ambele C4H10O) sunt abia solubile în apă (8 g/100 ml de apă).
Exemplu 5
Care este denumirea comună a fiecărui eter?
- CH3CH2CH2OCH2CH2CH2CH3
-
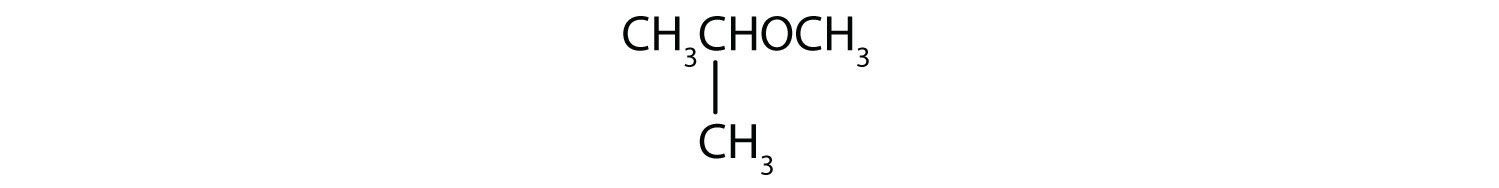
Soluție
- Grupele de carbon de o parte și de alta a atomului de oxigen sunt grupe propil (CH3CH2CH2CH2), deci compusul este eter dipropilic.
- Grupul cu trei atomi de carbon este atașat de atomul de carbon din mijloc, deci este un grup izopropil. Grupa cu un singur atom de carbon este o grupare metil. Compusul este izopropil metil eter.
Exercițiu de dezvoltare a abilităților
-
CH3CH2CH2CH2CH2OCH2CH2CH2CH2CH3
-
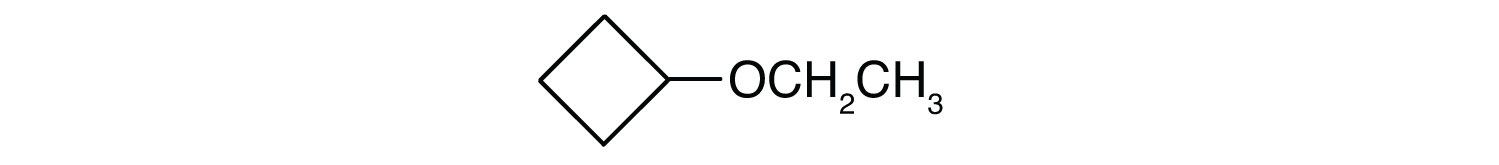
Care este numele comun al fiecărui eter?
În sănătatea ta: Eterii ca anestezice generale
Un anestezic general acționează asupra creierului pentru a produce inconștiență și o insensibilitate generală la senzații sau durere. Eterul dietilic (CH3CH2OCH2CH3) a fost primul anestezic general care a fost folosit.
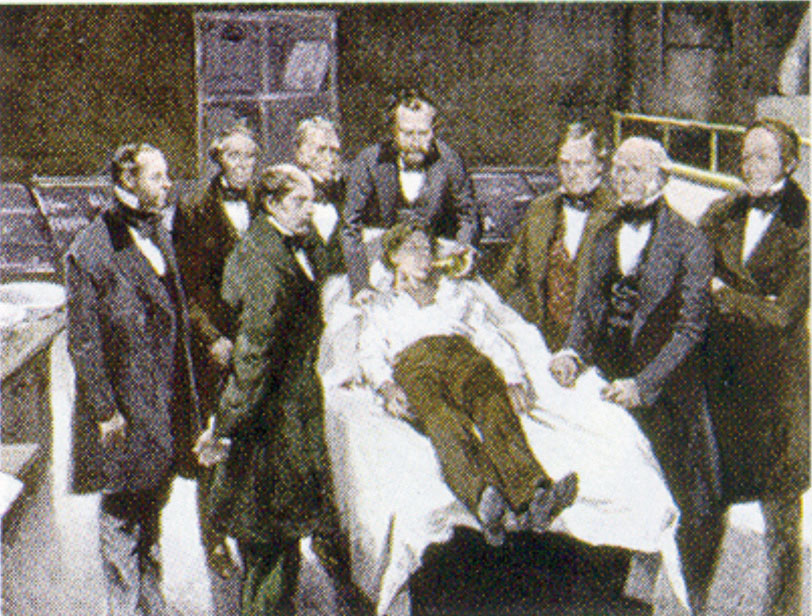
William Morton, un dentist din Boston, a introdus eterul dietilic în practica chirurgicală în 1846. Această pictură arată o operație din Boston în 1846 în care s-a folosit dietil eterul ca anestezic. Inhalarea vaporilor de eter produce inconștiență prin deprimarea activității sistemului nervos central.
Sursa: Pictură a lui William Morton de Ernest Board, din http://commons.wikimedia.org/wiki/File:Morton_Ether_1846.jpg.
Eterul etilic este relativ sigur, deoarece există o diferență destul de mare între doza care produce un nivel eficient de anestezie și doza letală. Cu toate acestea, deoarece este foarte inflamabil și are dezavantajul suplimentar de a provoca greață, a fost înlocuit de anestezice inhalante mai noi, inclusiv compușii cu conținut de fluor halotan, enfluran și izofluran. Din păcate, siguranța acestor compuși pentru personalul din sala de operație a fost pusă sub semnul întrebării. De exemplu, femeile care lucrează în sălile de operație expuse la halotan suferă o rată mai mare de avorturi spontane decât femeile din populația generală.
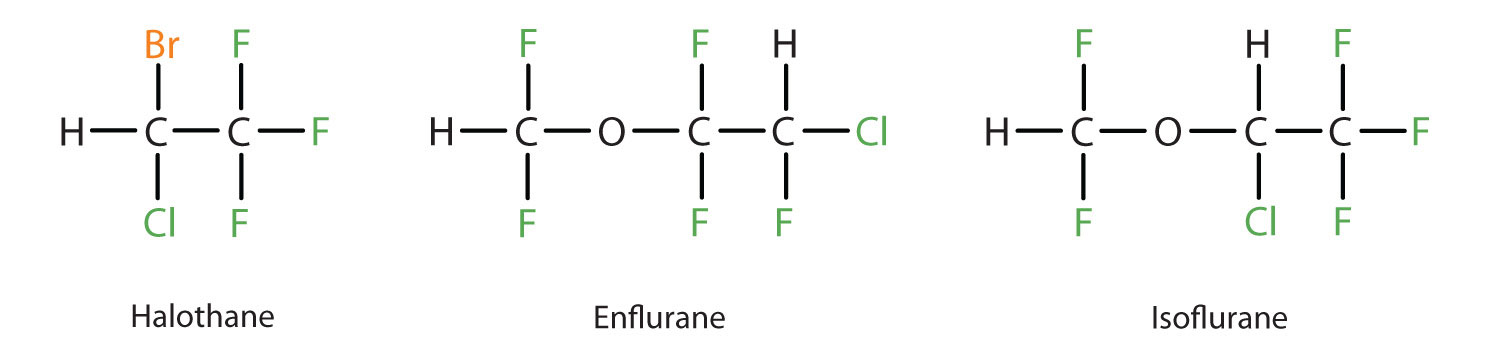
Cei trei compuși anestezici moderni, inhalanți, care conțin halogen, sunt mai puțin inflamabili decât eterul dietilic.
Exerciții de recapitulare a noțiunilor
-
De ce eterul dietilic (CH3CH2OCH2CH3) are un punct de fierbere mult mai mic decât 1-butanolul (CH3CH2CH2CH2OH)?
-
Ce este mai solubil în apă – eterul etilic de metil (CH3CH2OCH3) sau 1-butanolul (CH3CH2CH2CH2CH2OH)? Explicați.
Răspunsuri
-
Eterul etilic nu are legături de hidrogen intermoleculare, deoarece nu există o grupare OH; 1-butanolul are o grupare OH și se angajează în legături de hidrogen intermoleculare.
-
Eterul metilic etilic (trei atomi de carbon, un atom de oxigen) este mai solubil în apă decât 1-butanolul (patru atomi de carbon, un atom de oxigen), chiar dacă amândoi se pot angaja în legături de hidrogen cu apa.
Key Takeaways
- Pentru a da eteri nume comune, pur și simplu se numesc grupele atașate la atomul de oxigen, urmate de numele generic de eter. Dacă ambele grupe sunt identice, numele grupei trebuie să fie precedat de prefixul di-.
- Moleculele de eter nu au grupa OH și, prin urmare, nu au legături de hidrogen intermoleculare. Prin urmare, eterii au puncte de fierbere destul de scăzute pentru o masă molară dată.
- Molculele de eter au un atom de oxigen și se pot angaja în legături de hidrogen cu moleculele de apă. O moleculă de eter are aproximativ aceeași solubilitate în apă ca și alcoolul care este izomer cu ea.
Exerciții
-
Cum poate da etanolul doi produși diferiți atunci când este încălzit cu acid sulfuric? Numiți acești produși.
-
Care dintre acești eteri este izomer cu etanolul-CH3CH2OCH2CH3, CH3OCH2CH3 sau CH3OCH3?
-
Numiți fiecare compus.
- CH3OCH2CH2CH3
-
-
Numiți fiecare compus.
- CH3CH2CH2CH2CH2OCH3
- CH3CH2OCH2CH2CH2CH3
-
Desenați structura pentru fiecare compus.
- eter metilic etilic
- eter terț-butil etilic
-
Desenați structura pentru fiecare compus.
- diisopropil eter
- ciclopropil propil eter
Răspunsuri
-
Dishidratarea intramoleculară (atât H cât și OH provin din aceeași moleculă) dă etilenă; deshidratarea intermoleculară (H provine dintr-o moleculă, iar OH provine dintr-o altă moleculă) dă eter dietilic.
-
- eter metilpropilic
- eter izopropilic
.
-
- CH3OCH2CH3
-
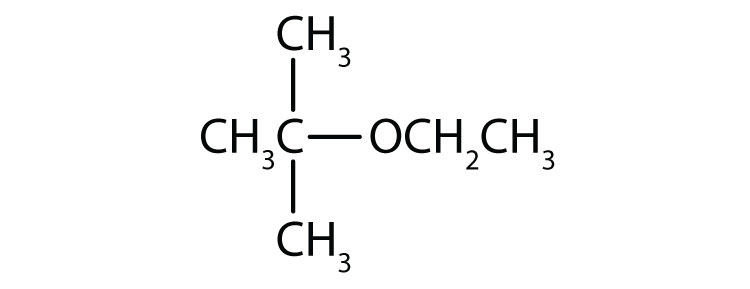
.
Lasă un răspuns