DOCUMENTE ORIGINALE
Detecția antigenului de suprafață al hepatitei B utilizând seruri combinate. O analiză cost-beneficiu
E. Fernández, L. Rodrigo1, S. García, S. Riestra1 și C. Blanco
Serviciul de Biochimie. Hospital de Cabueñes. Gijón. 1Serviciul de Gastroenterologie. Hospital Central de Asturias. Oviedo. Spania
Correspondență
ABSTRACT
Obiective: Examinarea fezabilității și efectuarea unei analize cost-beneficiu a unei strategii de grupare a 5 eșantioane folosind un imunoenzimatic (EIA) pentru depistarea antigenului de suprafață al hepatitei B (HBsAg).
Materiale și metode: pentru a evalua sensibilitatea și specificitatea metodei de grupare, fiecare dintre cele 40 de seruri pozitive (de la slab la intens pozitiv HBsAg) și 250 de seruri negative au fost testate într-un grup cu 4 seruri HBsAg-negative. Limita de detecție pentru HBsAg/ad și HBsAg/ay a fost evaluată folosind seruri dintr-un panel de subtipuri purificate. A fost efectuat un studiu în condiții reale folosind pool-uri de la 340 de femei însărcinate.
Rezultate: Sensibilitatea și specificitatea acestei tehnici au fost de 100%. Coeficientul de corelație între raporturile eșantion/cuvinte din 40 de probe studiate în condiții individuale și în condiții de pool a fost de 0,792 (p < 0,005). Metoda pooling are niveluri de detecție mai scăzute pentru HBsAg/ad și HBsAg/ay, la 0,20 ng/mL și 0,12 ng/mL, iar metoda unică la 0,34 ng/mL și, respectiv, 0,29 ng/mL. Metoda de punere în comun nu își pierde sensibilitatea pentru valori de până la 100 UI/L de anti-HBs în cele patru seruri amestecate cu un ser pozitiv. Analiza cost-beneficiu a arătat că metoda pooling ar putea economisi de la 30% până la 75% din costul determinării HBsAg, în funcție de faptul că seroprevalențele sunt de 10%, respectiv 1%.
Concluzii: EIA HBsAg grupat nu a dat rezultate mai proaste decât testul EIA unic și a fost o strategie rentabilă și valabilă în zonele cu o prevalență ridicată, medie sau scăzută.
Locuri cheie:
: Antigen de suprafață al hepatitei B. Reunirea serurilor. Analiza cost-beneficiu.
Rodrigo L, Fernández E, García S, Riestra S, Blanco C. Hepatitis B surface antigen detection using pooled sera. O analiză cost-beneficiu. Rev Esp Enferm Dig 2006; 98: 112-121.
Introducere
Infecția cu virusul hepatitei B (VHB) este o boală care afectează milioane de oameni din întreaga lume. Principalul său rezervor este cel al purtătorilor cronici de VHB. Se estimează că aproximativ 300 de milioane de persoane din întreaga lume sunt infectate cu acest virus (1). Consecințele medicale ale infecției cu VHB sunt atât variabile, cât și imprevizibile, în funcție de factori precum vârsta pacientului și starea imunitară. VHB este un agent etiologic bine recunoscut pentru hepatita cronică, ciroza hepatică și carcinomul hepatocelular.
Cu toate acestea, există mari diferențe în ceea ce privește prevalența infecției, ceea ce a dus la stabilirea a trei zone majore de endemie ridicată, medie și scăzută (2). În majoritatea țărilor dezvoltate, prevalența purtătorilor cronici de VHB este mai mică de 2%, iar transmiterea infecției are loc, mai ales, la adulții aparținând anumitor grupuri de risc (consumatori de droguri, bărbați homosexuali, heterosexuali promiscui, lucrători din domeniul sănătății) (3). În Spania, s-a constatat o prevalență de 1,2% a purtătorilor de VHB (4), iar identificarea AgHBs la donatorii de sânge, la femeile însărcinate și la subiecții supuși programelor de autotransfuzie este obligatorie.
Tehnica de grupare a serului încearcă să reducă costurile fără a pierde din eficacitate și a fost utilizată în principal în țările în curs de dezvoltare în căutarea anticorpilor împotriva virusului imunodeficienței umane (HIV) (5-14), și a virusului hepatitei C (VHC) (15-19). Rezultatele obținute cu această metodă s-au dovedit extrem de promițătoare, deoarece au scăzut semnificativ costul testelor de laborator fără a diminua semnificativ sensibilitatea acestora.
Studiul de față încearcă să evalueze dacă tehnica de grupare a serului este aplicabilă în detectarea AgHBs, pentru a elucida factorii care îi pot modifica sensibilitatea și pentru a efectua o analiză cost-beneficiu pentru această tehnică de diagnosticare.
Materiale și metode
Determinarea HBsAg
Pentru evaluarea HBsAg a fost utilizat testul Imx HBsAg (Abbott Laboratories, Abbott Park, IL), care este un imunoenzima imunoenzimatic (EIA) calitativ cu microparticule de a treia generație. Prezența sau absența HBsAg este determinată prin compararea ratei de formare a produsului fluorescent cu o valoare limită, care este calculată din rata calibratorului negativ (N) (plasmă umană nereactivă pentru HBsAg). Testul Imx HBsAg calculează un raport între rata eșantionului (S) și rata calibratorului negativ. Valoarea limită (S/N) a fost stabilită la 2 pentru EIA cu un singur ser.
Tehnica de pooling se realizează prin adăugarea a 200 mcL la pool, adică prin obținerea unui amestec de 40 mcL din fiecare dintre cele 5 seruri care alcătuiesc pool-ul (diluție 1/5). Cutoff-ul a fost stabilit ca fiind media probelor negative plus 3 deviații standard, obținându-se astfel o valoare de 1. Se consideră, prin urmare, că există o probă nereactivă în acest grup de 5 atunci când coeficientul S/N este < valoarea de cutoff, în timp ce un pool S/N > cutoff poate indica prezența a cel puțin o probă reactivă. În acest caz, este necesar să se testeze din nou probele individuale pentru a identifica proba (probele) reactivă (e). Toate testele se efectuează în dublu exemplar.
În conformitate cu cele de mai sus, specificitatea a fost evaluată prin evaluarea HBsAg în 50 de pool-uri de 250 de seruri negative. Pentru a calcula sensibilitatea, 40 de seruri cu aceeași distribuție a concentrației ca și populația generală din care au fost prelevate au fost testate într-un pool cu 4 seruri negative.
Subtipurile HBsAg (ad și ay)
Limita de detecție a Imx HBsAg pentru ad și ay a fost evaluată folosind seruri dintr-un panel de subtipuri HBsAg purificate (panel de sensibilitate HBsAg pentru hepatită, Abbott Laboratories). Concentrațiile HBsAg/ad și HBsAg/ay au variat de la 0,13 la 2,32 ng/mL și, respectiv, de la 0,21 la 2,24 ng/mL. Limita de detecție a fost determinată în seruri unice și într-un grup cu 4 seruri HBsAg negative.
Influența nivelului de anti-HBs
Pentru a stabili dacă existența anticorpilor anti-HBs în serurile studiate cu ajutorul testului în pool ar putea neutraliza HBsAg și interfera cu sensibilitatea tehnicii, am aplicat metoda de grupare a unui ser cu o concentrație cunoscută de HBsAg/ad și HBsAg/ay cu patru seruri cu titru cunoscut de anti-HBs.
Determinarea cantitativă a anti-HBs a fost efectuată cu o metodă de imunodozare enzimatică cu microparticule (mEIA) folosind un autoanalizator AxSYm (AxSYmTM AUSAB, Abbott Laboratories, Abbott Park, IL). Serurile cu titruri ridicate de anti-HBs au fost obținute de la controale post-vaccinate anti-HBs și de la pacienți care s-au vindecat de hepatita B.
Pool-test în screeningul HBsAg
Pentru a evalua validitatea testării în grup, s-a efectuat o simulare a operațiunilor de teren prin metoda de mai sus pe 1 525 de probe de ser obținute de la femei însărcinate în cadrul unui studiu anterior realizat de noi pentru a estima prevalența infecției cu VHC, și ale căror probe au fost păstrate la -20 ºC de la recoltare. Dintre acestea, am selectat aleatoriu 300 de probe de AgHBs negative și 14 probe de AgHBs pozitive. Determinările au fost făcute fără cunoașterea prealabilă a compoziției pool-ului.
Reducerea numărului de teste
Când un pool are un rezultat pozitiv, este necesară retestarea individuală a fiecărui component pentru a identifica proba sau probele care sunt pozitive la HBsAg. Astfel, cu cât este mai mare numărul de pool-uri pozitive (adică prevalența HBsAg), cu atât mai mică este reducerea numărului de teste efectuate.
Pe această bază, reducerea procentuală a numărului de teste atunci când s-au utilizat pool-uri de seruri pentru depistarea HBsAg, a fost calculată în condițiile cele mai nefavorabile și improbabile (prevalență scăzută), adică atunci când nu a fost prezent mai mult de un ser pozitiv în niciunul dintre pool-uri. De exemplu, pentru o seroprevalență HBsAg de 2%, dacă se analizează 100 de seruri în 20 de pool-uri, 2 dintre acestea vor fi pozitive. Prin urmare, este necesar să se adauge 10 determinări (10 seruri retestate individual) la cele 20 inițiale (20 de bazine), obținându-se astfel 30 de determinări în total. În acest exemplu, se poate economisi 70% din costuri. Pentru a efectua o analiză cost-beneficiu, prețul testării HBsAg a fost estimat la 3 dolari SUA pentru fiecare probă. Acesta fiind bazat pe prețul mediu real al kitului comercial din spitalul nostru.
Analiză statistică
Datele au fost colectate într-o bază de date și analizate ulterior cu ajutorul pachetului statistic SPSS pentru Windows, versiunea 10.0. S-a utilizat corelația liniară non-parametrică a lui Spearman. Rezultatele sunt exprimate ca medie ± SD. Un nivel de p < 0,05 a fost considerat semnificativ din punct de vedere statistic.
Rezultate
Niciunul dintre cele 50 de pool-uri de seruri HBsAg-negative nu a rezultat pozitiv (pool S/N > 1), iar următoarele valori ale pool-ului S/N au fost obținute: 0,767 ± 0,076 (interval 0,67-0,88). Cu acest eșantion, specificitatea acestei tehnici de grupare a fost, prin urmare, de 100 %. Pe de altă parte, toate cele 40 de seruri HBsAg-pozitive, atunci când au fost determinate sub formă de pool, au dat valori S/N mai mari de 1 (sensibilitatea fiind, de asemenea, de 100%). Coeficientul de corelație între rapoartele S/N pentru aceste 40 de probe, așa cum au fost studiate individual și în pool, a fost de 0,792 (p < 0,05).
Vreo 26,6% din pool-urile cu probe cu titruri ridicate de HBsAg au avut un raport S/N chiar mai mare decât cel al probei individuale. Cu toate acestea, coeficientul de corelație al eșantioanelor cu titruri scăzute de AgHBs (S/N unic < 25, n = 12) a fost excelent (R = 0,9739, p < 0,05), după cum se poate observa (Fig. 1).

Limita de detecție folosind metoda unică a fost de 0,5 %.34 ng/mL pentru subtipul ad și 0,29 ng/mL pentru subtipul ay, în timp ce pentru metoda de grupare au fost detectate niveluri mai scăzute de antigen: 0,20 ng/mL și, respectiv, 0,12 ng/mL. Sunt prezentate rezultatele aplicării tehnicilor simple și grupate la seruri cu diferite concentrații de HBsAg/ad și HBsAg/ay (Fig. 2).

Când titrul anti-HBs din grup este mai mic de 100 UI/L, tehnica nu-și pierde sensibilitatea; chiar și atunci când titrul anti-HBs ajunge la 10.000 UI/L, tehnica este încă capabilă să detecteze concentrații de HBsAg de până la 1,5 ng/mL. Este prezentată influența diferitelor concentrații de anti-HBs asupra limitei de detecție a subtipurilor HBsAg atunci când se utilizează metoda de pooling (media a 2 determinări) (Fig. 3).
În investigația efectuată în condiții reale în serurile de femei gravide, metoda de pooling a dus la clasificarea corectă a tuturor probelor analizate. În consecință, sensibilitatea și specificitatea au fost de 100%.
Există o scădere a procentului de reducere a numărului de teste realizat cu metoda de pooling pe măsură ce crește seroprevalența AgHBs. Se poate observa că, chiar și cu prevalențe ale AgHBs de până la 10% în eșantionul studiat, se atinge o economie minimă de cel puțin 30% (Fig. 4).

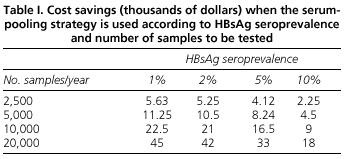
Analiza beneficiilor economice ale strategiei de punere în comun a serului arată că economiile realizate depind atât de prevalența AgHBs, cât și de numărul de determinări care trebuie efectuate. Astfel, pentru țările cu o prevalență scăzută, cum este cazul țării noastre, metoda de pooling reduce costul testării pentru HBsAg. De exemplu, am estimat că în cazul a 2.500 de determinări efectuate într-un laborator pe parcursul unui an prin metoda de pooling, economiile vor fi de 5.630 de dolari americani, iar în cazul unui spital foarte aglomerat care efectuează 20.000 de determinări anual, economiile vor ajunge la 45.000 de dolari americani (tabelul I).
Discuție
O abordare a metodei de pooling constă în menținerea diluției și a volumului final al amestecului de reacție în fiecare test pus în comun pentru a nu pierde din sensibilitate, pentru care se reduce diluantul și se înlocuiește parțial cu serurile suplimentare. În acest fel, nu este necesar să se modifice valoarea de cutoff în raport cu metoda standard în probele individualizate. Cu toate acestea, metoda utilizată în studiul nostru a fost automatizată, iar diluția probelor a fost realizată de un autoanalizator. Din acest motiv, fiecare eșantion prezintă o diluție de 1 la 5 la amestecarea cu celelalte 4 seruri. Prin urmare, în studiul nostru a fost necesar să modificăm valoarea de cutoff și să limităm numărul de seruri din pool pentru a nu pierde din sensibilitate.
În ceea ce privește specificitatea, este necesar să remarcăm faptul că valoarea medie pentru pool-uri a fost doar puțin peste 3 deviații standard față de cutoff. Astfel, un fals pozitiv ar putea fi așteptat în aproximativ 1% din ocazii. Considerăm că acest lucru este acceptabil, deoarece specificitatea este de aproape 100% (99,9%). Va fi necesar un studiu cu un număr mai mare de probe negative de la un număr mare de indivizi diferiți pentru a stabili adevărata specificitate a acestui test.
Deși corelația dintre testele cu probe unice și cu probe grupate este bună, linia de regresie interceptează axa X la un raport S/N de 3 (valoarea corespunzătoare a lui Y este 1). Acest lucru poate însemna că orice eșantion cu un raport S/N între 2 și 3 în testul pe eșantion unic ar avea o valoare sub 1 și, prin urmare, nu ar fi detectat în testul combinat.
Pentru o prevalență de 1% de seruri pozitive la AgHBs, un model matematic descris de Liu et al. (19) a obținut reducerea maximă (80,5%) a numărului de teste pentru o dimensiune a lotului de 11 seruri. Cu toate acestea, după părerea noastră, ar putea apărea o problemă cu privire la specificitate din cauza efectului grupării asupra ratei fals-pozitive. O creștere a proteinelor nespecifice, ca urmare a amestecului de seruri, poate da naștere la o creștere a culorii de fond. Cu dimensiunea pool-ului de 5 aleasă pentru studiul nostru și cu modificarea valorii de separare de la 2 la 1, nu au fost observate pierderi de sensibilitate (falsuri negative) sau de specificitate (falsuri pozitive).
Rezultatele prezentului studiu arată că tehnica de grupare a serurilor pentru detectarea AgHBs este foarte sensibilă și specifică și permite, de asemenea, economii economice considerabile. Aceste constatări sunt similare cu cele obținute de alți cercetători care au aplicat metoda de pooling la studiul infecției cu VHC și HIV (5-19). Până în prezent, au fost raportate doar două studii (20,21) privind aplicarea metodei de pooling la studiul infecției cu VHB. Într-unul dintre acestea (20), realizat cu ocazia efectuării unui screening antenatal de rutină pentru hepatita B prin testarea a 10 pool-uri de probe, autorii au constatat o prevalență scăzută a purtătorilor cronici (0,43%) și concluzionează că aceasta este o metodă eficientă din punct de vedere al costurilor și o strategie valabilă în zonele cu seroprevalență scăzută, cu o reducere a sensibilității estimată la 4,2%. Aplicarea în studiul nostru a metodei de grupare la femeile gravide, în rândul cărora prevalența purtătorilor cronici de AgHBs este de 0,93%, a demonstrat o sensibilitate și o specificitate de 100%.
Distribuția celor două subtipuri majore de AgHBs (ad și ay) în mediul nostru este de aproximativ 50% pentru fiecare dintre ele, ay fiind mai frecventă la toxicomanii care utilizează calea parenterală (22). Am demonstrat că metoda de grupare îmbunătățește sensibilitatea, adică scade limita de detecție a unui imunoanalizator utilizat pentru determinarea celor două subtipuri majore de HBsAg. Tehnica noastră de pooling permite detectarea unor cantități de până la 0,20 ng/mL de HBsAg/ad și 0,12 ng/mL de HBsAg/ay, chiar mai mici decât cele obținute cu metoda standard. Constatarea unei sensibilități crescute în cazul testării prin pool nu este surprinzătoare, deoarece acest lucru a fost raportat și de alți autori (16). Este important să se evalueze sensibilitatea kitului EIA utilizat pentru testul pool, deoarece nu toate kiturile pot fi adecvate pentru screeningul pool-urilor, așa cum s-a demonstrat în cazul anticorpilor împotriva virusului hepatitei C (23,24).
Prezența anti-HBs în serurile pool-urilor ar putea modifica sensibilitatea tehnicii, dar numai într-un mod semnificativ la titruri mai mari de 10.000 UI/mL, observate numai în probele din studiile de control post-vaccinare; în această situație, determinarea HBsAg nu este indicată. De fapt, Cunninghan și colab. (20) au constatat că numai 4,5% din pool-urile alcătuite cu seruri de femei gravide au avut un titru anti-HBs mai mare de 7.500 UI/L. Ținând cont de această limitare a sensibilității metodei de pooling, ei au constatat că aceasta a fost, de asemenea, de aproximativ 100% în ceea ce privește sensibilitatea și specificitatea. Rezultatele noastre ar putea fi reproductibile în alte zone cu prevalență scăzută, dar ar trebui să fie demonstrate anterior în zone cu o endemicitate ridicată pentru VHB. În aceste zone, majoritatea populației este deja imunizată împotriva acestui virus și este posibil ca titrurile anti-HBs găsite în seruri să fie ușor crescute.
Rabenau și colab. (21) au studiat siguranța testelor serologice în pool-uri de plasmă pentru HBsAg folosind un sistem EIA similar cu al nostru. În studiul lor, detectarea AgHBs a fost influențată de prezența unor titruri anti-HBs scăzute după 5 ore de incubare. Cu toate acestea, în urma disocierii complexului imun, HBsAg a fost încă detectabil în pool chiar și în prezența unui conținut ridicat de anti-HBs. În studiul nostru am demonstrat că doar o scădere semnificativă a sensibilității rezultă pentru titruri anti-HBs mai mari de 10.000 UI/L. Aceste diferențe se pot datora faptului că, în cazul nostru, probele au fost testate fără incubare prealabilă. Acest lucru ar putea împiedica neutralizarea antigenului prin formarea de imunocomplecși.
Prin urmare, considerăm că, atât titrul de anti-HBs din ser, cât și prelucrarea prealabilă a probelor cu EIA pot influența sensibilitatea metodei de pooling. Fiecare laborator care dorește să utilizeze această tehnică ar trebui să țină cont de acești doi factori înainte de a o utiliza în mod general.
OMS recomandă utilizarea metodei de pooling seric în cazul infecției cu HIV, atunci când prevalența bolii este mai mică de 2%, și cu un pooling de maximum 5 seruri (25). Urmând aceste indicații, majoritatea studiilor aplică și recomandă utilizarea tehnicilor de pooling în zonele cu seroprevalență scăzută. În studiul nostru, demonstrăm că punerea în comun a serurilor poate fi, de asemenea, rentabilă în populațiile cu o prevalență ridicată a purtătorilor de AgHBs. Acest lucru ar putea permite utilizarea sa în țările aparținând zonelor de endemie medie și ridicată pentru infecția cu VHB, care, în general, coincide cu țările subdezvoltate sau în curs de dezvoltare, adică cele care au o nevoie mai mare de reducere a costurilor economice implicate de testele de laborator. Cu toate acestea, va fi necesar să se efectueze studii similare în aceste zone pentru a confirma rezultatele noastre. Cu toate acestea, s-a demonstrat deja că, în țări precum Kenya, care are o frecvență ridicată a infecției cu HIV (7,3 %), aplicarea pooling-ului pentru depistarea acesteia ar permite economii economice de 62 %, fără pierderi semnificative în materie de siguranță (14). În Spania, o țară care aparține unei zone cu endemie scăzută pentru infecția cu VHB și cu o frecvență a purtătorilor de AgHBs în populația generală de 1,2% (4), poate fi utilizat în toate acele grupuri în care depistarea AgHBs este în prezent obligatorie (cum ar fi donatorii de sânge, subiecții supuși programelor de autotransfuzie, depistarea femeilor însărcinate).
Studiul cost-beneficiu al aplicării tehnicilor de depistare a purtătorilor cronici de VHB permite să se demonstreze că economiile economice sunt mai mari atunci când se realizează un număr mare de determinări în grupe cu seroprevalență scăzută, iar utilizarea sa ar putea fi rentabilă și în zonele cu o prevalență ridicată a infecției și chiar în laboratoarele care efectuează un număr mic de determinări. Am demonstrat economiile economice în funcție atât de diferitele prevalențe HBsAg, cât și de numărul de teste care trebuie efectuate anual. În zona noastră, aplicarea metodei de pooling ar putea economisi aproximativ 74% din costurile economice totale în comparație cu metoda unică.
Unii cercetători au început recent să practice strategii de detectare a acizilor nucleici virali la donatorii de sânge utilizând reacția în lanț a polimerazei (PCR) pentru a crește siguranța implicată în transfuzia de derivate sanguine (26-29). Datorită faptului că nu este posibil să se efectueze depistări individuale din cauza problemelor economice și a volumului de muncă implicat, se utilizează în prezent metoda de grupare a probelor de sânge serologic negativ. Această procedură ar putea crește siguranța sângelui printr-un screening sistematic al donațiilor de sânge la un cost relativ scăzut. Având în vedere că una dintre principalele limitări în practicarea acestor metode este de ordin economic, credem că, prin studiul nostru, ar putea exista o bază teoretică pentru utilizarea screening-ului pentru infecțiile cu VHB, VHC și HIV în două etape, la un cost economic relativ scăzut. În prima fază, un EIA comercial ar putea fi aplicat la un grup de seruri de donatori; în a doua fază, aplicarea tehnicilor PCR la un grup de probe seronegative ar putea crește siguranța analizei. Până când studiile viitoare vor putea dovedi valoarea acestei tehnici în cazul donatorilor de sânge, considerăm că aceasta ar putea fi aplicată doar la testele de diagnostic și epidemiologice.
Concluzionăm că aplicarea EIA la grupaje de seruri este o metodă sensibilă și specifică în detectarea celor două subtipuri majore de AgHBs într-o zonă cu seroprevalență scăzută. Sensibilitatea scade doar atunci când există titruri foarte ridicate de anti-HBs în serurile grupate. Tehnica de grupare este o metodă care poate permite, de asemenea, realizarea de economii financiare dacă este utilizată în studiul populațiilor cu o prevalență ridicată a purtătorilor de AgHBs. Considerăm că sunt necesare studii suplimentare pentru a confirma aceste constatări.
Recunoștințe
Vrem să-i mulțumim lui David H. Wallace (membru al Asociației Europene a Editorilor de Știință și al Consiliului Editorilor Biologici) pentru traducerea în limba engleză a manuscrisului.
1. Maynard JE. Hepatita B: importanța globală și nevoia de control. Vaccine 1990; 8 (Supl.): 18s-20s.
2. Margolis HS, Alter MJ, Hadler SC. Hepatita B: epidemiologie în evoluție și implicații pentru control. Sem Liver Dis 1991; 11: 84-92.
3. Alter MJ, Mast EE. Epidemiologia hepatitei virale în Statele Unite. Gastroenterol Clin North Am 1994; 23: 437-55.
4. Suárez A, Riestra S, Navascués CA, et al. Donatori de sânge HBsAg pozitivi în Asturias (Spania): prevalența actuală și semnificația sa. (rezumat în limba engleză). Med Clin (Barcelona) 1994; 102: 329-32.
5. Emmanuel JC, Basset MT, Smith HJ, Jacobs JA. Punerea în comun a serurilor pentru testarea virusului imunodeficienței umane (HIV): o metodă economică pentru utilizarea în țările în curs de dezvoltare. J Clin Pathol 1988; 41: 582-5.
6. Kline RL, Brothers TA, Brookmeyer R, et al. Evaluarea seroprevalenței virusului imunodeficienței umane în cadrul anchetelor de populație care utilizează seruri puse în comun. J Clin Microbiol 1989; 27: 1449-52.
7. Cahoon-Young B, Chandler A, Livermore T, et al. Sensitivity and specificity of pooled versus individual sera in a human immunodeficiency virus antibody prevalence study. J Clin Microbiol 1989; 27: 1893-5.
8. Frosner GG, Dobler G, Dobler G, von Sonnenburg FJ. Reducerea costurilor testelor nemijlocite pentru depistarea anti-HIV prin investigarea serurilor grupate. AIDS 1990; 4: 73-5.
9. Behets F, Bertozzi S, Kasali M, et al. Utilizarea cu succes a serurilor grupate pentru a determina seroprevalența HIV-1 în Zair cu dezvoltarea modelelor de eficiență a costurilor. AIDS 1990; 4: 737-41.
10. Monzon OT, Paladin FJ, Dimaandal E, et al. Relevanța conținutului de anticorpi și a formatului testului în testarea HIV a serurilor grupate. AIDS 1992; 6: 43-8.
11. Tamashiro H, Maskill W, Emmanuel J, et al. Reducerea costului testării anticorpilor HIV. Lancet 1993; 342: 87-90.
12. Perriens JH, Magazani K, Kapila N, et al. Utilizarea unui test rapid și a unui test ELISA pentru depistarea anticorpilor HIV din probe de ser reunite în Lubumbashi, Zair. J Virol Methods 1993; 41: 213-21.
13. McMahon EJ, Fang C, Layug L, Sandler SG. Punerea în comun a probelor donatorilor de sânge pentru a reduce costul testării anticorpilor HIV-1. Vox Sang 1995; 68: 215-9.
14. Verstraeten T, Farah B, Duchateau L, Matu R. Pooling sera pentru a reduce costul supravegherii HIV: un studiu de fezabilitate într-un district rural din Kenya. Trop Med Int Health 1998; 3: 747-50.
15. 15. Kamel MA, Ghaffar YA, Wasef MA, et al. Prevalența ridicată a VHC la donatorii de sânge egipteni. Lancet 1992; 340: 427.
16. Neil AGS, Conradie JD. Screening anti-HCV cu costuri reduse al donatorilor de sânge. Lancet 1992; 340: 1096.
17. Fernández E, Riestra S, García S, Rodríguez S. Teste de pool pentru detectarea infecției cu virusul hepatitei C. J Hepatol 1995; 23: 236.
18. García Z, Taylor L, Ruano A, et al. Evaluarea unei metode de pooling pentru depistarea de rutină anti-HCV a donatorilor de sânge pentru a reduce povara costurilor pentru băncile de sânge din țările în curs de dezvoltare. J Med Virol 1996; 49: 218-22.
19. Liu P, Shi ZX, Shi ZX, Zhang YC, et al. Studiu prospectiv al unei strategii de punere în comun a serului în screeningul donatorilor de sânge pentru depistarea anticorpilor la virusul hepatitei C. Transfuzii 1997; 37: 732-6.
20. 21. Cunningham R, Northwood JL, Kelly CD, et al. Screening antenatal de rutină pentru hepatita B utilizând seruri grupate: validare și revizuire a unei experiențe de 10 ani. J Clin Pathol 1998; 51: 392-5.
21. Rabenau H, Schutz R, Berger A, et al. Cât de precisă este testarea serologică a pool-urilor de plasmă pentru antigenul de suprafață al virusului hepatitei B, anti virusul imunodeficienței umane 1 și 2 și anti virusul hepatitei C? (rezumat în limba engleză). Infus Transfus 1996; 23: 124-30.
22. Echevarría JE, León P, López JA, et al. Distribuția subtipului HBsAg în rândul diferitelor populații de purtători HBsAg din Spania. Eur J Epidemiol 1995; 11: 39-45.
23. Neill AGS, Conradie JD. Teste de pool pentru virusul hepatitei C. Lancet 1994; 343: 738.
24. Liu P, Shi ZX, Shi ZX, Zhang YC, Zhang XY. Studiu comparativ asupra a 4 kituri EIA pentru depistarea anticorpilor la virusul hepatitei C în seruri grupate. Biomed Environ Sci 1998; 11: 75-80.
25. Recomandări pentru testarea anticorpilor HIV pe fondul de seruri. WHO Weekly Epidemiol Rec 1991; 44: 316-27.
26. Lefrere JJ, Coste J, Defer C, et al. Screening blood donations for viral genomes: studiu multicentric de simulare în timp real utilizând probe grupate pe modelul de detectare a ARN al virusului hepatitei C. Transfusion 1998; 38: 915-23.
27. Yerly S, Pedrocchi M, Perrin L. Utilizarea reacției în lanț a polimerazei în pool-uri de plasmă pentru detectarea concomitentă a virusului hepatitei C și a ARN-ului HIV tip 1. Transfusion 1998; 38: 908-14.
28. Schottstedt V, Tuma W, Bunger G, Lefevre H. PCR pentru VHB, VHC și HIV-1 experiențe și primele rezultate ale unui program de screening de rutină într-un mare serviciu de transfuzii de sânge. Biologicals 1998; 26: 101-4.
29. Morandi PA, Schockmel GA, Schockmel GA, Yerly S, et al. Detectarea ARN-ului virusului imunodeficienței umane de tip 1 (HIV-1) în bazine de seruri negative pentru anticorpii împotriva HIV-1 și HIV-2. J Clin Microbiol 1998; 36: 1534-8.
Lasă un răspuns