INTRODUCTION
Nachylenie zależności ciśnienie-objętość w końcowym okresie skurczu, określane przez Sugę i Sagawę jako Emax,1 było brane pod uwagę przy ocenie kurczliwości ze względu na wrażliwość na zmiany inotropowe i względną niezależność od obciążenia komory. Ponieważ określenie Emax wymaga uzyskania krzywych ciśnienie/objętość przy różnych obciążeniach, podjęto próby zidentyfikowania uproszczonego wskaźnika u ludzi.2 Zmienność między spoczynkową i szczytową obciążeniową zależnością ciśnienie-objętość końcowoskurczowa (ESPVR; wskaźnik Sugi) jest łatwa do uzyskania podczas rutynowej echokardiografii obciążeniowej i została uznana za niezależny od obciążenia wskaźnik kurczliwości mięśnia sercowego3-11 , który pozwala na dokładniejszą stratyfikację prognostyczną niż frakcja wyrzutowa u pacjentów bez indukowalnych zaburzeń kurczliwości.12-15
Jednakże, podobnie jak większość wskaźników, ESPVR nie uwzględnia wymiarów rozkurczowych lewej komory. Suga i wsp.16 opisali zależność wielkości Emax w warunkach eksperymentalnych i od tego czasu podkreśla się, że wskaźniki funkcji lewej komory (LV) u ludzi powinny być normalizowane17,18 , aby umożliwić porównanie funkcji skurczowej u różnych pacjentów. Obecne badanie miało na celu odniesienie wskaźnika ESPVR uzyskanego podczas echokardiografii obciążeniowej w spoczynku oraz ΔESPVR (różnica między szczytowym i spoczynkowym ESPVR) do objętości końcoworozkurczowej LV (LVEDV) zarówno w grupie kontrolnej, jak i u pacjentów.
METODY
Od stycznia 2003 roku 1142 pacjentów poddano echokardiografii obciążeniowej w kontrolowanych pod względem jakości laboratoriach echokardiografii obciążeniowej.9,11,12,14,19-23 Badanie było zgodne z Deklaracją Helsińską. Przed badaniem od wszystkich pacjentów (lub ich opiekunów) uzyskano świadomą zgodę, a protokół badania został zatwierdzony przez instytucjonalną komisję etyczną. Dane z echokardiografii obciążeniowej były zbierane i analizowane przez echokardiografistów niezaangażowanych w opiekę nad pacjentem. Kryteriami wyłączenia były: istotna wrodzona choroba serca, niezadowalające obrazowanie lewej komory w spoczynku lub podczas stresu, migotanie przedsionków lub dodatni wynik echokardiografii obciążeniowej. Z początkowej populacji 1142 pacjentów 118 zostało wykluczonych z powodu dodatniego wyniku echokardiografii obciążeniowej, 11 z powodu wrodzonej choroby serca, 18 z powodu migotania przedsionków, a 41 z powodu niezadowalającego wyniku echokardiografii obciążeniowej. W ten sposób do badania włączono 891 pacjentów, 593 (67%) mężczyzn i 298 (33%) kobiet; średni wiek wynosił 63 ± 12 lat, a średnia frakcja wyrzutowa 47% ± 12%, z ujemnym wynikiem echa wysiłkowego według kryteriów kurczliwości. Dane były zbierane prospektywnie i analizowane retrospektywnie. Pacjentów podzielono ex-post na następujące grupy: normalna, n = 91; idiopatyczna kardiomiopatia rozstrzeniowa, n = 222; znana choroba wieńcowa, n = 331 (kardiomiopatia niedokrwienna rozstrzeniowa, n = 102; nierozstrzeniowa, n = 229); badania diagnostyczne, n = 162, i nadciśnienie tętnicze, n = 85.
Grupa normalna składała się z uczestników z prawidłową czynnością LV w warunkach wyjściowych i przy szczytowym obciążeniu, którzy nie byli leczeni w czasie badania. Badania diagnostyczne obejmowały testy wysiłkowe u pacjentów z niskim wstępnym prawdopodobieństwem choroby wieńcowej, nieprawidłowościami elektrokardiogramu (EKG) w spoczynku lub elektrokardiografii wysiłkowej oraz brakiem poszerzenia LV. Rozpoznanie choroby wieńcowej stawiano na podstawie przebytego zawału serca lub rewaskularyzacji wieńcowej w wywiadzie i/lub obecności ≥ 1 udokumentowanego angiograficznie zwężenia tętnicy wieńcowej > 50%.
Użyty stresor (wysiłkowy, dipirydamol, dobutamina) wybierano na podstawie specyficznych przeciwwskazań, lokalnych możliwości i preferencji lekarza. Dobutamina była preferowanym stresorem do oceny żywotności.24
Dwuwymiarowe badanie echokardiograficzne i 12-odprowadzeniowe monitorowanie elektrokardiograficzne wykonywano w połączeniu z półsupinowym wysiłkiem rowerowym lub dobutaminą w dużej dawce (do 40μg/kg/min) lub dipirydamolem w dużej dawce (84mg/kg/min, przez 6min), zgodnie z protokołami sugerowanymi przez wytyczne European Association of Echocardiography24. Podczas zabiegu co minutę rejestrowano ciśnienie tętnicze i EKG. Obrazy echokardiograficzne oceniano półilościowo, stosując 17-segmentowy model lewej komory w 4-punktowej skali.24 Wskaźnik oceny kurczliwości uzyskano, dzieląc sumę ocen poszczególnych segmentów przez liczbę segmentów możliwych do interpretacji. Frakcję wyrzutową LV (LVEF) oceniano za pomocą dwupłaszczyznowej metody Simpsona.25 Niedokrwienie definiowano jako wywołane stresem pojawienie się i/lub pogorszenie wcześniej istniejących zaburzeń kurczliwości lub odpowiedź dwufazową (tj. poprawa po małej dawce, a następnie pogorszenie po dużej dawce). W drodze selekcji, wszyscy pacjenci mieli negatywne echo stresu według kryteriów kurczliwości. Poprawa wskaźnika wall motion score między spoczynkiem a szczytem stresu wskazywała na żywotność mięśnia sercowego.26
Objętość końcowoskurczową LV (LVESV) i LVEDV uzyskuje się w projekcji koniuszkowej 4-jamowej i 2-jamowej za pomocą dwupłaszczyznowej metody Simpsona.12,19,25 LVESV i LVEDV ocenia się w spoczynku i w szczycie stresu, a następnie normalizuje, dzieląc je przez powierzchnię ciała. Pomiaru dokonuje się tylko w reprezentatywnych cyklach z optymalną wizualizacją wsierdzia, przyjmując średnią z 3 pomiarów. Wyznacza się granicę wsierdzia z pominięciem mięśni brodawkowatych. Za ramkę końcowoskurczową uznaje się ramkę z najmniejszą jamą LV, a za ramkę końcoworozkurczową ramkę uchwyconą w załamku R EKG. Ciśnienie końcowoskurczowe LV (mmHg) uzyskuje się jako ciśnienie końcowoskurczowe LV = 0,9 × skurczowe ciśnienie krwi (mmHg), nieinwazyjną ocenę ciśnienia końcowoskurczowego, która dokładnie przewiduje pomiary ciśnienia końcowoskurczowego za pomocą pętli ciśnieniowo-objętościowej.27
Ciśnienie ESPVR (mmHg/mL/m2) uzyskuje się jako stosunek ciśnienia końcowoskurczowego do LVESV indeksowanej do powierzchni ciała. ESPVR określa się w spoczynku i przy szczytowym obciążeniu. Wartość ΔESPVR jest obliczana jako różnica między ESPVR w spoczynku i w szczycie obciążenia. Spoczynkowa ESPVR, szczytowa ESPVR i ΔESPVR są budowane w trybie offline.11,12,19
Analiza statystyczna
Analiza statystyczna została przeprowadzona przy użyciu programu SPSS 22 for Windows i obejmowała statystyki opisowe (częstość i odsetek zmiennych kategorycznych oraz średnia ± odchylenie standardowe zmiennych ciągłych). W celu potwierdzenia istotności przeprowadzono test chi kwadrat Pearsona z dokładnym testem Fishera dla zmiennych kategorycznych oraz test Manna-Whitneya dla zmiennych ciągłych dla porównań międzygrupowych (z zastosowaniem metody Monte Carlo dla porównań na małych próbach). Do porównania zmiennych ciągłych między grupami zastosowano jednokierunkową analizę wariancji (ANOVA), a w przypadku braku jednorodności wariancji test Kruskala-Wallisa dla nieparametrycznych prób niezależnych. Zależność między ESPVR a LVEDV określano w każdej grupie za pomocą analizy regresji liniowej metodą najmniejszych kwadratów. Porównania średnich dokonano za pomocą testu t. Dla wszystkich analiz istotność przypisywano przy P
WYNIKI
Wszystkie badania zostały wykonane przez doświadczonego kardiologa z udokumentowanym doświadczeniem w echokardiografii obciążeniowej, który przeszedł procedury kontroli jakości odczytu echokardiografii obciążeniowej zgodnie z kryteriami przyjętymi w wieloośrodkowych badaniach Echo Persantine International Cooperative i Echo Dobutamine International Cooperative.26 W drodze selekcji dwuwymiarowe pomiary objętości LV były możliwe do wykonania u wszystkich pacjentów. W drodze selekcji żadne badanie nie zostało przerwane z powodu ograniczających działań niepożądanych i żadne badanie nie było pozytywne dla regionalnych zaburzeń kurczliwości. Uwzględniono umiarkowane niedomykalności mitralne: 89 (40%) z 222 pacjentów z idiopatyczną kardiomiopatią rozstrzeniową, 47 (46%) ze 102 pacjentów z niedokrwienną kardiomiopatią rozstrzeniową i 6 (3%) z 229 pacjentów z chorobą niedokrwienną serca miało umiarkowaną niedomykalność mitralną. 331 pacjentów z rozstrzenią serca z umiarkowaną niedomykalnością mitralną lub bez niej miało podobną spoczynkową LVEF (28% ± 7% vs 29% ± 9%, P = ns) i ΔESPVR (0,92 ± 2mmHg/mL/m2 vs 0,87 ± 1,6mmHg/mL/m2, P = ns).
W 60 losowo wybranych pacjentach istniała doskonała zgodność międzyobserwacyjna metodą Blanda Altmana ze średnią ± odchylenie standardowe dla LVEDV w spoczynku (2.3 ± 18 mL; 95% przedział ufności, -38 mL do 34 mL) i w szczycie wysiłku (5,8 ± 16 mL; 95%CI, -38 mL do 26 mL), LVESV w spoczynku (3,6 ± 23 mL; 95%CI, -48 do 41 mL) i w szczycie wysiłku (0,3 ± 13 mL; 95%CI, -27 do 27 mL). Zmienność była mniejsza dla LVEDV i LVESV zarówno w przypadku echa farmakologicznego, jak i wysiłkowego przy niskiej częstości akcji serca (
Objętości lewej komory i zmienne związane ze stresem przedstawiono oddzielnie dla echa wysiłkowego, dipirydamolowego i dobutaminowego w Tabeli 1, Tabeli 2 i Tabeli 3. W spoczynku u osób zdrowych i w każdej grupie pacjentów zaobserwowano odwrotną zależność między ESPVR a objętością końcoworozkurczową (tj. im większa jama LV, tym mniejsza ESPVR) (ryc. 1). Nachylenie wskaźnika ESPVR/LVEDV (marker zależności wielkości stosunku ciśnienia końcoworozkurczowego do objętości) różniło się istotnie między rozszerzoną kardiomiopatią niedokrwienną, rozszerzoną idiopatyczną kardiomiopatią i innymi grupami, ponieważ nachylenie było bardziej strome u pacjentów bez rozszerzonej lewej komory (Figura 1, górne panele). Przy danej objętości końcowo-rozkurczowej średni stosunek ciśnienia końcowo-skurczowego do objętości był wyższy w grupach pacjentów bez rozstrzeni niż w grupach z kardiomiopatią niedokrwienną rozstrzeniową i idiopatyczną kardiomiopatią rozstrzeniową (ryc. 1, dolne panele).
Exercise Stress Echocardiography. Left Ventricular Volumes and Stress-related Variables
| NL | Testy diagnostyczne | HYP | CAD | DC | DCM | |
|---|---|---|---|---|---|---|
| Pacjenci, nie. | 32 | 45 | 15 | 44 | 18 | 18 |
| Wiek, y | 46 ± 16 | 58 ± 13 | 64 ± 7 | 63 ± 8 | 68 ± 8 | 66 ± 9* |
| Wall motion score index | 1.00 ± 0.00 | 1.04 ± 0.21 | 1.14 ± 0.35 | 1.20 ± 0.33 | 1.97 ± 0.30 | 1.99 ± 0.03* |
| Częstotliwość pracy serca, bpm | ||||||
| Odpoczynek | 78 ± 13 | 73 ± 14 | 75 ± 17 | 68 ± 13 | 77 ± 11 | 75 ± 13* |
| Szczytowe naprężenie | 142 ± 16 | 127 ± 22 | 114 ± 15 | 114 ± 18 | 114 ± 13 | 113 ± 21* |
| LVEF, % | ||||||
| Spoczynek | 62 ± 5 | 59 ± 10 | 54 ± 11 | 57 ± 9 | 33 ± 6 | 31 ± 7* |
| Peak stress | 73 ± 8 | 68 ± 11 | 65 ± 9 | 61 ± 11 | 33 ± 11 | 38 ± 10* |
| LVESVI, mL/m2 | ||||||
| Spoczynek | 17 ± 6 | 22 ± 10 | 27 ± 12 | 23 ± 10 | 64 ± 28 | 72 ± 29* |
| Naprężenie szczytowe | 11 ± 3 | 16 ± 8 | 16 ± 7 | 20 ± 11 | 57 ± 25 | 63 ± 31* |
| LVEDVI, mL/m2 | ||||||
| Spoczynek | 46 ± 12 | 52 ± 18 | 56 ± 16 | 51 ± 16 | 95 ± 34 | 103 ± 34* |
| Naprężenie szczytowe | 42 ± 10 | 47 ± 14 | 45 ± 11 | 48 ± 16 | 85 ± 27 | 98 ± 37* |
| Koniec-.ciśnienie skurczowe (mmHg) | ||||||
| Odpoczynek | 116 ± 14 | 119 ± 19 | 138 ± 20 | 118 ± 15 | 106 ± 22 | 107 ± 16* |
| Stres szczytowy | 182 ± 23 | 171 ± 25 | 181 ± 27 | 169 ± 19 | 133 ± 28 | 124 ± 22* |
| Wskaźnik ESPVR, mmHg/mL/m2 | ||||||
| Spoczynek | 7.58 ± 3.26 | 7.20 ± 5.13 | 6.59 ± 4.59 | 6.27 ± 3.24 | 2.00 ± 0.96 | 1.68 ± 0.70* |
| Naprężenie szczytowe | 18,51 ± 6,59 | 14,77 ± 9,52 | 13,37 ± 5,97 | 11.83 ± 8,81 | 2,72 ± 1,15 | 2,46 ± 1,40* |
| ΔESPVR index, mmHg/mL/m2 | 10.93 ± 4.56 | 7.56 ± 6.57 | 6.78 ± 3.20 | 5.56 ± 6.35 | 0.72 ± 0.43 | 0.78 ± 0.78* |
ΔESPVR, zmienność między spoczynkowym i szczytowym wysiłkowym ESPVR; CAD, choroba wieńcowa; DC, rozstrzeniowa kardiomiopatia niedokrwienna; DCM, idiopatyczna kardiomiopatia rozstrzeniowa; ESPVR, zależność ciśnienie końcoworozkurczowe-objętość; HYP, uczestnicy z nadciśnieniem; LVEDVI, wskaźnik objętości końcoworozkurczowej lewej komory; LVEF, frakcja wyrzutowa lewej komory; LVESVI, wskaźnik objętości końcowoskurczowej lewej komory; NL, uczestnicy normalni.
Jeśli nie wskazano inaczej, dane wyrażono jako średnią ± odchylenie standardowe.
P
Dipyridamole Stress Echocardiography. Left Ventricular Volumes and Stress-related Variables
| NL | Testy diagnostyczne | HYP | CAD | DCM | |
|---|---|---|---|---|---|
| Pacjenci, nr. | 33 | 104 | 59 | 140 | 146 |
| Wiek, y | 62 ± 12 | 63 ± 11 | 67 ± 12 | 67 ± 10 | 58 ± 12* |
| Wall motion score index | 1.00 ± 0.00 | 1.01 ± 0.08 | 1.00 ± 0.00 | 1.11 ± 0.23 | 2.30 ± 0.34* |
| Częstotliwość pracy serca, bpm | |||||
| Spoczynek | 71 ± 12 | 70 ± 13 | 71 ± 12 | 67 ± 12 | 76 ± 17* |
| Peak stress | 99 ± 19 | 90 ± 14 | 87 ± 16 | 85 ± 15 | 90 ± 17* |
| LVEF, % | |||||
| Spoczynek | 59 ± 5 | 61 ± 7 | 60 ± 5 | 59 ± 9 | 28 ± 10* |
| Peak stress | 70 ± 7 | 70 ± 9 | 68 ± 8 | 63 ± 10 | 34 ± 13* |
| LVESVI, mL/m2 | |||||
| Spoczynek | 19 ± 4 | 19 ± 6 | 22 ± 7 | 22 ± 9 | 65 ± 30* |
| Naprężenie szczytowe | 12 ± 5 | 15 ± 7 | 18 ± 7 | 20 ± 9 | 56 ± 27* |
| LVEDVI, mL/m2 | |||||
| Spoczynek | 46 ± 10 | 49 ± 12 | 57 ± 14 | 54 ± 16 | 91 ± 39* |
| Stres szczytowy | 42 ± 12 | 49 ± 13 | 56 ± 12 | 53 ± 15 | 85 ± 36* |
| Końcówka-.ciśnienie skurczowe, mmHg | |||||
| Spoczynek | 126 ± 20 | 122 ± 19 | 134 ± 19 | 128 ± 18 | 119 ± 17* |
| Stres szczytowy | 114 ± 17 | 114 ± 19 | 117 ± 19 | 114 ± 21 | 106 ± 17* |
| Wskaźnik ESPVR, mmHg/mL/m2 | |||||
| Odpoczynek | 6.94 ± 1.53 | 7.06 ± 2.75 | 6.45 ± 2.26 | 6.72 ± 3.11 | 2.07 ± 1.08* |
| Naprężenie szczytowe | 10,34 ± 3,41 | 9,24 ± 4,59 | 7,51 ± 3.50 | 6,62 ± 2,82 | 2,42 ± 1,40* |
| ΔESPVR index, mmHg/mL/m2 | 3.40 ± 2.75 | 2.17 ± 2.94 | 1.06 ± 2.49 | -0.10 ± 2.39 | 0.35 ± 0.62* |
ΔESPVR, zmienność między spoczynkową i szczytową ESPVR w stresie; CAD, choroba wieńcowa; DC, rozstrzeniowa kardiomiopatia niedokrwienna; DCM, idiopatyczna kardiomiopatia rozstrzeniowa; ESPVR, zależność ciśnienie końcoworozkurczowe-objętość; HYP, uczestnicy z nadciśnieniem; LVEDVI, wskaźnik objętości końcoworozkurczowej lewej komory; LVEF, frakcja wyrzutowa lewej komory; LVESVI, wskaźnik objętości końcowoskurczowej lewej komory; NL, uczestnicy normalni.
Jeśli nie wskazano inaczej, dane wyrażono jako średnią ± odchylenie standardowe.
P
Dobutamine Stress Echocardiography. Left Ventricular Volumes and Stress-related Variables
| NL | Testy diagnostyczne | HYP | CAD | DC | DCM | |
|---|---|---|---|---|---|---|
| Pacjenci, nie. | 26 | 13 | 11 | 45 | 84 | 58 |
| Wiek, y | 60 ± 11 | 70 ± 10 | 69 ± 8 | 66 ± 10 | 67 ± 9 | 65 ± 10* |
| Wall motion score index | 1.00 ± 0.00 | 1.11 ± 0.26 | 1.29 ± 0.41 | 1.31 ± 0.39 | 2.32 ± 0.35 | 2.14 ± 0.34* |
| Częstotliwość pracy serca, bpm | ||||||
| Odpoczynek | 60 ± 5 | 65 ± 7 | 68 ± 19 | 65 ± 9 | 72 ± 14 | 76 ± 15* |
| Szczytowe naprężenie | 155 ± 15 | 126 ± 17 | 142 ± 21 | 133 ± 15 | 109 ± 22 | 117 ± 18* |
| LVEF, % | ||||||
| Spoczynek | 60 ± 6 | 57 ± 9 | 55 ± 9 | 54 ± 9 | 28 ± 6 | 30 ± 7* |
| Peak stress | 71 ± 6 | 67 ± 9 | 64 ± 7 | 63 ± 10 | 40 ± 13 | 42 ± 15* |
| LVESVI, mL/m2 | ||||||
| Spoczynek | 18 ± 5 | 23 ± 9 | 30 ± 13 | 28 ± 12 | 73 ± 26 | 71 ± 29* |
| Peak stress | 10 ± 3 | 16 ± 8 | 19 ± 9 | 21 ± 12 | 57 ± 29 | 55 ± 32* |
| LVEDVI, mL/m2 | ||||||
| Odpoczynek | 45 ± 11 | 53 ± 16 | 65 ± 27 | 60 ± 18 | 99 ± 30 | 100 ± 36* |
| Szczytowe naprężenie | 36 ± 9 | 47 ± 15 | 51 ± 19 | 55 ± 20 | 91 ± 33 | 90 ± 35* |
| Końcówka-.ciśnienie skurczowe, mmHg | ||||||
| Spoczynek | 108 ± 7 | 113 ± 14 | 125 ± 16 | 115 ± 14 | 104 ± 17 | 101 ± 22* |
| Naprężenie szczytowe | 154 ± 10 | 133 ± 26 | 155 ± 18 | 145 ± 30 | 120 ± 24 | 117 ± 25* |
| Wskaźnik ESPVR, mmHg/mL/m2 | ||||||
| Odpoczynek | 6.61 ± 2.17 | 5.71 ± 2.59 | 5.05 ± 2.39 | 4.76 ± 2.03 | 1.62 ± 0.67 | 1.70 ± 0.86* |
| Naprężenie szczytowe | 16,72 ± 6,41 | 10,39 ± 5,81 | 10,32 ± 5,70 | 8.92 ± 4,45 | 2,94 ± 2,60 | 3,41 ± 3,50* |
| ΔESPVR index, mmHg/mL/m2 | 10.12 ± 5.05 | 4.67 ± 4.29 | 5.27 ± 4.69 | 4.16 ± 2.91 | 1.32 ± 2.17 | 1.71 ± 2.86* |
ΔESPVR, zmienność między spoczynkowym i szczytowym wysiłkowym ESPVR; CAD, choroba wieńcowa; DC, rozstrzeniowa kardiomiopatia niedokrwienna; DCM, idiopatyczna kardiomiopatia rozstrzeniowa; ESPVR, zależność ciśnienie końcoworozkurczowe-objętość; HYP, uczestnicy z nadciśnieniem; LVEDVI, wskaźnik objętości końcoworozkurczowej lewej komory; LVEF, frakcja wyrzutowa lewej komory; LVESVI, wskaźnik objętości końcowoskurczowej lewej komory; NL, uczestnicy normalni.
Jeśli nie wskazano inaczej, dane wyrażono jako średnią ± odchylenie standardowe.
P
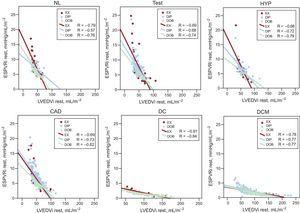
Zależności między ESPVRi a LVEDVi w spoczynku. Zależności między LVEDVi a ESPVRi przedstawiono oddzielnie dla chorych zaplanowanych do EX (symbole czerwone), DIP (symbole niebieskie) i DOB (symbole zielone). Dla każdej grupy chorych przedstawiono wartości regresji liniowej. CAD, choroba wieńcowa; DC, rozstrzeniowa kardiomiopatia niedokrwienna; DCM, idiopatyczna kardiomiopatia rozstrzeniowa; DIP, dipirydamolowe echo wysiłkowe; DOB, dobutaminowe echo wysiłkowe; ESPVRi, wskaźnik zależności ciśnienie końcoworozkurczowe-objętość; EX, wysiłkowe echo wysiłkowe; HYP, uczestnicy z nadciśnieniem tętniczym; LVEDVi, wskaźnik objętości końcoworozkurczowej lewej komory; NL, normalni uczestnicy; Test, pacjenci z testem diagnostycznym.
W ogólnej populacji, odwrotna zależność między ESPVR i LVEDV była obecna w spoczynku (r2 = 0,69, P 2
= 0,56, P 2 = 0,13). Wartość ΔESPVR była najwyższa u osób z prawidłowym lub zbliżonym do prawidłowego ciśnieniem tętniczym oraz u osób z nadciśnieniem tętniczym, a najniższa u pacjentów z niedokrwienną lub nie niedokrwienną kardiomiopatią rozstrzeniową. Bezwzględne wartości ΔESPVR były wyższe dla wysiłku fizycznego i dobutaminy niż dla dipirydamolu. Przy szczytowym obciążeniu, podobnie jak przy obciążeniu podstawowym, u osób zdrowych i w każdej grupie chorych obserwowano odwrotną zależność między ESPVR a objętością końcoworozkurczową (tj. im większa jama LV, tym mniejszy stosunek ciśnienia końcoworozkurczowego do objętości) zarówno w grupie obciążonej wysiłkiem fizycznym, dipirydamolem, jak i dobutaminą.
Zależność ESPVR od objętości końcoworozkurczowej zanikała i/lub istotnie zmniejszała się w stosunku do spoczynku, gdy braliśmy pod uwagę ΔESPVR (tab. 4). Zależności między LVEDV a ΔESPVR przedstawiono oddzielnie dla grup echa wysiłkowego, dipirydamolu i dobutaminowego stresu (ryc. 2, kolorowe symbole) oraz dla normalnych uczestników i pacjentów wewnątrz grupy stresu (ryc. 2, górny i dolny panel).
Size Dependence of the End-systolic Pressure-volume Relation at Rest and During Stress
| Pacjenci, n | Zależność ESPVR od LVEDV | ZależnośćΔESPVR od LVEDV | Zmniejszona korelacja ΔESPVR | Brak korelacji ΔESPVR | Od korelacji ujemnej do dodatniej | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| r | P (2 ogony) | r | P (2 ogony) | |||||||
| NL | ||||||||||
| EX | 32 | -0.785a | -0,240 | .187 | + | |||||
| DIP | 33 | -0,565a | .001 | -0.309 | .080 | + | ||||
| DOB | 26 | -0.756a | -0.418b | .034 | + | |||||
| Test | ||||||||||
| EX | 45 | -0.688a | -0,224 | .139 | + | |||||
| DIP | 104 | -0.675a | -0,365a | + | ||||||
| DOB | 13 | -0.741a | .004 | -0.351 | .240 | + | ||||
| HYP | ||||||||||
| EX | 15 | -0,681a | .005 | -0,142 | .615 | + | ||||
| DIP | 59 | -0.715a | -0.192 | .145 | + | |||||
| DOB | 11 | -0.792a | .004 | 0.095 | .781 | + | + | |||
| CAD | ||||||||||
| EX | 44 | -0,691a | -0,481a | .001 | + | |||||
| DIP | 140 | -0,726a | 0,258a | .002 | + | + | ||||
| DOB | 45 | -0.821a | -0.577a | + | ||||||
| DC | ||||||||||
| EX | 17 | -0,913a | -0,310 | .226 | + | |||||
| DIP | – | . | ||||||||
| DOB | 84 | -0.840a | -0.435a | + | ||||||
| DCM | ||||||||||
| EX | 18 | -0.783a | -0,602a | .008 | + | |||||
| DIP | 146 | -0.768a | -0,191b | .021 | + | |||||
| DOB | 58 | -0,771a | -0.464a | + | ||||||
ΔESPVR, zmiana między spoczynkowym i szczytowym wysiłkowym ESPVR; CAD, choroba wieńcowa; DC, rozstrzeniowa kardiomiopatia niedokrwienna; DCM, idiopatyczna kardiomiopatia rozstrzeniowa; DIP, dipyridamole stress echo; DOB, dobutamine stress echo; ESPVR, end-systolic pressure-volume relation; EX, exercise stress echo; HYP, hypertensive participants; LVEDV, left ventricular end-diastolic volume; NL, normal participants; Test, diagnostic tests.
P
P
P.
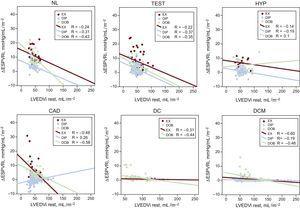
Zależności między ΔESPVRi a LVEDVi. Dla każdej grupy pacjentów reprezentowane są wartości regresji liniowej. Zależności między LVEDVi a ΔESPVRi przedstawiono oddzielnie dla chorych, u których wykonano EX (symbole czerwone), DIP (symbole niebieskie) i DOB (symbole zielone). ΔESPVRi, end-systolic pressure-volume relationship index changes with stress; CAD, coronary artery disease; DC, dilated ischemic cardiomyopathy; DCM, idiopathic dilated cardiomyopathy; DIP, dipyridamole stress echo; DOB, dobutamine stress echo; EX, exercise stress echo; HYP, hypertensives; LVEDVi, left ventricular end-diastolic volume index at rest; NL, normals; Test, diagnostic test patients.
DYSKUSJA
Stosunek ciśnienia końcoworozkurczowego do wskaźnika objętości końcowoskurczowej (wskaźnik Suga) przy wzrastającej częstości akcji serca jest łatwy do uzyskania podczas rutynowej echokardiografii obciążeniowej i został uznany za w miarę niezależny od obciążenia wskaźnik kurczliwości mięśnia sercowego.3
End-systolic Pressure-volume Ratio and End-diastolic Volume Relation at Rest
Stosunek ciśnienie końcowoskurczowe/objętość jest obecnie uznawany za względnie niezależny od obciążenia wskaźnik kurczliwości mięśnia sercowego, ale jego zależność od wielkości komory może ograniczać jego wartość w porównaniach między pacjentami. Foult i wsp.28 dostarczyli dowodów, że stosunek naprężenia końcowoskurczowego do objętości jest wysoce zależny od wielkości komory LV u ludzi i że zależność ta różni się w zależności od charakteru choroby podstawowej mięśnia sercowego. Nasze wyniki wykazują liniową odwrotną zależność między stosunkiem ciśnienia końcoworozkurczowego do objętości i LVEDV u pacjentów z prawidłową lewą komorą i u pacjentów z chorym sercem. Zakres zmienności stosunku ciśnienie końcoworozkurczowe/objętość był taki, że u 2 pacjentów, u których wartość objętości końcoworozkurczowej różniła się o 50%, różnica w stosunku ciśnienie końcoworozkurczowe/objętość wynosiła ≈ 30%. Zależność ta wynika prawdopodobnie z faktu, że podczas gdy ciśnienie w aorcie jest względnie stałe, większa komora miałaby większą objętość końcoworozkurczową. W związku z tym stosunek ciśnienia końcowo-skurczowego do objętości będzie niższy w dużej komorze niż w mniejszym sercu, nawet jeśli można przypuszczać, że wydajność skurczowa jest taka sama. Wyniki te są zgodne z wcześniejszymi danymi29 wskazującymi, że prawidłowa komora dziecka ma większe nachylenie stosunku ciśnienia do objętości w końcowo-skurczowym okresie skurczu niż prawidłowa komora dorosłego. Dlatego na porównanie stanu inotropowego komory u pacjentów z różnymi chorobami za pomocą stosunku ciśnienia końcowoskurczowego do objętości w spoczynku i prawdopodobnie w szczytowym obciążeniu wpływa zależność tego wskaźnika od wielkości komory. Chociaż zależność ta była sugerowana we wcześniejszych doniesieniach,16-18 nie została potwierdzona u dużej liczby pacjentów. Obecne badanie obejmowało dużą serię pacjentów z prawidłową komorą, jak również pacjentów z różnymi typami przerostu lub poszerzenia komory, lub z obiema tymi chorobami, i dlatego dostarcza danych, które mogą rozstrzygnąć problem w klinicznej ocenie funkcji LV.
End-systolic Pressure-volume Ratio and End-diastolic Volume Relation at Peak Stress
Dane z tego badania wykazały, że przy szczytowym obciążeniu (podobnie jak w spoczynku) na stosunek ciśnienia końcoworozkurczowego do objętości wpływała zależność tego wskaźnika od wielkości komory, zwłaszcza u pacjentów z rozstrzeniową kardiomiopatią niedokrwienną lub idiopatyczną, lub z obiema tymi postaciami. Odwrotną zależność między ESPVR a LVEDV stwierdzono u pacjentów z prawidłową lewą komorą oraz u pacjentów z sercem rozstrzeniowym.28 Zależność ESPVR od wielkości doprowadziła do kilku „normalizacji”, jednak we wcześniejszych doniesieniach próby te nie były udane, a znormalizowane wskaźniki nadal zależały od wielkości komory.
End-systolic Pressure-volume Ratio Changes With Stress and Independence From the Left Ventricular End-diastolic Volume
Zależność ESPVR od objętości końcoworozkurczowej zanikała i/lub była istotnie mniejsza, gdy braliśmy pod uwagę ΔESPVR. Korelacje Pearsona i istotności dla osób zdrowych i pacjentów z grupy stresowej przedstawiono w tabeli 4. W konsekwencji ΔESPVR, zamiast spoczynkowej lub szczytowej wartości ESPVR, wykazuje niewielką wrażliwość na warunki obciążenia, ale również niewielką zależność od wielkości komory.12,19,22 ΔESPVR jest najsilniej związana ze szczytową odpowiedzią hemodynamiczną i wysiłkową funkcją skurczową, z których obie są głównymi klinicznymi wyznacznikami kurczliwości LV i rezerwy kurczliwości.30,31 Dane te podkreślają niezależność wielkości ΔESPVR od spoczynkowej lub szczytowej wartości ESPVR i jej konsekwencje dla oceny porównawczej pacjentów.
Dziesięć lat temu ΔESPVR wprowadzono do laboratorium echa wysiłkowego jako miarę zależnych od częstości akcji serca zmian kurczliwości, związanych lub nie ze stymulacją adrenergiczną.10,12,19 We wszystkich badaniach, przy wszystkich rodzajach obciążeń i w różnych populacjach pacjentów – od niedokrwiennej lub idiopatycznej kardiomiopatii rozstrzeniowej do ciężkiej niedomykalności mitralnej – konsekwentnie stwierdzano bardzo wysoką wykonalność i powtarzalność pomiarów.7,8,12,23
Pomimo że kliniczny i naukowy wpływ echa wysiłkowego opiera się, z wielu ważnych powodów, na zaletach regionalnych zaburzeń kurczliwości w porównaniu z niewrażliwymi globalnymi wskaźnikami funkcji LV, takimi jak LVEF, atrakcyjnie proste podejście ΔESPVR wzbudziło nowe zainteresowanie informacjami obecnymi w całej lewej komorze, które są nieobecne w funkcji regionalnej.15 W przeciwieństwie do LVEF, rezerwa elastancji LV jest niezależna od obciążenia następczego i – jak pokazuje obecne badanie – od wymiarów rozkurczowych LV, i jest bardziej przydatna niż rezerwa frakcji wyrzutowej do stratyfikacji diagnostycznej i prognostycznej, przy różnych stresorach.10-12,19,20
Limitations
Nieinwazyjna ocena ESPVR opiera się na równaniu: ESPVR = (ciśnienie końcowoskurczowe / wskaźnik objętości końcowoskurczowej – V0) i zakłada, że V0 (teoretyczna objętość, gdy nie jest generowane ciśnienie) jest pomijalnie mała w porównaniu z objętością końcowoskurczową. Chen i wsp.32 stwierdzili, że obliczanie ciśnienia końcowoskurczowego na podstawie wartości 0,9 × skurczowe ciśnienie tętnicze ramienia w rozsądny sposób przybliżało ciśnienie końcowoskurczowe mierzone inwazyjnie: współczynnik korelacji między tymi dwiema zmiennymi wynosił 0,75, a linia regresji miała nachylenie 1,01 (P
Wzór stosowany do nieinwazyjnego szacowania ciśnienia końcowoskurczowego (0,9 × skurczowe ciśnienie tętnicze) nie został zatwierdzony podczas wysiłku. W tym względzie pomocne mogą być metody wykorzystujące radialną tonometrię aplanacyjną, ponieważ pozwalają one na nieinwazyjne i dokładne oszacowanie centralnego skurczowego ciśnienia tętniczego w spoczynku i podczas wysiłku, przynajmniej w pozycji leżącej na wznak i przy małej intensywności ćwiczeń.33 Pomiar ciśnienia tętniczego jest prostszy i dokładniejszy podczas echokardiografii obciążeniowej (dipirydamol lub dobutamina), ponieważ nie występują artefakty związane z ruchem.24 Ponadto pomiar objętości jest prostszy podczas farmakologicznej echokardiografii obciążeniowej, gdy pacjent leży na lewym boku, co zapewnia optymalną wizualizację struktur serca, zwłaszcza podczas echokardiografii obciążeniowej z dipirydamolem, ze względu na niskie wartości częstości akcji serca w szczytowym okresie obciążenia. Objętości oceniano za pomocą echokardiografii dwuwymiarowej. Pomiary byłyby dokładniejsze i bardziej powtarzalne przy zastosowaniu echokardiografii trójwymiarowej w czasie rzeczywistym, która z pewnością jest możliwa do wykonania i może być zastosowana do oceny elastyczności LV i tętnic w pracowni echokardiograficznej. Jednak retrospektywnie analizowaliśmy pacjentów badanych ze wskazań klinicznych w laboratoriach echokardiografii obciążeniowej o dużej objętości, a w tym rzeczywistym otoczeniu, w rozpatrywanym przedziale czasowym,26 nie było miejsca na stosowanie złożonych, drogich i wówczas technicznie wymagających technologii, takich jak echokardiografia trójwymiarowa w czasie rzeczywistym. Zmienność pomiarów była niska na poziomie wyjściowym i podczas obciążenia, ale ze względu na projekt badania nie można było ocenić zmienności między kolejnymi akwizycjami, która również jest istotna.
WNIOSKI
Dane te podkreślają niezależność ΔESPVR od wielkości i jej konsekwencje dla oceny porównawczej dużej liczby pacjentów z różnymi chorobami. LVEDV nie wpływa na zmiany ESPVR w warunkach spoczynkowych w prawidłowych lub nieprawidłowych lewych komorach podczas stresu fizycznego lub farmakologicznego.
KONFLIKTY INTERESÓW
Nie zgłoszono.
- –
Począwszy od 2003 roku w pracowni echokardiografii obciążeniowej wprowadzono zależność ciśnienie-objętość poprzez zastosowanie ESPVR przy wzrastającej częstości rytmu serca.
- –
Zależność ΔESPVR jest łatwa do uzyskania podczas rutynowej echokardiografii obciążeniowej i została uznana za niezależny od obciążenia następczego wskaźnik kurczliwości LV.
- –
W kilku recenzowanych artykułach wykazano kliniczną przydatność ΔESPVR w rozpoznawaniu utajonych zaburzeń kurczliwości w pozornie prawidłowych sercach oraz resztkowej rezerwy kurczliwości w idiopatycznej i niedokrwiennej kardiomiopatii rozstrzeniowej.
- –
Stratyfikacja prognostyczna pacjentów była lepsza dzięki ΔESPVR, poza standardową oceną LVEF. Czy ΔESPVR zależy od objętości końcoworozkurczowej, pozostaje niejasne.
Czego dotyczy to badanie?
- –
Badanie to pokazuje niezależność LV ΔESPVR od wielkości LVEDV.
- –
Jest to patofizjologicznie ważna koncepcja, którą przetestowaliśmy dla stresorów wysiłkowych, dobutaminowych i dipirydamolowych we wszystkich populacjach pacjentów (od prawidłowej funkcji LV do kardiomiopatii rozstrzeniowej).
- –
Dzięki tym informacjom mamy solidną patofizjologiczną platformę do badania rezerwy elastancyjnej LV przy wszystkich 3 obciążeniach w różnych populacjach pacjentów.
- –
W przeciwieństwie do LVEF, rezerwa elastancji LV (ΔESPVR) jest niezależna od obciążenia następczego i – jak pokazuje obecne badanie – od wymiarów rozkurczowych LV.
.
Dodaj komentarz