- Co to jest żelazo
- Gdzie znajduje się żelazo
- Historia
- Identyfikacja
- Klasyfikacja, Właściwości i cechy charakterystyczne żelaza
- Właściwości ogólne
- Właściwości fizyczne
- Właściwości chemiczne
- Dane atomowe żelaza (pierwiastek 26)
- Jakie są powszechne zastosowania żelaza
- Does the Element Have Any Toxic Effects
- Interesting Facts
- Cena metalu żelaznego
Co to jest żelazo
Żelazo (wymawiane jako EYE-ren) jest twardym metalem o dużej wartości handlowej, należącym do rodziny metali przejściowych. Oznaczany symbolem chemicznym Fe, jest reaktywny chemicznie z tendencją do łatwej korozji w powietrzu, tworząc czerwonawą warstwę zwaną rdzą, gdy jest wystawiony na działanie wilgotnego powietrza.

Symbol żelaza
Gdzie znajduje się żelazo
Jest czwartym co do obfitości metalem w skorupie ziemskiej, powszechnie związanym z innymi rudami mineralnymi, takimi jak hematyt, takonit i magnetyt, występującymi w rezerwach górniczych Ukrainy, Brazylii, Rosji, Australii i Chin. Jego komercyjna produkcja odbywa się w wielkim piecu przez ogrzewanie rud z koksem i wapieniem .
Historia
Origin of its Name: Nazwa pierwiastka pochodzi od anglosaskiego słowa „iron”.
Kto go odkrył: Nieznany
Kiedy, gdzie i jak został odkryty
Około 3500 r. p.n.e. uważano, że Egipcjanie używali przedmiotów z żelaza. Hetyci z Azji Mniejszej byli znani z wytapiania tego metalu z jego rud w 1500 r. p.n.e. W 1722 roku René Antoine Ferchault de Réaumur, francuski entomolog, opublikował książkę, w której opisał znaczenie różnych stopów żelaza.

Metal żelazny
Identyfikacja |
|||
| Liczba atomowa | 26 | ||
| Liczba CAS | 7439-89-.6 | ||
| Pozycja w układzie okresowym | Grupa | Okres | Blok |
| 8 | 4 | d | |
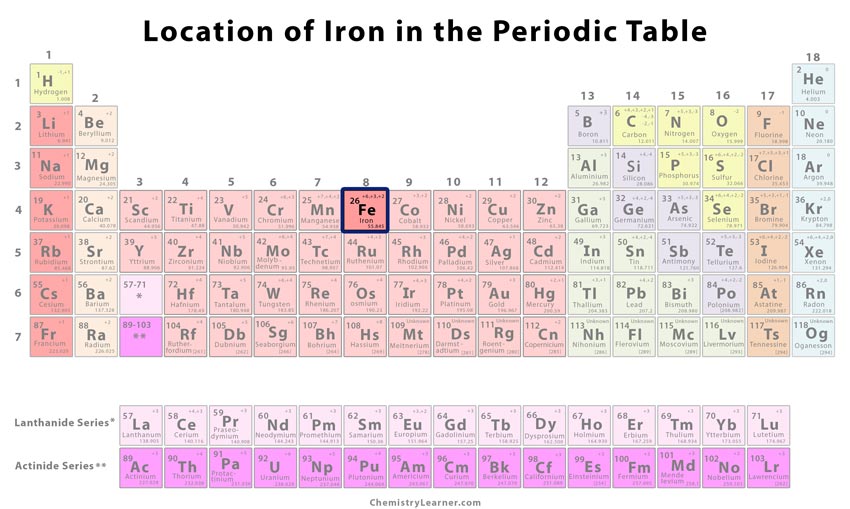
Gdzie znajduje się żelazo w układzie okresowym
Klasyfikacja, Właściwości i cechy charakterystyczne żelaza
Właściwości ogólne |
||
| Relatywna masa atomowa | 55.845 | |
| Masa atomowa/waga | 55.845 atomowych jednostek masy | |
| Masa molowa/waga cząsteczkowa | 55.845 g/mol | |
| Liczba masowa | 56 | |
Właściwości fizyczne |
||
| Kolor/wygląd fizyczny | Srebrnoszary | |
| Punkt topnienia/punkt zamarzania | 1538°C (2800°F) | |
| Punkt wrzenia | 2861°C (5182°F) | |
| Gęstość | 7.87 g/cm3 | |
| Stan normalny/naturalny w temperaturze pokojowej (ciało stałe/ciecz/gaz) | Stan stały | |
| Równoległość | Tak | |
| Odpuszczalność | Tak | |
| Twardość | 4-.5 Mohs | |
| Ciepło właściwe | 0.444 J g-1 oC | |
| Przewodność cieplna | 80.4 Wm-1K-1 | |
Właściwości chemiczne |
||
| Palność | Niepalny | |
| Stany utlenienia (liczby) | 6, 3, 2, 0,-2 | |
Dane atomowe żelaza (pierwiastek 26)
| Konfiguracja elektronowa (konfiguracja gazu szlachetnego) | 3d64s2 | ||||||
| Struktura atomu | |||||||
| -. Liczba Elektronów | 26 | ||||||
| – Liczba Neutronów | 30 | ||||||
| – Liczba Protonów | 26 | ||||||
| Radius of atom | |||||||
| – Atomic Radius | 2.04 Å | ||||||
| – Promień kowalencyjny | 1.24 Å | ||||||
| Energia jonizacji
(kJmol-.1) |
1st | 2nd | 3rd | 4th | 5th | 6th | 7th |
| 762.466 | 1561.876 | 2957.469 | 5287.4 | 7236 | 9561.7 | 12058.74 | |
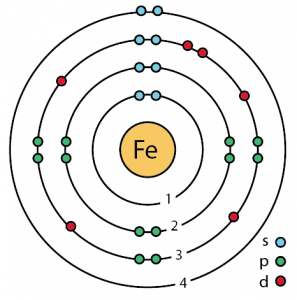
Struktura atomowa żelaza (model Bohra)
Jakie są powszechne zastosowania żelaza
- Żelazo jest stosowane w produkcji różnych rodzajów stali poprzez tworzenie stopów z innymi pierwiastkami, takimi jak węgiel, nikiel, chrom i wolfram do produkcji urządzeń tnących, łańcuchów rowerowych, luf karabinów, wież transmisyjnych, dźwigarów mostowych i betonu zbrojonego.
- Stal bezołowiowa zawierająca wysoki procent żelaza wraz z innymi metalami ma ogromną wytrzymałość i lepszą funkcję, która jest przydatna w produkcji narzędzi chirurgicznych, spinaczy do papieru, sztućców, łożysk kulkowych i biżuterii.
- Inna forma Fe zwana kutym żelazem otrzymywana przez wytapianie jest używana do produkcji narzędzi stolarskich, haków do podnoszenia, łańcuchów, ogrodzeń i bram.
- Wypełnienia żelazne mają zastosowanie w eksperymentach naukowych dotyczących elektromagnetyzmu w celu oceny siły magnesów, jak również w metalurgii siłowej, sztuce, fajerwerkach i piaskowaniu.
- Fe działa jako skuteczny katalizator w niektórych przemysłowych procesach chemicznych, takich jak proces Habera i Fischer-Tropsch.

Iron Bar
Does the Element Have Any Toxic Effects
Accidental ingestion of Fe has been associated with vomiting, diarrhea, and other gastrointestinal issues, a common type of metal poisoning. Długotrwałe gromadzenie się w organizmie może powodować problemy z oddychaniem i zaburzenia serca. Wdychanie pyłu metalowego lub oparów może spowodować poważną reakcję płucną .
Interesting Facts
- Uważa się, że meteoryty mają wysoką zawartość żelaza .
- Żelazo było używane jako metal magnetyczny przez starożytnych nawigatorów w postaci kamieni do tworzenia kompasów .
- W przeciętnym ludzkim ciele obecne są 4 gramy Fe, związane z hemoglobiną, która z kolei pomaga w przenoszeniu tlenu do płuc .
-

Proszek żelaza
Cena metalu żelaznego
Koszt czystego żelaza może wahać się od 0,24 USD do 0,30 USD za funt.
- http://www.rsc.org/periodic-table/element/26/iron
- https://education.jlab.org/itselemental/ele026.html
- https://www.chemicool.com/elements/iron.html
- https://www.radiochemistry.org/periodictable/elements/26.html
- https://www.thoughtco.com/iron-facts-606548
- https://www.tedpella.com/company_html/hardness.htm
- https://www.tedpella.com/company_html/hardness.htm
- http://www2.ucdsb.on.ca/tiss/stretton/database/specific_heat_capacity_table.html
- https://www.angelo.edu/faculty/kboudrea/demos/burning_iron/burning_iron.htm
- https://extrudesign.com/wrought-iron-properties-applications/
- http://www.iron-filing.com/
- https://www.clinicaladvisor.com/labmed/toxicity-associated-with-iron/article/614895/
- https://www.ncbi.nlm.nih.gov/pubmed/1592301
Dodaj komentarz