- Czym są kortykoidy?
- Kortykoidy i kortyzol
- Typy
- Choroby, które można leczyć kortykosteroidami
- Wchłanianie ogólnoustrojowe
- Działania niepożądane
- Skórne działania niepożądane
- Działania niepożądane dotyczące oczu
- Skutki metaboliczne
- Działanie na układ sercowo-naczyniowy
- Wpływ na układ mięśniowo-szkieletowy
- Działania niepożądane ze strony ośrodkowego układu nerwowego
- Efekty immunologiczne
- Inne działania niepożądane
- Opieka i zagrożenia związane ze stosowaniem kortykosteroidów
- Referencje
Czym są kortykoidy?
Glukokortykoidy, zwane również kortykosteroidami lub kortykosteroidami, są silnymi lekami pochodzącymi z hormonu kortyzolu, który jest wytwarzany przez nadnercza.
Kortykosteroidy są często stosowane w ramach leczenia chorób o podłożu zapalnym, alergicznym, immunologicznym, a nawet przeciwko niektórym rodzajom nowotworów.
Pomimo że są bardzo skutecznymi lekami przeciwko kilku poważnym chorobom, kortykosteroidy mają jedną poważną wadę: bardzo obszerny profil działań niepożądanych, niektóre z nich poważne, inne estetycznie niepożądane.
Przedłużone stosowanie kortykosteroidów prowadzi do przyrostu masy ciała, może powodować rozstępy, trądzik, osłabienie kości, zwiększenie ryzyka infekcji itp.
W tym artykule zajmiemy się wskazaniami i działaniami niepożądanymi kortykosteroidów, ze szczególnym uwzględnieniem prednizonu i prednizolonu, najczęściej stosowanych leków tej klasy.
Jeśli szukasz uproszczonej ulotki dołączonej do opakowania prednizonu, zapoznaj się z poniższym artykułem: PREDNISONE – What It’s For, Doses and Care
W celu uzyskania informacji na temat stosowania glikokortykosteroidów w badaniu COVID-19, należy zapoznać się z następującymi artykułami:
- DEXAMETHASONE – BULA DLA PACJENTÓW.
- INFORMACJE O COVID-19.
Kortykoidy i kortyzol
Glukokortykoidy są hormonami steroidowymi, nieanabolicznymi i nieseksualnymi, wytwarzanymi przez korę nadnerczy. Hormonem naturalnie produkowanym przez nasz organizm jest kortyzol.
Normalny poziom kortyzolu jest niezbędny dla naszego zdrowia, ponieważ hormon ten ma działanie na metabolizm glukozy, funkcje metaboliczne organizmu, gojenie, układ odpornościowy, funkcję serca, kontrolę wzrostu i wiele innych podstawowych działań naszego ciała.
Kortyzol jest hormonem stresu, jak jego produkcja wzrasta za każdym razem, gdy nasze ciało jest w stresie fizycznym, jak w przypadku urazu, infekcji lub operacji. Kortyzol zwiększa dostępność glukozy i energii, podnosi ciśnienie krwi, zwiększa napięcie serca i przygotowuje organizm do cierpienia i walki z urazami.
Typy
Glukokortykoidy stosowane w praktyce medycznej są syntetycznymi, laboratoryjnie wytwarzanymi wersjami naturalnego hormonu kortyzolu.
Istnieje kilka syntetycznych preparatów kortykosteroidów, najczęściej stosowane to prednizon, prednizolon, hydrokortyzon, deksametazon, metyloprednizolon i beklometazon (droga wziewna).
Wszystkie syntetyczne kortykosteroidy są silniejsze niż naturalny kortyzol, z wyjątkiem hydrokortyzonu, który ma podobną siłę działania.
Siła działania każdego rodzaju kortykoidu w stosunku do kortyzolu:
- Hydrokortyzon → podobna siła działania do kortyzolu.
- Deflazacort → 3 razy silniejszy od kortyzolu.
- Prednizolon → 4-5 razy silniejszy od kortyzolu.
- Prednizon → 4-5 razy silniejszy od kortyzolu.
- Triamcynolon → 5 razy silniejszy od kortyzolu.
- Metyloprednizolon → 5-7,5 razy silniejszy od kortyzolu.
- Betametazon → 25-30 razy silniejszy od kortyzolu.
- Deksametazon → 25-30 razy silniejszy od kortyzolu.
- Beclometazon (wziewny) → 8 puf 4 razy na dobę jest równoważny 14 mg doustnego prednizonu na dobę.
60 mg prednizonu ma takie samo działanie jak 2 mg deksametazonu lub 300 mg naturalnego kortyzolu. Ze względu na tę większą siłę działania syntetycznych kortykosteroidów, jesteśmy w stanie podawać pacjentom dawki znacznie przekraczające fizjologiczny poziom kortyzolu, co jest niezbędne w leczeniu niektórych chorób.
Choroby, które można leczyć kortykosteroidami
Prednizon i kortykosteroidy w ogóle są lekami, które mogą modulować procesy zapalne i immunologiczne w naszym organizmie, co czyni je niezwykle przydatnymi w wielu chorobach. Każda choroba o podłożu alergicznym, zapalnym lub autoimmunologicznym może być leczona którymś z tych kortykoidów (przeczytaj też: CO TO JEST CHOROBA AUTOIMUNOLOGICZNA?).
Aby uzyskać wyobrażenie o znaczeniu kortykoidów w praktyce medycznej, możemy przytoczyć następujące choroby jako wskazania do ich podawania:
- Astma.
- Stwardnienie rozsiane.
- POChP.
- Alergie, zwłaszcza anafilaksja.
- Autoimmunologiczne zapalenie wątroby.
- Opryszczka zwykła.
- Toczeń.
- Reumatoidalne zapalenie stawów.
- Białaczka.
- Chłoniak.
- Idiopatyczna plamica małopłytkowa (ITP).
- Szpiczak mnogi.
- Obrzęk mózgu.
- Porażenie twarzowe Bella.
- Podagra.
- Sarkoidoza.
- Alergiczny nieżyt nosa.
- Vitiligo.
- Łuszczyca.
- Ziarniniakowatość Wegenera.
- Zapalne choroby jelit.
- Miastenia Gravis.
- Choroby naczyń.
- Choroba Addisona (niedoczynność kory nadnerczy).
- Kłębuszkowe zapalenie nerek.
- Choroby skóry pochodzenia zapalnego lub autoimmunologicznego.
- Zespół Sjögrena.
- Przeszczepianie narządów.
- Pokrzywka.
Dzienne dawki równoważne 5-10 mg prednizonu nazywane są dawkami fizjologicznymi, ponieważ są one zgodne z naturalną dzienną produkcją kortyzolu. W tych dawkach syntetyczne kortykosteroidy wykazują jedynie działanie przeciwzapalne.
W normalnych sytuacjach wydzielanie kortyzolu przez nadnercza wykazuje cykl okołodobowy, czyli ulega zmianom w zależności od pory dnia. W pierwszych godzinach porannych jego wydzielanie jest bardzo wysokie, zmniejszając się do maksimum około godziny 23.00. Dlatego wybieramy podawanie kortykoidów w godzinach porannych, aby spróbować symulować fizjologiczne wydzielanie, do którego organizm jest przyzwyczajony, co zmniejsza częstość występowania skutków ubocznych.
W miarę zwiększania dawki prednizon, jak i każdy inny glikokortykoid, zaczyna wykazywać działanie immunosupresyjne, co uzasadnia jego stosowanie w chorobach autoimmunologicznych i przeszczepach narządów.
W chorobach autoimmunologicznych i kłębuszkowym zapaleniu nerek możemy stosować do 80 mg prednizonu na dobę. W ciężkich przypadkach stosujemy postępowanie zwane terapią pulsacyjną, która polega na dożylnym podawaniu do 1000 mg metyloprednizolonu przez 3 kolejne dni. Ta terapia pulsacyjna może być stosowana w ciężkim zapaleniu naczyń, w przypadkach odrzucenia przeszczepionych narządów oraz w leczeniu ciężkich i zdekompensowanych chorób autoimmunologicznych, jak występuje w niektórych przypadkach tocznia, na przykład.
Kortykosteroidy mogą być podawane różnymi drogami. Na przykład, kortykosteroidy ogólnoustrojowe to te przyjmowane doustnie lub dożylnie. W astmie bardzo powszechne jest podawanie wziewnych glikokortykosteroidów. W zapaleniu błony śluzowej nosa i zatok preferowana jest droga donosowa. W chorobach skóry kortykoidy stosuje się miejscowo, tzn. w kremach lub maściach. Kortykoidy mogą być dostępne w postaci kropli do oczu i roztworów do podawania do uszu. W zapaleniu stawów droga podania może być wewnątrzstawowa (infiltracja).
Wchłanianie ogólnoustrojowe
Ogromna większość działań niepożądanych występuje u pacjentów przyjmujących długotrwale kortykosteroidy doustne lub dożylne w dużych dawkach. Nie oznacza to jednak, że inne formy podawania kortykosteroidów są wolne od działań niepożądanych.
Kortykosteroidy wziewne, szeroko stosowane w leczeniu astmy, mogą mieć istotne wchłanianie ogólnoustrojowe, chociaż jest ono znacznie mniejsze niż to, które występuje w przypadku kortykosteroidów podawanych doustnie. Wiadomo na przykład, że flutikazon podawany wziewnie hamuje wytwarzanie kortyzolu przez nadnercza i może powodować ogólnoustrojowe działania niepożądane, jeśli jest stosowany nieprzerwanie przez kilka miesięcy, zwłaszcza u dzieci. Inne formy kortykosteroidów wziewnych wydają się mieć mniejsze wchłanianie ogólnoustrojowe.
Wstrzyknięcia deksametazonu śródstawowe mogą powodować zespół Cushinga (wyjaśniam, na czym polega ta zmiana później).
Nawet kortykosteroidy w maści lub kremie mogą być wchłaniane do organizmu w stopniu wystarczającym do wywołania działań niepożądanych, jeśli są stosowane przez dłuższy czas. Wchłanianie kortykosteroidów przez skórę różni się w zależności od wielu czynników. Na przykład, obszary takie jak fałdy skórne, skóra głowy i czoło są bardziej narażone na wchłanianie. U dzieci i w obszarach z zapaleniem lub złuszczaniem skóry ogólnoustrojowe wchłanianie kortykosteroidów jest również większe.
Ogólnie rzecz biorąc, nie ma postaci kortykosteroidu, która jest wolna od działań niepożądanych. Niezależnie od drogi podania, im dłuższy czas leczenia i stosowana dawka, tym większe ryzyko wystąpienia działań niepożądanych.
Działania niepożądane
Kortykosteroidy, choć są lekami niezwykle przydatnymi w wielu poważnych chorobach, mają, zwłaszcza przy długotrwałym stosowaniu, ogromną listę niepożądanych działań ubocznych, począwszy od problemów kosmetycznych, a skończywszy na poważnych zakażeniach spowodowanych zahamowaniem układu odpornościowego.
Działania niepożądane są ściśle związane z dawką i czasem stosowania. Nie jest prawdopodobne, aby sporadyczne i krótkotrwałe stosowanie prowadziło do działań niepożądanych, które zostaną opisane poniżej. Nie ma obaw przed przepisaniem kortykoidów tylko na jeden tydzień, nawet jeśli są w dużych dawkach. Zastosowanie będzie wskazany w każdym przypadku, gdy lekarz ocenia, że choroba, która ma być leczona jest bardziej poważne niż potencjalnych działań niepożądanych.
Po przeczytaniu tego artykułu może być pod wrażeniem, że prednizon i podobne leki są straszne leki. Należy pamiętać, że długotrwałe stosowanie dużych dawek jest zwykle wskazane tylko w poważnych chorobach, które mogą prowadzić do śmierci lub poważnych ograniczeń.
Skórne działania niepożądane
Estetyczne działania kortykosteroidów są tymi, które najbardziej niepokoją pacjentów, zwłaszcza kobiety. U około połowy osób stosujących prednizon w dawce co najmniej 20 mg na dobę lub równoważną dawkę innego kortykosteroidu przez trzy lub więcej miesięcy wystąpią estetyczne działania niepożądane.
Najczęstsze z nich to związane z kortykosteroidami wybroczyny i plamica. Zmiany te to niewielkie wylewy, które pojawiają się pod skórą, zwykle w miejscach narażonych na działanie promieni słonecznych, takich jak dłonie i przedramiona. Innym częstym działaniem niepożądanym jest cieńsza i bardziej delikatna skóra.
Purpurowe pasemka zlokalizowane w okolicy brzucha, łysienie, porost włosów u kobiet i trądzik również często występują u osób przewlekle stosujących doustne kortykosteroidy.
Ryzyko wystąpienia nowotworów skóry typu nonmelanoma wydaje się być wyższe u osób przyjmujących kortykosteroidy przez dłuższy czas.
Pacjenci, którzy przyjmują kortykosteroidy w kremach i maściach przez długi czas, mogą również doświadczać niepożądanych skutków na skórze, takich jak atrofia, rozstępy, teleangiektazje i purpurowe plamy. Zwiększone ryzyko zakażeń grzybiczych skóry występuje również przy długotrwałym leczeniu.
Typowym objawem toksyczności kortykosteroidów jest rozwój wyglądu „cushingoidalnego”, który charakteryzuje się zaokrągloną twarzą (zwaną twarzą księżycowatą), nagromadzeniem tłuszczu w tylnej części szyi i pleców (zwanym garbem lub gibą bawolą) oraz nierównomiernym rozmieszczeniem tkanki tłuszczowej, z przewagą w okolicy brzucha i tułowia.
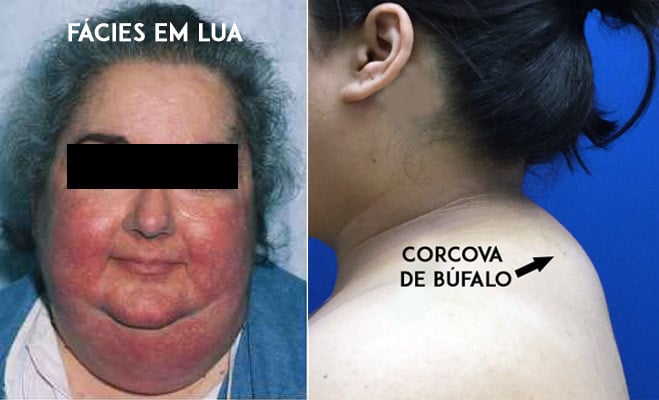
Ten zespół działań niepożądanych, zwany zespołem Cushinga, jest jednym z najbardziej uciążliwych, ponieważ znacznie zmienia wygląd pacjenta, zwłaszcza u osób, które wcześniej były szczupłe.
Zespół Cushinga pojawia się zwykle w ciągu pierwszych dwóch miesięcy leczenia kortykosteroidami w dawkach powyżej 20 mg na dobę. Jednak u niektórych pacjentów dawki powyżej 10 mg na dobę są już wystarczające do wywołania tej zmiany.
Działania niepożądane dotyczące oczu
Przerwane stosowanie kortykosteroidów o działaniu ogólnym, zwykle przez ponad 1 rok z dawkami większymi niż równowartość 10 mg prednizonu na dobę, może prowadzić do zmian okulistycznych, takich jak zaćma i jaskra. Zarówno kortykosteroidy stosowane doustnie, donosowo (aerozol do nosa w przypadku astmy lub zapalenia oskrzeli), jak i w postaci kropli do oczu mogą powodować obie choroby.
Pacjenci, którzy przewlekle przyjmują kortykosteroidy, powinni być okresowo oceniani przez okulistę w celu wykrycia wczesnych objawów zaćmy lub jaskry.
Skutki metaboliczne
Po dawce 5 mg na dobę występuje wyraźna tendencja do przyrostu masy ciała i gromadzenia się tłuszczu w okolicy tułowia i brzucha. Im wyższa dawka kortykoidu, tym większy przyrost masy ciała.
Oprócz odkładania się tłuszczu, przewlekła kortykoterapia prowadzi również do zmian w metabolizmie glukozy, a nawet może być przyczyną cukrzycy. Ryzyko to jest większe u osób, które już przed rozpoczęciem kortykoterapii mają nieznacznie zmienione wartości glukozy. Chociaż cukrzyca jest odwracalna w większości przypadków po odstawieniu leku, niektórzy pacjenci pozostają cukrzykami przez całe życie.
Dzienne dawki prednizonu powyżej 10 mg przez ponad 3 miesiące mogą również powodować zmiany w stężeniu cholesterolu, a mianowicie podwyższenie stężenia cholesterolu LDL (złego cholesterolu) i trójglicerydów oraz obniżenie stężenia cholesterolu HDL (dobrego cholesterolu).
Działanie na układ sercowo-naczyniowy
Przy długotrwałym stosowaniu kortykosteroidów zwykle zwiększa się częstość występowania różnych chorób układu sercowo-naczyniowego. Możemy przytoczyć zwiększone występowanie nadciśnienia tętniczego, zawału serca, niewydolności serca i udaru mózgu.
Ryzyko wystąpienia chorób układu krążenia zależy od dawki i długości leczenia. Pacjenci, u których rozwija się zespół Cushinga, zwykle mają najwyższy wskaźnik miażdżycy i najwyższe ryzyko problemów kardiologicznych.
Małe dawki kortykosteroidów przez krótki czas nie wydają się zwiększać ryzyka sercowo-naczyniowego w żaden istotny sposób.
Wpływ na układ mięśniowo-szkieletowy
Przewlekłe stosowanie glikokortykoidów jest związane z kilkoma zmianami w układzie mięśniowo-szkieletowym. Najczęstszą z nich jest osteoporoza. W tym przypadku nawet małe dawki, takie jak 2,5 mg lub 5 mg na dobę, stosowane przewlekle, mogą przyspieszać utratę masy kostnej.
Przedłużona kortykoterapia jest również odpowiedzialna za zwiększoną częstość występowania martwicy kości, uszkodzenia mięśni (miopatii), złamań kości i zaburzeń wzrostu, gdy jest stosowana u dzieci.
Działania niepożądane ze strony ośrodkowego układu nerwowego
Stosowanie kortykoidów, na początku, może powodować dobre samopoczucie i euforię. Jednak w dłuższej perspektywie wiąże się to z częstszym występowaniem schorzeń psychiatrycznych, takich jak psychozy i depresja, a także bezsenność i zaburzenia pamięci.
Efekty immunologiczne
Odporność wywołana kortykoterapią jest efektem pożądanym w przypadku chorób autoimmunologicznych, ale może też stanowić duży problem, gdyż ułatwia występowanie zakażeń. Trzeba wiedzieć, jak dobrze zrównoważyć ryzyko z korzyściami.
Ryzyko infekcji powstaje u osób przyjmujących równoważnik 10 mg dziennie lub więcej prednizonu przez kilka dni. Ryzyko to staje się bardzo duże przy dawkach powyżej 40 mg na dobę lub w przypadku uzyskania dawki kumulacyjnej 700 mg prednizonu w ciągu całego leczenia.
Oprócz ułatwiania zakażenia, kortykosteroidy hamują również wystąpienie gorączki, utrudniając rozpoznanie toczącego się procesu zakaźnego.
Pacjenci poddawani dużym dawkom kortykosteroidów powinni unikać szczepionek złożonych z żywych wirusów, ze względu na ryzyko rozwoju zakażeń szczepionkowych. Można podawać szczepionki z zabitymi wirusami, jednak kortykoterapia może również zapobiegać tworzeniu się przeciwciał, co sprawia, że immunizacja jest mało skuteczna. Większe dawki są często wymagane do skutecznej immunizacji.
Kandydoza jamy ustnej i kandydoza pochwy są bardzo częstymi zakażeniami u pacjentów przewlekle stosujących glikokortykoidy.
Inne działania niepożądane
Lista możliwych działań niepożądanych kortykosteroidów jest bardzo obszerna. Oprócz tych już wymienionych, inne stosunkowo częste działania niepożądane to zatrzymanie płynów, zmiany miesiączkowania, zapalenie błony śluzowej żołądka, choroba wrzodowa, stłuszczenie wątroby, zapalenie trzustki i niepłodność.
Opieka i zagrożenia związane ze stosowaniem kortykosteroidów
Długotrwała kortykoterapia wymaga pewnej ostrożności, zwłaszcza podczas odstawiania leku.
Długotrwałe stosowanie prednizonu lub podobnych leków hamuje naturalne wytwarzanie kortyzolu przez nadnercza. Ponieważ okres półtrwania syntetycznych glikokortykosteroidów wynosi zaledwie kilka godzin, nagłe odstawienie leku powoduje, że po 2-3 dniach poziom kortyzolu jest bliski zeru. Kiedy nadnercze jest hamowane przez długi czas przez podawanie egzogennych kortykosteroidów, potrzeba czasu zanim powróci do naturalnego wytwarzania kortyzolu.
Ogólnie, zabiegi, które trwają krócej niż 3 tygodnie zazwyczaj nie powodują poważnych skutków ubocznych lub spowodować długotrwałe hamowanie nadnerczy.
Jako że kortyzol jest hormonem niezbędnym do życia, pacjent, który gwałtownie odstawia syntetyczne kortykosteroidy, wchodzi w stan zwany niewydolnością kory nadnerczy i może przejść do wstrząsu krążeniowego, śpiączki i śmierci, jeśli nie zostanie szybko zareagowany.
Dlatego odstawienie kortykosteroidów po długotrwałym stosowaniu powinno zawsze odbywać się powoli i stopniowo. Leczenia nigdy nie należy przerywać bez wiedzy lekarza.
Referencje
- Systemowa terapia kortykosteroidami – działania niepożądane i ich postępowanie –
British Journal of Ophthalmology. - Review: Long-term side effects of glucocorticoids – Journal Expert Opinion on Drug Safety.
- Glukokortykoidy – Huntington’s Outreach Project for Education, w Stanford.
- Profilaktyka i leczenie działań niepożądanych glikokortykoidów systemowych – International journal of dermatology.
- Pharmacologic use of glucocorticoids – UpToDate.
- Główne działania niepożądane glikokortykoidów systemowych – UpToDate.
- Działania niepożądane kortykosteroidów – StatPearls.
Dodaj komentarz