Le cause dell’anisocoria sono diverse e varie. Tradizionalmente, l’anisocoria fisiologica mostra un’asimmetria uguale in condizioni di luce e di buio. Il seguente diagramma di flusso per dedurre la causa specifica. Vedere il diagramma qui sotto.
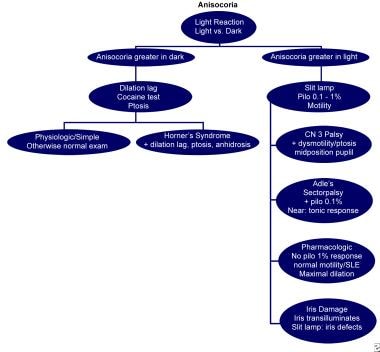 Flowchart to assist in the diagnosis of anisocoria (modificato con il permesso di Thompson e Pilley)
Flowchart to assist in the diagnosis of anisocoria (modificato con il permesso di Thompson e Pilley) Per discussioni specifiche di molti di questi argomenti, vedere gli articoli Oculomotor Nerve Palsy e Horner Syndrome.
Sindrome di Horner
Due condizioni producono comunemente pupille normalmente reattive con anisocoria uguale o maggiore al buio: Sindrome di Horner e anisocoria fisiologica. Nella letteratura di lingua inglese, la sindrome di Horner si riferisce alla paresi simpatica che colpisce l’occhio (conosciuta anche come paresi oculosimpatica, sindrome di Claude Bernard-Horner). Le caratteristiche includono ptosi, miosi e anidrosi; tuttavia, la presentazione esatta varia con il sito della lesione. Le cause variano dal pericolo di vita a condizioni benigne.
La via simpatica inizia nell’ipotalamo, viaggia lungo il tronco cerebrale (dove è spesso interrotta nel midollo laterale), attraverso il midollo spinale cervicale al livello del centro ciliospinale di Budge-Waller a C8-T1, poi sopra l’apice del polmone, infine sale con l’arteria carotide nel seno cavernoso ai dilatatori della pupilla e al muscolo Muller della palpebra. Le fibre sudomotorie che riforniscono il viso escono sulla carotide esterna e i suoi rami. La via nervosa simpatica ha 3 divisioni: di primo ordine (dall’ipotalamo a C8-T1), di secondo ordine (da C8-T1 ai gangli cervicali superiori) e di terzo ordine (dai gangli cervicali superiori ai dilatatori della pupilla e alla palpebra).
La ptosi misura tipicamente 1-2 mm; la miosi misura spesso meno di 2 mm ed è massima al buio. Le fibre simpatiche servono a dilatare la pupilla in condizioni di buio o in risposta alla stimolazione psicosensoriale (cioè, startle o dolore).
Il ritardo di dilatazione si riferisce alla dilatazione rallentata della pupilla colpita in risposta al buio. Può essere valutato osservando le pupille attraverso diversi cicli di stimolazione di luce e buio.
L’anisocoria stessa è asintomatica, e la ptosi minima spesso passa inosservata. Le caratteristiche associate spesso richiedono attenzione medica, o la condizione può essere scoperta incidentalmente da un osservatore.
I test farmacologici della sindrome di Horner sono utili per la conferma della diagnosi e per aiutare nella localizzazione. L’applicazione di una soluzione oftalmica di cocaina al 4-10% può determinare se la sindrome di Horner è presente.
Tuttavia, non ne specifica la sede o la causa. La cocaina impedisce la ricaptazione della norepinefrina e dilata una pupilla normale ma non una pupilla simpaticotomica. Dopo l’instillazione di 1-2 gocce di soluzione al 4-10% (dolorosa per diversi minuti), l’anisocoria post-goccia superiore a 0,8 mm è correlata a più di 1000:1 di probabilità che il paziente abbia la sindrome di Horner. Le gocce richiedono circa 30-45 minuti per il massimo effetto, e più di 2 gocce possono essere tossiche per la cornea. Il test risulta anche in uno screening positivo per la cocaina nelle urine per diversi giorni.
Il test con la cocaina può dare risultati equivoci, e può essere difficile da ottenere e conservare in sicurezza come sostanza controllata. L’Apraclonidina 1% o 0,5% è stata proposta come sostituto. Nei pazienti con sindrome di Horner, l’inversione dell’anisocoria di solito si verifica dopo l’instillazione bilaterale di apraclonidina attraverso la debole attività alfa-1 del farmaco che agisce su una pupilla supersensibile denervata. Tuttavia, sono stati riportati risultati falsi negativi in questo contesto.
L’idrossiamfetamina (Paredrine) stimola il rilascio di norepinefrina da un neurone simpatico di terzo ordine intatto.
Se il neurone di terzo ordine è intatto e funzionale, l’idrossiamfetamina dilata la pupilla. Al contrario, se il neurone del terzo ordine è disfunzionale, il farmaco non produrrà questo effetto.
Perché l’idrossiamfetamina dilata la pupilla se i neuroni simpatici oculari del primo o del secondo ordine sono disfunzionali, non è un farmaco di screening utile per rilevare la sindrome di Horner (vedi cocaina e apraclonidina, discussi sopra).
L’idrossiamfetamina aiuta a rispondere alla domanda “Il neurone simpatico del 3° ordine è intatto?”
Il test viene interpretato calcolando la differenza tra il grado di anisocoria prima e dopo il farmaco. Se, dopo l’instillazione di idrossiamfetamina, l’anisocoria aumenta di 1,2 mm o più rispetto a prima della medicazione, la lesione è postgangliare con una probabilità superiore al 90%.
L’idrossiamfetamina può essere ottenuta da farmacie locali o nazionali, tra cui Leiter’s (San Jose, CA; telefono 800-292-6773). Anche se le cause della sindrome di Horner sono variabili, diverse condizioni sono relativamente comuni.
L’apraclonidina 0,5% è più facilmente disponibile della cocaina o dell’idrossiamfetamina. L’apraclonidina viene instillata in entrambi gli occhi e, dopo 30 minuti, la pupilla di Horner dovrebbe essere dilatata (inversione dell’anisocoria).
La sindrome di Horner di primo ordine è spesso causata da un ictus, più comunemente la sindrome midollare laterale di Wallenberg.
La malattia della colonna vertebrale cervicale può causare una sindrome di Horner di primo o di secondo ordine a seconda della fisiopatologia e della localizzazione (per esempio, malattia del disco o malattia intrinseca del midollo come la siringa, il tumore o l’infiammazione).
Le lesioni dell’apice del polmone (per esempio, il tumore di Pancoast) possono produrre una sindrome di Horner di secondo ordine.
La dissezione dell’arteria carotidea spesso produce dolore ed è accompagnato dalla sindrome di Horner in molti pazienti. Vedere le immagini qui sotto.
 Sindrome di Horner secondaria a dissezione carotidea. Si noti che il grado di anisocoria è relativamente lieve alla luce della stanza. Inoltre, vedere l’immagine qui sotto dello stesso paziente.
Sindrome di Horner secondaria a dissezione carotidea. Si noti che il grado di anisocoria è relativamente lieve alla luce della stanza. Inoltre, vedere l’immagine qui sotto dello stesso paziente.  Sindrome di Horner dovuta a dissezione carotidea. Si noti l’aumento del grado di anisocoria in condizioni di oscurità.
Sindrome di Horner dovuta a dissezione carotidea. Si noti l’aumento del grado di anisocoria in condizioni di oscurità. La malattia del seno cavernoso può produrre una sindrome di Horner di terzo ordine, spesso accompagnata da altri sintomi legati alla paralisi dei nervi cranici III, IV, V o VI come la diplopia.
La sindrome di Horner è una componente della cefalea autonoma del trigemino in alcuni casi. Ci può essere cefalea neuralgiforme unilaterale di breve durata con iniezione della congiuntiva e lacrimazione (SUNCT).
Palsia del nervo oculomotore
La paralisi del terzo nervo (nervo oculomotore) che colpisce l’innervazione parasimpatica della pupilla è spesso associata ad una fisiopatologia compressiva (a differenza della paralisi del terzo nervo diabetico o ischemico, che tipicamente risparmia la pupilla, e generalmente produce anisocoria ≤1 mm in un terzo delle paralisi ischemiche del nervo oculomotore che colpisce la pupilla).
La pupilla nella paralisi del terzo nervo è scarsamente reattiva e midriatica rispetto alla pupilla controlaterale, come mostrato sotto; di conseguenza, l’anisocoria è massima alla luce.
 Pupilla tipica nella paralisi del terzo nervo, con midriasi. Si noti l’incapacità di addurre l’occhio destro. Questo paziente ha un meningioma su base cranica che sta comprimendo il terzo nervo destro. A riposo, la ptosi completa è presente nell’occhio destro; tuttavia, si nota l’elevazione delle palpebre con il tentativo di adduzione dell’occhio destro, che è coerente con la rigenerazione aberrante.
Pupilla tipica nella paralisi del terzo nervo, con midriasi. Si noti l’incapacità di addurre l’occhio destro. Questo paziente ha un meningioma su base cranica che sta comprimendo il terzo nervo destro. A riposo, la ptosi completa è presente nell’occhio destro; tuttavia, si nota l’elevazione delle palpebre con il tentativo di adduzione dell’occhio destro, che è coerente con la rigenerazione aberrante. Una pupilla dilatata isolata senza dismotilità oculare o ptosi rappresenta raramente (“mai”) una paralisi del terzo nervo (è importante controllare l’estremo dello sguardo per un sottile disallineamento suggestivo di paralisi parziale del nervo oculomotore). È più probabile che sia legata ad una pupilla tonica, meccanica o farmacologicamente colpita.
La pupilla può contrarsi all’adduzione a causa di una rigenerazione aberrante. Il medico dovrebbe verificare la sincinesia pupillare con il paziente che guarda in lontananza mentre muove l’occhio sospetto in adduzione.
Pupilla farmacologica
La pupilla dilatata farmacologicamente è più grande che nella maggior parte delle altre cause di anisocoria con midriasi (spesso misura inizialmente 8-9 mm).
La pupilla non risponde agli stimoli luminosi, agli stimoli da vicino o alla soluzione di pilocarpina all’1%; la rottura meccanica dell’iride può anche spiegare tali risultati e può essere distinta con l’esame della lampada a fessura.
Il resto dei risultati dell’esame (cioè, motilità, palpebre, fondo, funzione trigeminale) dovrebbe essere normale, tranne l’acuità da vicino (che è normalizzata con l’uso di una lente di lettura plus).
L’instillazione di farmaci simili all’atropina può essere accidentale o intenzionale, e le potenziali fonti di tale esposizione devono essere ricercate (per esempio, vecchi colliri in casa, esposizione a farmaci come gli inalatori, esposizione a piante tossiche come la Datura).
Meccanico
I danni meccanici al muscolo dell’iride stesso derivanti da traumi, interventi chirurgici (es. estrazione della cataratta), sinechie dell’iride (uveite) e sindrome endoteliale iridocorneale possono produrre anisocoria.
La chiusura acuta dell’angolo è una causa importante di disfunzione meccanica dell’iride e scarsa reattività pupillare. Un aumento acuto della pressione intraoculare può far sì che l’iride occluda meccanicamente il reticolo trabecolare (o i canali di drenaggio) nell’angolo della camera anteriore. La presentazione acuta spesso include dolore, edema corneale, aumento della pressione intraoculare e una pupilla in posizione media fissata alla luce. Il glaucoma ad angolo chiuso è più frequente negli iperopi e in alcune razze come gli asiatici e gli inuit. La presentazione può essere confusa con una paralisi aneurismatica del nervo oculomotore a causa del dolore e della pupilla fissa, ma l’edema corneale e la normale motilità con chiusura dell’angolo aiutano a separare queste entità. Il trattamento è diretto all’abbassamento urgente della pressione intraoculare.
L’esame alla lampada, spesso un utile strumento diagnostico, dimostra l’assottigliamento o i difetti dell’iride, o l’evidenza di un’infiammazione precedente o attuale.
Pupilla tonica
Le pupille toniche rispondono poco alla luce ma vivacemente a un obiettivo vicino, e mantengono questa miosi indotta da vicino per un periodo prolungato (tonica). Questa condizione costituisce una delle sindromi di dissociazione da vicino. Altre sindromi da dissociazione da vicino includono le seguenti:
-
Neuropatie autonomiche (es, DM)
-
Danno grave al sistema afferente
-
Rigenerazione aberrante CN3
-
Sindrome del mesencefalo dorsale di Parinaud
-
Pupille di Argyll Robertson
La classica pupilla tonica è la pupilla tonica di Adie. La pupilla tonica di Adie risponde tonicamente alla stimolazione da vicino (la pupilla impiega più tempo a ridilatarsi dopo la fissazione da vicino).
L’esame alla lampada è utile, spesso dimostrando la paralisi del settore dell’iride (solo una parte dell’iride reagisce alla luce), i movimenti vermiformi dell’iride (movimenti dell’iride orientati radialmente o “purse-stringing”), e fornendo un eccellente ingrandimento per osservare la dissociazione dalla luce vicina. La pupilla può essere supersensibile a una soluzione debole (1/8-1/16%) di pilocarpina, che non costringe una pupilla normale.
Anisocoria transitoria: Questa è stata documentata come una caratteristica intermittente in diverse condizioni. Il più delle volte, riflette una condizione benigna e può essere associata all’emicrania, specialmente se non sono presenti altre caratteristiche associate, ma può rappresentare una disfunzione parasimpatica o simpatica transitoria da altre cause.
La ganglionopatia autonoma autoimmune è una causa rara di anisocoria.
Lascia un commento