La combustione di idrocarburi si riferisce alla reazione chimica in cui un idrocarburo reagisce con l’ossigeno per creare anidride carbonica, acqua e calore. Gli idrocarburi sono molecole composte da idrogeno e carbonio. Sono famosi soprattutto per essere il costituente principale dei combustibili fossili, cioè il gas naturale, il petrolio e il carbone. Per questo motivo, le risorse di combustibili fossili sono spesso chiamate risorse di idrocarburi. L’energia si ottiene dai combustibili fossili attraverso la combustione del combustibile. Anche se esistono impurità nei combustibili fossili, la combustione di idrocarburi è il processo principale nella combustione del combustibile fossile. Un esempio di combustione di idrocarburi è illustrato nella Figura 1. Vedi la simulazione in fondo alla pagina per altri esempi.
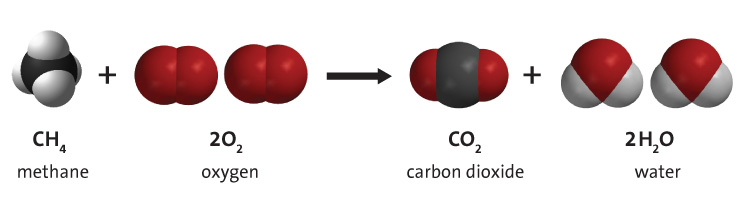
Descrizione
A prescindere dal tipo di idrocarburo, la combustione con l’ossigeno produce 3 prodotti: anidride carbonica, acqua e calore, come mostrato nella reazione generale sottostante. L’energia richiesta per rompere i legami nelle molecole di idrocarburo è sostanzialmente inferiore all’energia rilasciata nella formazione dei legami nelle molecole di CO2 e H2O. Per questo motivo, il processo rilascia una quantità significativa di energia termica (calore). Questa energia termica può essere usata direttamente (forse per riscaldare una casa) o può essere convertita in energia meccanica, usando un motore termico. Tuttavia, questo è soggetto a perdite di efficienza, con conseguenti necessarie significative perdite di energia (come calore di scarto) regolate dalla seconda legge della termodinamica. L’energia meccanica utile risultante sarà molto inferiore all’energia termica iniziale fornita dalla combustione degli idrocarburi.
Equazione generale di reazione:
- si riferisce al numero di atomi di carbonio nell’idrocarburo
- si riferisce al numero di atomi di idrogeno nell’idrocarburo
- si riferisce al numero di atomi di ossigeno richiesti nella reazione di combustione dell’idrocarburo
Combustione di idrocarburi e combustibili fossili
Nota che la CO2 è sempre prodotta nella combustione di idrocarburi; non importa quale tipo di molecola di idrocarburo. Produrre CO2 e H2O è in realtà il modo in cui si ottiene energia utile dai combustibili fossili. Per questo motivo, è importante distinguere tra l’anidride carbonica e altri prodotti “di scarto” che derivano da impurità nel combustibile come i composti di zolfo e azoto. I rifiuti che derivano dalle impurità possono essere eliminati con la giusta tecnologia; il CO2 non può essere eliminato a meno che i combustibili fossili non vengano bruciati (usati) in primo luogo.
Non tutti i combustibili fossili hanno la stessa composizione. Il gas naturale è composto da oltre il 90% di metano (CH4) che è la più piccola molecola di idrocarburo. Il petrolio tende ad essere composto da molecole di medie dimensioni, anche se la composizione varia notevolmente da un grado di greggio all’altro. In generale, più denso è il petrolio, più lunghe sono le catene di carbonio nelle molecole. Infine il carbone contiene le molecole di idrocarburi più grandi e complesse.
Siccome diversi idrocarburi hanno diversi rapporti di idrogeno e carbonio, producono diversi rapporti di acqua e anidride carbonica. In generale, più lunga e complessa è la molecola, maggiore è il rapporto tra carbonio e idrogeno. Per questo motivo, la combustione di quantità uguali di idrocarburi diversi produrrà quantità diverse di anidride carbonica, a seconda del rapporto tra carbonio e idrogeno nelle molecole di ciascuno. Poiché il carbone contiene le molecole di idrocarburi più lunghe e complesse, bruciare il carbone rilascia più CO2 che bruciare la stessa massa di petrolio o gas naturale. Questo cambia anche la densità energetica di ciascuno di questi combustibili.
Emissioni di anidride carbonica
Di seguito un grafico della CO2 emessa dalla produzione di 293,1 kWh (1.000.000 BTU) di energia da vari combustibili idrocarburici.
| Combustibile | kg di emissioni di CO2 |
|---|---|
| Carbone antracite | 104 |
| Carbone bituminoso | 93.5 |
| Carbone di lignite | 97.9 |
| Carbone stopposo | 97.4 |
| Diesel | 73.2 |
| Benzina | 71,5 |
| Propano | 63,2 |
| Gas naturale | 53.2 |
Animazione della combustione
Scegli un combustibile dal menu a discesa per vedere la reazione netta che avviene durante la combustione.
Per ulteriori letture
Per ulteriori informazioni vedi le pagine correlate qui sotto:
- Combustibile fossile
- Energia primaria
- Risorsa idrocarburi
- Carbone
- Petrolio
- Gas naturale
- Una pagina casuale
Lascia un commento