LA REGIONE BUCCALE – UN PERCORSO VANTAGGIOSO PER LA CONSEGNA DEI FARMACI
Le innovazioni nella consegna dei farmaci hanno la promessa di ridurre al minimo gli effetti collaterali dose-dipendenti e massimizzare l’attività biologica, migliorando l’aderenza del paziente.
La somministrazione perorale dei farmaci, la via preferita di somministrazione dei farmaci in termini di esperienza del paziente, ha diversi svantaggi, come il metabolismo epatico di primo passaggio, l’inizio più lungo dell’azione e la degradazione enzimatica dei farmaci nel tratto gastrointestinale (GI). Quando il GI e la degradazione epatica limitano la sicurezza o l’efficacia di un farmaco, le iniezioni invasive sono spesso l’unica modalità possibile di somministrazione – con la potenziale conseguenza di una minore aderenza del paziente.

La somministrazione orale può ottenere effetti locali e sistemici ed è attraente in quanto supera le carenze della somministrazione perorale. Infatti, le sostanze assorbite attraverso la mucosa buccale bypassano la degradazione enzimatica gastrointestinale e l’effetto di primo passaggio epatico. La somministrazione buccale rappresenta inoltre una migliore alternativa alle iniezioni o alle compresse per quei pazienti che hanno difficoltà a deglutire.
Che cos’è il sito buccale?
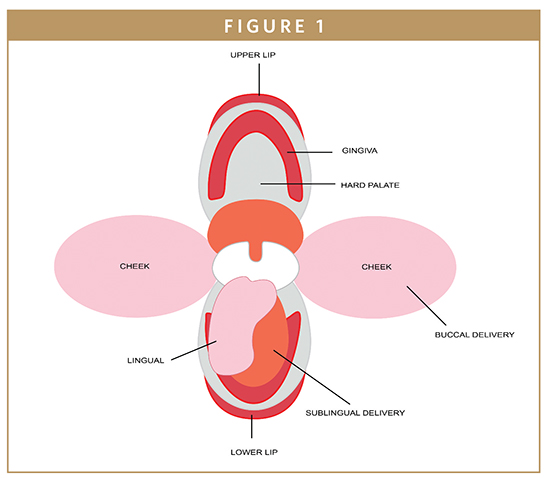
L’area buccale è il rivestimento interno della guancia e del labbro, che rappresenta circa un terzo della superficie della cavità orale (Figura 1).1 La mucosa buccale consiste in uno strato superficiale di epitelio squamoso stratificato collegato al tessuto connettivo sottostante da una lamina basale. Una rete di capillari sanguigni è presente nel tessuto connettivo dove i farmaci che hanno permeato attraverso l’epitelio possono entrare nella circolazione sistemica attraverso la vena giugulare interna.2
L’epitelio buccale agisce come una barriera alla permeazione dei farmaci idrofili, mentre il tessuto connettivo, che è più idrofilo in natura, sembra influenzare il tempo di diffusione dei composti lipofili.3 Il trasporto dei farmaci attraverso la mucosa può essere trans- o paracellulare (Figura 2), con la maggior parte dei farmaci idrofili e delle macromolecole che permeano attraverso la diffusione paracellulare passiva e i composti lipofili e le piccole molecole idrofobiche che passano prevalentemente attraverso il trasporto paracellulare.4 Come tale, la membrana cellulare agisce come la principale barriera di trasporto per i composti idrofili, e gli spazi intercellulari costituiscono la principale barriera alla permeazione dei composti lipofili.

L’importanza della mucoadesione
La mucoadesione è quando due superfici, una delle quali è una membrana mucosa, aderiscono tra loro. È un parametro critico per la somministrazione buccale e i materiali di formulazione con proprietà adesive ottimali devono essere selezionati. La mucoadesione avviene in due fasi – la fase di contatto seguita dalla fase di consolidamento quando si stabiliscono le interazioni adesive. Ci sono probabilmente molteplici meccanismi in gioco che causano l’adesione. È importante che il fallimento dell’adesione si verifichi come risultato della sovraidratazione di una forma di dosaggio, o come risultato del turnover dell’epitelio o del muco. Il tempo di turnover dell’epitelio buccale è stato stimato in 3-8 giorni rispetto a circa 30 giorni per la pelle.4

Vantaggi del sito
Oltre al vantaggio principale della somministrazione sistemica che bypassa la degradazione epatica e intestinale per una maggiore biodisponibilità e minori effetti collaterali, la bocca ha un’area relativamente ampia per l’applicazione del farmaco e una buona accessibilità rispetto al naso, al retto e alla vagina.5 Inoltre, il rapido ricambio cellulare nella mucosa buccale riduce il rischio di danni ai tessuti o di irritazione.6 Mentre la mucosa sublinguale è più permeabile, vascolarizzata e sottile della mucosa buccale, la superficie di questa mucosa è più piccola, costantemente lavata dalla saliva, e il taglio esercitato dalla lingua rende difficile mantenere la forma di dosaggio in contatto con la mucosa sublinguale.7 Per tutte queste ragioni, la mucosa della guancia è un sito preferito all’interno della cavità orale per la somministrazione di sistemi a rilascio controllato che devono aderire per un lungo periodo di tempo.8
Limitazioni del sito
Aumentare il tasso di assorbimento (μg/mm2/s) o la permeabilità del tessuto buccale è spesso necessario per compensare la limitata superficie disponibile. L’uso di potenziatori di permeazione (cioè sostanze che riorganizzano l’epidermide o le strutture epiteliali o aprono le giunzioni strette intercellulari) è molto importante in questo settore. Le macromolecole sono più complesse da far passare attraverso la mucosa a causa della degradazione enzimatica della saliva e della scarsa permeazione attraverso l’epitelio buccale senza un miglioramento della permeazione basato su sostanze chimiche o elettriche.9 L’uso improprio dei potenziatori di permeazione può causare problemi di sicurezza per quanto riguarda l’irritazione locale dei tessuti, ma anche come risultato di un effetto bolo indesiderato che spinge la concentrazione del farmaco nel sangue a livelli che non sono sicuri.
Una strategia alternativa per garantire un maggiore assorbimento di farmaci poco solubili o permeabili nel tessuto è quello di aumentare il tempo di permanenza nella bocca. Come per i potenziatori di permeazione, l’aumento del tempo di permanenza può causare irritazione dei tessuti e disagio al paziente e richiede un’attenta valutazione degli effetti immediati e a lungo termine sull’integrità e la funzionalità dei tessuti. Aumentare il tempo di permanenza nella cavità orale può essere ulteriormente impegnativo in quanto il farmaco può essere rapidamente eliminato a causa dell’azione di lavaggio della saliva. Di conseguenza, possono essere necessarie dosi ripetute e frequenti, a meno che la forma di dosaggio non crei un forte legame con la mucosa assorbente. La ricerca è necessaria per quantificare quanto il lavaggio salivare influenzi l’efficienza della consegna orale transmucosale da diversi sistemi di consegna dei farmaci.
I fattori umani sono importanti da prendere in considerazione quando si sviluppa un prodotto buccale. Dato che la mucosa buccale si estende dagli spazi superiori e inferiori tra le guance, le labbra e le gengive, la posizione precisa in cui il paziente colloca la forma di dosaggio può influenzare l’aderenza e l’assorbimento del farmaco, e queste implicazioni dei fattori umani possono influenzare la variabilità interpaziente. Il modo in cui la forma di dosaggio viene posizionata può causare ulteriori complicazioni quando la forma di dosaggio è progettata per il rilascio unidirezionale e ha un lato adesivo specifico da posizionare contro la guancia interna. Infine, quando e cosa il paziente mangia, beve o fuma può influenzare ulteriormente l’assorbimento del farmaco attraverso la mucosa.
Il rischio di slittamento e la variabilità del paziente a causa della stimolazione della saliva possono essere minimizzati se il farmaco viene somministrato durante la notte, per esempio, quando il paziente non mangia o parla.
Forme di dosaggio buccali
Anche se la mucosa buccale è solo ora ampiamente studiata come una nuova via di somministrazione dei farmaci, il suo potenziale per la somministrazione di farmaci è noto all’umanità da secoli. I nativi americani hanno introdotto il tabacco da masticare ai coloni europei nel 1500, e le foglie di coca sono state masticate 8.000 anni fa dai peruviani. La mucosa buccale è stata presa di mira utilizzando forme di dosaggio convenzionali, come compresse, troches e pastiglie, lavaggi della bocca e spray, con diversi prodotti di questo tipo attualmente sul mercato. La sfida consiste nel mantenere queste forme di dosaggio nel sito di assorbimento, nella precisione del dosaggio (liquidi) e nel disagio (compresse). Le compresse hanno il potenziale di separarsi dalla mucosa, essere inghiottite e poi aderire alla parete dell’esofago causando un pericolo di soffocamento, specialmente per i bambini e gli anziani.
Sistemi più avanzati di consegna dei farmaci includono film, cerotti, compresse bilayer, idrogeli e nastri insieme all’uso di micro- e nano-particelle sono in fase di sviluppo per superare i limiti delle forme di dosaggio convenzionali.
FILM PER LA CONSEGNA BUCCALE – CUREFILM
I film mucoadesivi sono una forma di dosaggio preferita per la somministrazione alla mucosa buccale grazie alla loro flessibilità, comodità, appetibilità e dimensione regolabile. Hanno dimostrato una migliore compliance del paziente rispetto alle compresse adesive.10,11 In contrasto con le formulazioni liquide, in gel e in pomata, i film mucoadesivi rimangono a contatto con la mucosa più a lungo, coprono una superficie maggiore e quindi forniscono un dosaggio più accurato del farmaco.12 Infatti, i film mucoadesivi possono essere progettati attraverso un’attenta selezione del materiale per mantenere un ampio contatto adesivo con la membrana mucosale, prolungando il tempo di ritenzione del sistema di somministrazione per un maggiore assorbimento totale del farmaco. Inoltre, i film mucoadesivi sono adatti per la terapia locale, proteggendo le superfici delle ferite orali dalle infezioni, per esempio.13
Le composizioni dei film sono progettate per ottenere le seguenti proprietà fisiche: forza bioadesiva, resistenza alla trazione, duttilità, flessibilità e disintegrazione estesa. Queste proprietà sono fondamentali per raggiungere il profilo di rilascio del farmaco, l’accettabilità da parte del paziente e la compatibilità con i processi di produzione commerciali. Raggiungere le specifiche target dei film polimerici buccali è altamente dipendente dal tipo e dalla concentrazione dei polimeri selezionati e dalla dose di principi attivi che vengono rilasciati.
Come discusso qui, anche con un film fortemente adesivo, il flusso salivare causerà la dissoluzione di parte del film nella cavità orale e l’ingestione. I film a doppio strato con uno strato di supporto occlusivo sono stati progettati per guidare il rilascio unidirezionale del farmaco e l’assorbimento nella mucosa buccale e possono fornire alte dosi di principio attivo. Mentre tali disegni possono migliorare l’assorbimento buccale, presentano diversi svantaggi. Possono portare all’errore dell’utente nella loro applicazione, lo strato occlusivo può staccarsi e diventare un pericolo di soffocamento e, infine, la complessità della scalabilità di un film a doppio strato fa aumentare i costi di produzione.
Prendendo in considerazione questi vincoli, l’approccio di CURE Pharmaceutical allo sviluppo del film buccale con CUREfilm sfrutta l’inevitabile flusso salivare di un film a strato singolo per creare profili di rilascio del farmaco migliori. Progettiamo i nostri prodotti per combinare l’effetto bolo a rapida insorgenza della somministrazione buccale con il rilascio prolungato della somministrazione gastrointestinale per ottenere un profilo complessivo a rilascio pulsatile o prolungato. Infatti, con la somministrazione buccale, i livelli ematici possono raggiungere il picco rapidamente e un’emivita più breve può significare che l’effetto si esaurisce rapidamente. Inoltre, se si consegnano alte dosi di un farmaco solo per via buccale (ad esempio, oltre 100 mg), la concentrazione locale del tessuto potrebbe essere troppo alta e danneggiare il tessuto. Un approccio a singolo strato è preferibile in quanto minimizza i costi e l’errore dell’utente.
Per creare un CUREfilm buccale, una miscela accuratamente selezionata di polimeri, potenziatori di permeazione e lipidi sono combinati per ottimizzare l’aderenza, la diffusione del farmaco e la permeazione attraverso la mucosa. I lipidi svolgono un ruolo cruciale nella solubilizzazione e nella stabilità degli ingredienti attivi. Aiutano a guidare i composti idrofili attraverso l’epitelio della mucosa e promuovono il trasporto transcellulare dei composti lipofili attraverso l’epitelio per raggiungere i vasi sanguigni. La nano-particolazione del principio attivo può fornire un’ulteriore freccia nella faretra del formulatore per aumentare il tasso di assorbimento.
Per ottenere una sufficiente protezione gastrica e un efficiente rilascio intestinale della porzione di farmaco che viene ingerita, le particelle di farmaco possono essere completamente o parzialmente incapsulate, rivestite entericamente o reticolate a polimeri, come il chitosano, prima della loro incorporazione nella matrice del film. Altre strategie includono la formazione liposomica o micellare, la co-cristallizzazione e l’uso di polimeri gelificanti o rigonfiabili.
Questa doppia strategia può essere molto utile per i farmaci di combinazione con diversi profili metabolici in cui un farmaco è preparato per l’assorbimento buccale (cioè, se ha un alto effetto di primo passaggio), e l’altro è preparato per il rilascio nel GI.
SOMMARIO
L’effettiva progettazione e costruzione di un film orale capace di un’efficace somministrazione terapeutica può essere impegnativa e richiede la creazione di nuove tecnologie. Come risultato di queste innovazioni, i film buccali sono ora una forma di dosaggio commercialmente praticabile che può risolvere molti problemi affrontati dall’industria farmaceutica, dai pazienti e dai loro assistenti. Potranno sostituire le iniezioni quotidiane, come le iniezioni di apomorfina prese dai pazienti che soffrono del morbo di Parkinson. Possono migliorare la biodisponibilità dei farmaci, come i cannabinoidi, abbassando potenzialmente la loro dose e gli effetti collaterali psicoattivi. Quando è necessario un rapido sollievo dei sintomi, possono fornire un effetto in bolo. Sono una comoda alternativa ai liquidi sgradevoli per i bambini e alle pillole difficili da inghiottire per gli anziani.
Dato l’importante bisogno di mercato insoddisfatto che soddisfano, il tasso di adozione dei film orali è stato alto. Infatti, il mercato globale è stato valutato a 2,1 miliardi di dollari nel 2017 e si prevede che si espanderà ad un CAGR del 13% durante il periodo di previsione dal 2018 al 2026.14 Questa crescita commerciale dei film orali, compresi i film buccali, riflette la maggiore attenzione dell’industria farmaceutica sull’innovazione incentrata sul paziente nello sviluppo di nuovi farmaci e sul miglioramento dei vecchi farmaci – dove l’esperienza del paziente guida la progettazione della somministrazione dei farmaci, che a sua volta migliora i risultati per il paziente.
- Curatolo W. Le barriere di permeabilità lipoidale della pelle e del tratto alimentare. Pharm Res. 1987;4(4):271-277.
- Colombo P, Cagnani S, Buttini F, Santi P, et al. Biological In Vitro Models for Absorption by Non-Oral Routes, Reference Module in Chemistry, Molecular Sciences and Chemical Engineering, Elsevier. 2013.
- Kulkarni U, Mahalingam R, Pather SI, Li X, Jasti B. Mucosa buccale suina come modello in vitro: contributo relativo di epitelio e tessuto connettivo come barriere di permeabilità. J Pharm Sci. 2009;98(2):471-483. doi: 10.1002/jps.21436.
- Gandhi RB, Robinson JR. La cavità orale come sito per la somministrazione di farmaci bioadesivi Adv Drug Deliv Rev. 1994;13:43-74.
- Rathbone MJ, Drummond BK, Tucker IG. La cavità orale come sito per la somministrazione sistemica di farmaci Adv Drug Deliv Rev. 1994;13:1-22.
- Squier CA, Wertz PW. Struttura e funzione della mucosa orale e implicazioni per la somministrazione di farmaci M.J. Rathbone (Ed.), Oral Mucosal Drug Delivery, Marcel Dekker, New York. 1996:1-26.
- Madhav NVS, Shakya AK, Shakya P, Singh K. Orotransmucosal drug delivery systems: a review. J Control Release. 2009;140:2-11.
- Madhav NVS, Shakya AK, Shakya P, Singh K. Orotransmucosal drug delivery systems: a review J Control Release. 2009;140:2-11.
- Morales JO, Brayden DJ. Consegna buccale di piccole molecole e biologici: di polimeri mucoadesivi, film e nanoparticelle. Current Opinion Pharmacol. 2017;36:22-28.
- Kraisit P, Limmatvapirat S, Nunthanid J, et al. Preparazione e caratterizzazione di film di miscela idrossipropilmetilcellulosa/polycarbophil mucoadesiva utilizzando un approccio di progettazione di miscela Chem Pharm Bull. 2017;65(3):284-294.
- Giovino C, Ayensu I, Tetteh J, et al. Sviluppo e caratterizzazione di film di chitosano impregnati di nanoparticelle (NPs) PEGb-PLA caricate con insulina: un potenziale approccio per la consegna buccale di macromolecole. Int J Pharm. 2012;428(1-2):143-151.
- Abruzzo A, Bigucci F, Cerchiara T, et al. Film mucoadesivi di chitosano/gelatina per il rilascio buccale di propranololo cloridrato. Carbohydr Polym. 2012;87(1):581-588.
- Tejada G, Lamas MC, Svetaz L, Salomón CJ, Alvarez VA, et al. Effetto della tecnica di incorporazione del farmaco e della combinazione di polimeri sulle prestazioni dei film buccali biopolimerici antifungini. Int J Pharmaceut. 2018;548(1):431-442.
- Transparency Market Research (TMR) report. Oral Thin Films Market – Global Industry Analysis, Size, Share, Growth, Trends, and Forecast, 2018-2026.

Robert Davidson è il CEO di CURE e Chariman del Consiglio di Amministrazione. Prima del suo ruolo alla CURE Pharmaceutical, è stato presidente e amministratore delegato di InnoZen Inc., amministratore delegato di Gel Tech LLC, amministratore delegato di Bio Delivery Technologies Inc. ed è stato membro di diversi consigli di amministrazione. Davidson è stato responsabile dello sviluppo di diverse tecnologie di consegna dei farmaci e delle estensioni commerciali del marchio. Ha un Master Certificate in Applied Project Management della Villanova University, un Master in Public Health dell’American Military University, Virginia e un Master in Health and Wellness della Liberty University, Virginia. Davidson ha anche completato i suoi studi post-laurea presso l’Università di Cambridge con lettera di encomio.

Jessica Rousset è il direttore operativo di CURE. La signora Rousset supervisiona le operazioni e guida la strategia e la crescita aziendale. La signora Rousset è stata in precedenza responsabile dell’innovazione al Children’s Hospital di Los Angeles, dove per dieci anni ha contribuito al lancio di aziende terapeutiche e di dispositivi medici e ha fondato e gestito un acceleratore tecnologico pediatrico nazionale. In precedenza, la signora Rousset ha ricoperto posizioni presso The Scripps Research Institute e GlaxoSmithkline Biologicals in ruoli di laboratorio, ricerca clinica e sviluppo aziendale. Si è formata come ingegnere biochimico all’Institut National des Sciences Appliquées di Lione, Francia.
Lascia un commento