- Che cosa sono i corticoidi?
- Corticoidi e cortisolo
- Tipi
- Malattie che possono essere trattate con i corticosteroidi
- Assorbimento sistemico
- Effetti collaterali
- Effetti collaterali della pelle
- Effetti collaterali sugli occhi
- Effetti metabolici
- Effetti cardiovascolari
- Effetti muscoloscheletrici
- Effetti collaterali del sistema nervoso centrale
- Effetti immunologici
- Altri effetti
- Cura e pericoli dell’uso di corticosteroidi
- Riferimenti
Che cosa sono i corticoidi?
I glucocorticoidi, chiamati anche corticosteroidi o corticosteroidi, sono potenti farmaci derivati dall’ormone cortisolo, che è prodotto dalla ghiandola surrenale.
I corticosteroidi sono spesso utilizzati come parte del trattamento di malattie di origine infiammatoria, allergica, immunitaria e anche contro alcuni tipi di cancro.
Anche se un farmaco molto efficace contro diverse malattie gravi, i corticosteroidi hanno un grande difetto: un profilo molto esteso di effetti collaterali, alcuni dei quali gravi, altri esteticamente indesiderabili.
Se usati in modo prolungato, i corticosteroidi portano all’aumento di peso, possono causare smagliature, causare acne, indebolire le ossa, aumentare il rischio di infezioni, ecc.
In questo articolo ci occuperemo delle indicazioni e degli effetti collaterali dei corticosteroidi, con particolare attenzione al prednisone e al prednisolone, i farmaci più usati di questa classe.
Se stai cercando un foglietto illustrativo semplificato per il prednisone, accedi al seguente articolo: PREDNISONE – A cosa serve, dosi e cura
Per informazioni sull’uso dei corticosteroidi in COVID-19, accedere ai seguenti articoli:
- DEXAMETHASONE – BULA PER PAZIENTI.
- INFORMAZIONI SU COVID-19.
Corticoidi e cortisolo
I glucocorticoidi sono ormoni steroidei, non anabolici e non sessuali, prodotti dalla corteccia della ghiandola surrenale. L’ormone prodotto naturalmente dal nostro corpo è il cortisolo.
I livelli normali di cortisolo sono essenziali per la nostra salute, poiché questo ormone ha un’azione sul metabolismo del glucosio, le funzioni metaboliche del corpo, la guarigione, il sistema immunitario, la funzione cardiaca, il controllo della crescita e molte altre azioni fondamentali del nostro corpo.
Il cortisolo è un ormone dello stress, poiché la sua produzione aumenta ogni volta che il nostro corpo è sotto stress fisico, come in caso di trauma, infezioni o interventi chirurgici. Il cortisolo aumenta la disponibilità di glucosio e di energia, alza la pressione sanguigna, aumenta il tono cardiaco e prepara il corpo a subire e combattere gli insulti.
Tipi
I glucocorticoidi usati nella pratica medica sono versioni sintetiche, prodotte in laboratorio, dell’ormone naturale cortisolo.
Ci sono diverse formulazioni sintetiche di corticosteroidi, le più comunemente usate sono prednisone, prednisolone, idrocortisone, desametasone, metilprednisolone e beclometasone (via inalatoria).
Tutti i corticosteroidi sintetici sono più potenti del cortisolo naturale, tranne l’idrocortisone, che ha una potenza simile.
Potenza di ogni tipo di corticoide rispetto al cortisolo:
- Idrocortisone → potenza simile al cortisolo.
- Deflazacort → 3 volte più potente del cortisolo.
- Prednisolone → 4-5 volte più potente del cortisolo.
- Prednisone → 4-5 volte più potente del cortisolo.
- Triamcinolone → 5 volte più potente del cortisolo.
- Metilprednisolone → 5-7,5 volte più potente del cortisolo.
- Betamethasone → 25-30 volte più potente del cortisolo.
- Il desametasone → 25-30 volte più potente del cortisolo.
- Il beclometasone (inalato) → 8 puf 4 volte al giorno è equivalente a 14 mg di prednisone orale quotidiano.
60 mg di prednisone hanno lo stesso effetto di 2 mg di desametasone o 300 mg di cortisolo naturale. Grazie a questa maggiore potenza dei corticosteroidi sintetici, siamo in grado di somministrare ai pazienti dosi molto superiori ai livelli fisiologici di cortisolo, il che è essenziale per il trattamento di alcune malattie.
Malattie che possono essere trattate con i corticosteroidi
Il prednisone e i corticosteroidi in generale sono farmaci in grado di modulare i processi infiammatori e immunologici nel nostro corpo, rendendoli estremamente utili in una moltitudine di malattie. Qualsiasi malattia di origine allergica, infiammatoria o autoimmune può essere trattata con uno qualsiasi di questi corticoidi (leggi anche: COSA È UNA MALATTIA AUTOIMUNE?).
Per avere un’idea dell’importanza dei corticoidi nella pratica medica, possiamo citare le seguenti malattie come indicazioni per la loro somministrazione:
- Asma.
- Sclerosi multipla.
- BPCO.
- Allergie, specialmente anafilassi.
- Epatite autoimmune.
- Herpes Zoster.
- Lupus.
- Artrite reumatoide.
- Leucemia.
- Linfoma.
- Porpora trombocitopenica idiopatica (ITP).
- Mieloma multiplo.
- Edema cerebrale.
- Paralisi facciale di Bell.
- Gotta.
- Sarcoidosi.
- Rinite allergica.
- Vitiligo.
- Psoriasi.
- Granulomatosi di Wegener.
- Malattia infiammatoria intestinale.
- Miastenia Gravis.
- Vasculitidi.
- Malattia di Addison (insufficienza surrenale).
- Glomerulonefrite.
- Malattie della pelle di origine infiammatoria o autoimmune.
- Sindrome di Sjögren.
- Trapianto di organi.
- Orticaria.
Dosi giornaliere equivalenti a 5-10 mg di prednisone sono chiamate dosi fisiologiche perché sono compatibili con la naturale produzione quotidiana di cortisolo. A queste dosi, i corticosteroidi sintetici presentano solo un effetto antinfiammatorio.
In situazioni normali, la secrezione di cortisolo da parte del surrene presenta un ciclo circadiano, cioè, subisce dei cambiamenti secondo il periodo della giornata. Durante le prime ore del mattino, la sua secrezione è molto alta, riducendosi ad un massimo intorno alle 11 di sera. Pertanto, abbiamo scelto di somministrare i corticoidi durante la mattina per cercare di simulare la secrezione fisiologica a cui il corpo è abituato, riducendo così l’incidenza degli effetti collaterali.
Con l’aumento della dose, il prednisone, o qualsiasi altro glucocorticoide, comincia a presentare effetti immunosoppressivi, il che giustifica il suo uso nelle malattie autoimmuni e nei trapianti d’organo.
Nelle malattie autoimmuni e nella glomerulonefrite possiamo usare fino a 80 mg di prednisone al giorno. Nei casi gravi, usiamo una procedura chiamata terapia a impulsi, che consiste nella somministrazione endovenosa di fino a 1000 mg di metilprednisolone per 3 giorni consecutivi. Questa terapia a impulsi può essere utilizzata nelle vasculiti gravi, nei casi di rigetto di organi trapiantati e nel trattamento di malattie autoimmuni gravi e scompensate, come avviene in alcuni casi di Lupus, per esempio.
I corticosteroidi possono essere somministrati per varie vie. Per esempio, i corticoidi sistemici sono quelli assunti per via orale o endovenosa. Nell’asma, la somministrazione di corticosteroidi per via inalatoria è molto comune. Nella rinite e nella sinusite la via preferita è quella intranasale. Nelle malattie della pelle, i corticoidi sono topici, cioè in creme o unguenti. I corticoidi possono essere disponibili in gocce oculari e soluzioni da somministrare nelle orecchie. Nell’artrite, la via può essere intra-articolare (infiltrazione).
Assorbimento sistemico
La grande maggioranza degli effetti collaterali si verifica in pazienti che assumono corticosteroidi prolungati, ad alte dosi, per via orale o endovenosa. Questo non significa, tuttavia, che le altre forme di somministrazione di corticosteroidi siano prive di effetti avversi.
I corticosteroidi inalati, ampiamente utilizzati nel trattamento dell’asma, possono avere un assorbimento sistemico rilevante, anche se questo è molto inferiore a quello che si verifica con corticosteroidi somministrati per via orale. Il fluticasone inalato, per esempio, è noto per inibire la produzione di cortisolo da parte della ghiandola surrenale e può causare effetti collaterali sistemici se usato continuamente per diversi mesi, soprattutto nei bambini. Altre forme di corticosteroide inalato sembrano avere un minore assorbimento sistemico.
Le iniezioni intra-articolari di desametasone possono causare la sindrome di Cushing (spiego più tardi cos’è questo cambiamento).
Anche i corticosteroidi in pomata o crema possono essere assorbiti nel corpo abbastanza da causare effetti collaterali se usati per un tempo prolungato. L’assorbimento dei corticosteroidi nella pelle varia a seconda di una serie di fattori. Per esempio, aree come le pieghe della pelle, il cuoio capelluto e la fronte hanno maggiori probabilità di essere assorbite. Nei bambini e nelle zone con infiammazioni cutanee o peeling l’assorbimento sistemico dei corticosteroidi è anche maggiore.
In generale, non esiste una forma di corticosteroide che sia priva di effetti collaterali. Non importa la via, più lungo è il tempo di trattamento e la dose usata, maggiori sono i rischi di effetti avversi.
Effetti collaterali
Mentre sono farmaci estremamente utili in una varietà di malattie gravi, i corticosteroidi hanno, specialmente se usati a lungo termine, una lista enorme di effetti collaterali indesiderati, che vanno da problemi cosmetici a gravi infezioni dovute all’inibizione del sistema immunitario.
Gli effetti collaterali sono strettamente correlati alla dose e al tempo di utilizzo. L’uso sporadico e a breve termine non è probabile che porti agli effetti avversi che saranno descritti di seguito. Non c’è da preoccuparsi di prescrivere corticoidi per una sola settimana, anche se sono in dosi elevate. L’uso sarà indicato ogni volta che il medico giudicherà che la malattia da trattare è più grave dei potenziali effetti avversi.
Dopo aver letto questo articolo si può avere l’impressione che il prednisone e farmaci simili siano farmaci terribili. È importante notare che l’uso prolungato e ad alte dosi è di solito indicato solo in malattie gravi, che possono portare alla morte o a gravi limitazioni.
Effetti collaterali della pelle
Gli effetti estetici dei corticosteroidi danno più fastidio ai pazienti, soprattutto alle donne. Circa la metà degli individui che utilizzano almeno 20 mg al giorno di prednisone, o una dose equivalente di qualsiasi altro corticosteroide per tre o più mesi sperimenteranno effetti collaterali estetici.
Il più comune di questi includono ecchimosi e porpora associate ai corticosteroidi. Questi cambiamenti sono piccole emorragie che si verificano sotto la pelle, di solito in aree esposte al sole come mani e avambracci. Un altro effetto avverso comune è una pelle più sottile e fragile.
Strisce di colore viola situate nella regione addominale, calvizie, crescita dei capelli nelle donne e acne si verificano anche frequentemente in utenti cronici di corticosteroidi orali.
Il rischio di tumori della pelle di tipo non melanoma sembra essere più alto nelle persone che assumono corticosteroidi per un tempo prolungato.
I pazienti che assumono corticosteroidi in creme e unguenti per lungo tempo possono anche sperimentare effetti indesiderati sulla pelle, come atrofia, smagliature, teleangiectasia e macchie viola. Un aumento del rischio di infezioni fungine nella pelle si verifica anche con un trattamento prolungato.
Un segno tipico della tossicità dei corticosteroidi è lo sviluppo dell’aspetto “cushingoide”, che è caratterizzato da un viso arrotondato (chiamato facies lunare), accumulo di grasso nella regione posteriore del collo e della schiena (chiamato gobba o giba di bufalo), e distribuzione irregolare del grasso corporeo, con predominanza nella regione addominale e nel tronco.
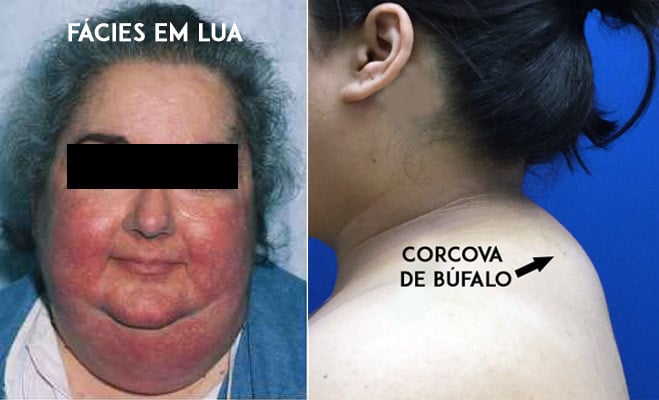
Questo insieme di effetti collaterali, chiamato sindrome di Cushing, è uno dei più fastidiosi, in quanto cambia notevolmente l’aspetto del paziente, soprattutto in persone che prima erano magre.
La sindrome di Cushing di solito appare entro i primi due mesi di trattamento con corticosteroidi a dosi superiori a 20 mg al giorno. In alcuni pazienti, tuttavia, dosi superiori a 10 mg al giorno sono già sufficienti a causare questo cambiamento.
Effetti collaterali sugli occhi
L’uso continuato di corticosteroidi sistemici, di solito per più di 1 anno con dosi maggiori dell’equivalente di 10 mg di prednisone al giorno, può portare a cambiamenti oftalmologici, come cataratta e glaucoma. Entrambi i corticosteroidi usati per via orale, nasale (spray nasale per l’asma o la bronchite) o sotto forma di collirio possono causare entrambe le malattie.
I pazienti che prendono corticosteroidi cronicamente dovrebbero essere valutati periodicamente da un oculista al fine di rilevare i segni precoci di cataratta o glaucoma.
Effetti metabolici
Dopo una dose di 5 mg al giorno c’è una chiara tendenza all’aumento di peso e all’accumulo di grasso nella regione del tronco e dell’addome. Più alta è la dose di corticoide, maggiore è l’aumento di peso.
Oltre all’accumulo di grasso, la corticoterapia cronica porta anche ad alterazioni del metabolismo del glucosio, e può anche causare il diabete mellito. Il rischio è maggiore negli individui che hanno già valori di glucosio leggermente alterati prima dell’inizio della corticoterapia. Anche se il diabete è reversibile nella maggior parte dei casi dopo la sospensione del farmaco, alcuni pazienti rimangono diabetici per tutta la vita.
Dosi giornaliere di prednisone superiori a 10 mg per più di 3 mesi possono anche causare cambiamenti nei livelli di colesterolo, cioè aumenti del colesterolo LDL (colesterolo cattivo) e trigliceridi, e ridotti livelli di colesterolo HDL (colesterolo buono).
Effetti cardiovascolari
L’incidenza di varie malattie cardiovascolari di solito aumenta con l’uso prolungato di corticosteroidi. Possiamo citare l’aumento di ipertensione, infarto miocardico, insufficienza cardiaca e ictus.
Il rischio di malattie cardiovascolari dipende dalla dose e dalla durata del trattamento. I pazienti che sviluppano la sindrome di Cushing di solito hanno il più alto tasso di aterosclerosi e il più alto rischio di problemi cardiaci.
Piccole dosi di corticosteroidi per un breve periodo non sembrano aumentare il rischio cardiovascolare in alcun modo rilevante.
Effetti muscoloscheletrici
L’uso cronico di glucocorticoidi è associato a diversi cambiamenti muscoloscheletrici. La più comune è l’osteoporosi. In questo caso, anche dosi basse come 2,5 mg o 5 mg al giorno, se usate cronicamente, possono accelerare la perdita di massa ossea.
La corticoterapia prolungata è anche responsabile di una maggiore incidenza di necrosi ossea, danni muscolari (miopatia), fratture ossee e disturbi della crescita quando viene usata nei bambini.
Effetti collaterali del sistema nervoso centrale
L’uso di corticoidi, all’inizio, può causare una sensazione di benessere ed euforia. Tuttavia, a lungo termine è associato a una maggiore incidenza di condizioni psichiatriche, come psicosi e depressione, così come insonnia e alterazioni della memoria.
Effetti immunologici
L’immunosoppressione causata dalla corticoterapia è un effetto desiderabile nei casi di malattie autoimmuni, ma può anche essere un grosso problema, poiché facilita la comparsa di infezioni. Bisogna saper bilanciare bene i rischi con i benefici.
Il rischio di infezione si presenta in coloro che prendono l’equivalente di 10 mg al giorno o più di prednisone per diversi giorni. Questo rischio diventa molto alto con dosi superiori a 40 mg al giorno o quando si ottiene una dose cumulativa di 700 mg di prednisone durante l’intero trattamento.
Oltre a facilitare l’infezione, i corticosteroidi inibiscono anche la comparsa della febbre, rendendo difficile il riconoscimento di un processo infettivo in corso.
I pazienti in dosi elevate di corticosteroidi dovrebbero evitare i vaccini composti da virus vivi, a rischio di sviluppare infezioni da vaccino. Si possono somministrare vaccini con virus uccisi, ma la corticoterapia può anche impedire la formazione di anticorpi, causando una scarsa efficacia dell’immunizzazione. Dosi maggiori sono spesso richieste per un’immunizzazione efficace.
La candidosi orale e la candidosi vaginale sono infezioni molto comuni nei pazienti che usano glucocorticoidi cronici.
Altri effetti
La lista dei possibili effetti collaterali dei corticosteroidi è molto ampia. Oltre a quelli già menzionati, altri effetti avversi relativamente comuni sono ritenzione di liquidi, cambiamenti mestruali, gastrite, ulcera peptica, steatosi epatica, pancreatite e infertilità.
Cura e pericoli dell’uso di corticosteroidi
La corticoterapia prolungata richiede una certa attenzione, soprattutto quando si interrompe il farmaco.
L’uso a lungo termine del prednisone o di farmaci simili inibisce la produzione naturale di cortisolo da parte della ghiandola surrenale. Poiché i corticosteroidi sintetici hanno un’emivita di poche ore, una brusca interruzione fa sì che dopo 2 o 3 giorni i livelli di cortisolo siano vicini allo zero. Quando il surrene è inibito per lungo tempo dalla somministrazione di corticosteroidi esogeni, ci vuole tempo prima che ritorni a produrre cortisolo naturalmente.
In generale, i trattamenti che durano meno di 3 settimane di solito non causano grandi effetti collaterali o provocano un’inibizione prolungata delle surrenali.
Poiché il cortisolo è un ormone essenziale per la vita, il paziente che interrompe bruscamente i corticosteroidi sintetici entra in uno stato chiamato insufficienza surrenalica, e può progredire verso lo shock circolatorio, il coma e la morte se non è curato rapidamente.
Pertanto, la sospensione dei corticosteroidi dopo un uso prolungato dovrebbe sempre essere fatta lentamente e gradualmente. Il trattamento non dovrebbe mai essere interrotto senza conoscenza medica.
Riferimenti
- Terapia corticosteroidea sistemica – effetti collaterali e loro gestione –
British Journal of Ophthalmology. - Recensione: effetti collaterali a lungo termine di glucocorticoidi – Journal Expert Opinion on Drug Safety.
- Glucocorticoidi – Huntington’s Outreach Project for Education, a Stanford.
- Prevenzione e trattamento degli effetti collaterali dei glucocorticoidi sistemici – International journal of dermatology.
- Uso farmacologico dei glucocorticoidi – UpToDate.
- Principali effetti collaterali dei glucocorticoidi sistemici – UpToDate.
- Effetti avversi dei corticosteroidi – StatPearls.
Lascia un commento