Dipol – dipólus erők
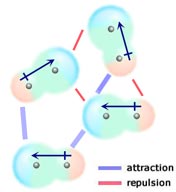
Ha két semleges, állandó dipólusmomentummal rendelkező molekula úgy kerül egymáshoz, hogy ellentétesen töltött végeik egymáshoz igazodnak, akkor vonzzák egymást. Folyadékban vagy szilárd anyagban ezek az együttállások előnyben vannak azokkal szemben, ahol a molekulák hasonló töltésű végei közel vannak egymáshoz, és ezért taszítják egymást.
Az egyik oka annak, hogy a CH3F forráspontja magasabb (-84 °C), mint a CF4-é (-128 °C), az, hogy a CF3H-nak állandó dipólusmomentuma van, míg a CF4-nek nincs. Ennek teljes megértéséhez tudni kell, hogy a CF4 tetraéderes alakú, a CH3F pedig nagyjából tetraéderes (nincs nagy különbség e molekulák alakja között). A szén-fluor kötések mindkét molekulában polárisak (a fluor sokkal elektronegatívabb, mint a szén), azonban a négy C-F kötés jelenléte a tetraéderes CF4 molekulában összességében nem teszi a molekulát polárissá. A CH3F-ben lévő egyetlen C-F kötés dipólusmomentumát nem semlegesítik a C-H kötés dipólusai (amelyek nagyon kicsik), így a CH3F-nek van állandó dipólusmomentuma.
A hidrogénkötés egy olyan típusú intermolekuláris erő, amely bizonyos körülmények között létrejöhet, és általában a dipólus-dipólus kölcsönhatások közé sorolják, bár van némi kovalens kötés jellege is.
Vélemény, hozzászólás?