THE BUCCAL REGION – AN ADVANTAGEOUS ROUTE FOR DRUG DELIVERY
Innovációk a gyógyszeradagolásban a dózisfüggő mellékhatások minimalizálását és a biológiai aktivitás maximalizálását ígérik, miközben javítják a betegek adherenciáját.
A gyógyszerek perorális beadása, amely a betegek tapasztalatai alapján a gyógyszerek beadásának preferált módja, számos hátrányt rejt magában, mint például a hepatikus first-pass metabolizmus, a hosszabb hatáskezdet és a gyógyszerek enzimatikus lebomlása a gasztrointesztinális (GI) traktusban. Ha a GI és a hepatikus lebomlás korlátozza egy gyógyszer biztonságosságát vagy hatékonyságát, gyakran az invazív injekció az egyetlen járható beviteli mód – aminek lehetséges következménye a betegek alacsonyabb adherenciája.

A bukkális beadással helyi és szisztémás hatást lehet elérni, és vonzó, mivel kiküszöböli a perorális beadás hiányosságait. A bukkális nyálkahártyán keresztül felszívódó anyagok ugyanis megkerülik a gasztrointesztinális enzimatikus lebomlást és a hepatikus first-pass hatást. A bukkális beadás továbbá jobb alternatívát jelent az injekciók vagy tabletták helyett azon betegek számára, akiknek nehézséget okoz a nyelés.
Mi a bukkális terület?
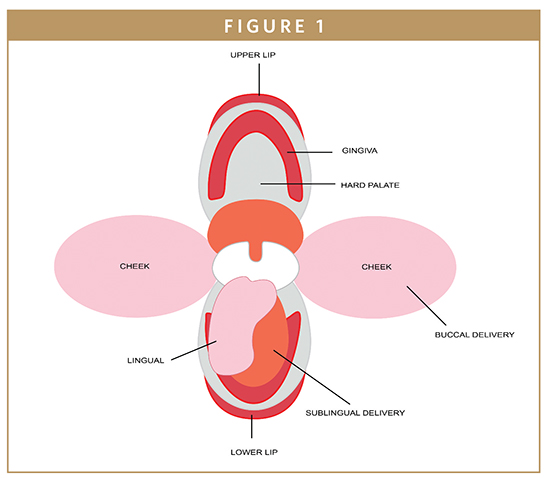
A bukkális terület az arc és az ajak belső bélése, amely a szájüreg felületének körülbelül egyharmadát teszi ki (1. ábra).1 A bukkális nyálkahártya rétegzett laphámból álló felszíni rétegből áll, amelyet egy bazális lamina köt össze az alatta lévő kötőszövettel. A kötőszövetben vérkapillárisok hálózata található, ahol a hámon áthatoló gyógyszerek a belső nyaki vénán keresztül a szisztémás keringésbe juthatnak.2
A bukkális hám a hidrofil gyógyszerek permeációjának gátjaként működik, míg a kötőszövet, amely inkább hidrofil jellegű, úgy tűnik, befolyásolja a lipofil vegyületek diffúziós késleltetési idejét.3 A nyálkahártyán keresztüli gyógyszer-transzport lehet transz- vagy paracelluláris (2. ábra), a legtöbb hidrofil hatóanyag és makromolekula passzív paracelluláris diffúzióval, a lipofil vegyületek és a kis hidrofób molekulák pedig túlnyomórészt paracelluláris transzporttal jutnak át.4 Így a sejtmembrán a hidrofil vegyületek fő transzportgátjaként működik, és a sejtek közötti terek jelentik a lipofil vegyületek permeációjának fő akadályát.

A mucoadhézió jelentősége
Mucoadhézióról akkor beszélünk, amikor két felület, amelyek közül az egyik egy nyálkahártya, egymáshoz tapad. Ez kritikus paraméter a bukkális beadás és az optimális tapadási tulajdonságokkal rendelkező formulációs anyagok kiválasztása szempontjából. A mukoadhézió két szakaszban történik – az érintkezési szakaszban, amelyet a konszolidációs szakasz követ, amikor az adhéziós kölcsönhatások létrejönnek. Az adhéziót valószínűleg többféle mechanizmus okozza. Fontos, hogy az adhéziós kapcsolat meghibásodása az adagolási forma túlhidratáltsága, vagy a hám- vagy nyálkahártya-forgalom következtében következik be. A bukkális epithelium forgalmi idejét 3-8 napra becsülik, szemben a bőr kb. 30 napos forgalmi idejével4.

A helyszín előnyei
A szisztémás adagolás fő előnye mellett, amely megkerüli a máj és a bél lebontását a nagyobb biológiai hozzáférhetőség és a kisebb mellékhatások érdekében, a szájban viszonylag nagy terület áll rendelkezésre a gyógyszer alkalmazásához és jó hozzáférhetőséggel rendelkezik az orrhoz, a végbélhez és a hüvelyhez képest.5 Emellett a bukkális nyálkahártya gyors sejtforgalma csökkenti a szövetkárosodás vagy irritáció kockázatát.6 Míg a nyelv alatti nyálkahártya áteresztőképesebb, vaszkularizáltabb és vékonyabb, mint a bukkális nyálkahártya, addig e nyálkahártya felülete kisebb, a nyál folyamatosan mossa, és a nyelv által kifejtett nyírás megnehezíti az adagolási forma érintkezésben tartását a nyelv alatti nyálkahártyával.7 Mindezen okok miatt az arcnyálkahártya a szájüregben az olyan szabályozott hatóanyag-leadású rendszerek beadásához, amelyeknek hosszabb ideig kell megtapadniuk.8
A hely korlátai
A bukkális szövet abszorpciós sebességének (μg/mm2/s) vagy permeabilitásának fokozása gyakran szükséges a rendelkezésre álló korlátozott felület kompenzálásához. A permeációfokozók (azaz az epidermisz vagy a hámstruktúrákat átrendező vagy a sejtek közötti szoros kapcsolódási pontokat megnyitó anyagok) alkalmazása nagyon fontos ezen a területen. A makromolekulákat bonyolultabb a nyálkahártyán keresztül juttatni a nyál enzimatikus lebomlása és a bukkális hámon keresztül történő gyenge permeáció miatt kémiai és elektromos alapú permeációfokozó nélkül.9 A permeációfokozók nem megfelelő alkalmazása biztonsági aggályokat okozhat a helyi szöveti irritáció tekintetében, de a nemkívánatos bolushatás következtében is, amely a vérben lévő gyógyszerkoncentrációt olyan szintre emeli, amely nem biztonságos.
A rosszul oldódó vagy permeábilis gyógyszerek szövetbe való nagyobb felszívódásának biztosítására szolgáló alternatív stratégia a szájban való tartózkodási idő növelése. A permeációfokozókhoz hasonlóan a tartózkodási idő növelése is okozhat szöveti irritációt, valamint a betegnek kellemetlen érzést, és gondos értékelést igényel mind a szöveti integritásra és funkcionalitásra gyakorolt azonnali, mind a hosszú távú hatások tekintetében. A szájüregben való tartózkodási idő növelése további kihívást jelenthet, mivel a gyógyszer a nyál öblítő hatása miatt gyorsan kiürülhet. Ennek eredményeként ismételt és gyakori adagolásra lehet szükség, kivéve, ha az adagolási forma erős kötést hoz létre a felszívódó nyálkahártyával. Kutatásokra van szükség annak számszerűsítésére, hogy a nyálöblítés mennyire befolyásolja a különböző gyógyszerhordozó rendszerekből történő orális transzmukózális adagolás hatékonyságát.
A humán tényezőket fontos figyelembe venni egy bukkális termék kifejlesztésekor. Tekintettel arra, hogy a bukkális nyálkahártya az orcák, az ajkak és az íny közötti felső és alsó térben húzódik, a pontos hely, ahová a beteg az adagolási formát helyezi, befolyásolhatja a gyógyszer tapadását és felszívódását, és ezek az emberi tényezők hatásai befolyásolhatják a betegek közötti variabilitást. Az adagolási forma elhelyezésének módja további komplikációkat okozhat, ha az adagolási formát egyirányú felszabadulásra tervezték, és a belső arcon elhelyezendő speciális tapadó oldallal rendelkezik. Végül, az, hogy a beteg mikor és mit eszik, iszik vagy dohányzik, tovább befolyásolhatja a gyógyszer nyálkahártyán keresztüli felszívódását.
A nyálstimuláció miatti kioldódás és a beteg variabilitásának kockázata minimalizálható, ha a gyógyszert például éjszaka adják be, amikor a beteg nem eszik vagy nem beszél.
Bukkális adagolási formák
Bár a bukkális nyálkahártyát mint új gyógyszerbeviteli útvonalat csak most vizsgálják széles körben, a gyógyszerbevitelben rejlő potenciálját az emberiség már évszázadok óta ismeri. Az amerikai őslakosok az 1500-as években ismertették meg a rágódohányt az európai telepesekkel, a kokaleveleket pedig 8000 évvel ezelőtt a perui gyűjtögetők rágták. A szájnyálkahártyát a hagyományos adagolási formák, mint például a tabletták, trócsák és pasztillák, valamint szájöblítők és spray-k segítségével célozták meg, és jelenleg számos ilyen termék van forgalomban. A kihívást az jelenti, hogy ezeket az adagolási formákat a felszívódás helyén kell tartani, az adagolás pontossága (folyadékok) és kényelmetlensége (tabletták). A tabletták képesek leválni a nyálkahártyáról, lenyelni, majd a nyelőcső falához tapadni, ami fulladásveszélyt jelent, különösen a gyermekek és az idősek számára.
A hagyományos adagolási formák korlátainak leküzdésére egyre fejlettebb gyógyszerhordozó rendszereket fejlesztenek ki, többek között filmeket, tapaszokat, kétrétegű tablettákat, hidrogéleket és szalagokat, valamint mikro- és nanorészecskék használatát.
FILMEK BUKKÁLIS BEADAGOLÁSHOZ – CUREFILM
A mukoadhezív filmek a bukkális nyálkahártya-adagolás kedvelt adagolási formái rugalmasságuk, kényelmük, ízletességük és állítható méretük miatt. A tapadó tablettákhoz képest jobb betegkövetést mutattak ki.10,11 A folyékony, gél és kenőcs formulákkal ellentétben a mukoadhezív filmek hosszabb ideig maradnak kapcsolatban a nyálkahártyával, nagyobb felületet fednek le, és ezért pontosabb gyógyszeradagolást biztosítanak.12 A mukoadhezív filmeket gondos anyagválasztással úgy lehet kialakítani, hogy a nyálkahártyával kiterjedt tapadó kapcsolatot tartsanak fenn, meghosszabbítva az adagolórendszer retenciós idejét a nagyobb teljes gyógyszerfelszívódás érdekében. Továbbá a mukoadhezív filmek jól alkalmazhatók helyi terápiára, például a szájüregi sebfelületek fertőzéssel szembeni védelmére.13
A filmkompozíciókat a következő fizikai tulajdonságok elérésére tervezték: bioadhezív szilárdság, szakítószilárdság, hajlékonyság, rugalmasság és meghosszabbított dezintegráció. Ezek a tulajdonságok kritikusak a megcélzott hatóanyag-felszabadulási profil, a betegek elfogadhatósága és a kereskedelmi gyártási folyamatokkal való kompatibilitás elérése érdekében. A bukkális polimer filmek célspecifikációinak elérése nagymértékben függ a kiválasztott polimerek típusától és koncentrációjától, valamint a hatóanyag adagjától.
Amint azt itt tárgyaltuk, még egy erősen tapadó film esetében is a nyálfolyás hatására a film egy része feloldódik a szájüregben és lenyelésre kerül. Az okkluzív fedőréteggel ellátott kétrétegű filmeket úgy tervezték, hogy egyirányú hatóanyag-felszabadulást és felszívódást eredményezzenek a bukkális nyálkahártyán, és nagy hatóanyag-dózisokat tudnak szállítani. Bár az ilyen kialakítások javíthatják a bukkális felszívódást, számos hátrányuk van. Alkalmazásuk során felhasználói hibákhoz vezethetnek, az okklúziós réteg leválhat és fulladásveszélyessé válhat, végül pedig a kétrétegű filmek méretezésének bonyolultsága növeli a gyártási költségeket.
A CURE Pharmaceuticalnak a CUREfilmmel a bukkális filmek fejlesztéséhez alkalmazott megközelítése ezeket a korlátokat figyelembe véve a jobb hatóanyag-felszabadulási profilok létrehozása érdekében kihasználja az egyrétegű filmek elkerülhetetlen nyálcsorgását. Termékeinket úgy tervezzük, hogy a bukkális adagolás gyors bólushatását kombináljuk a GI adagolás meghosszabbított felszabadulásával, hogy átfogó pulzáló vagy tartós felszabadulású profilt érjünk el. A bukkális adagolás esetén a vérszint gyorsan tetőzhet, és a rövidebb felezési idő azt jelentheti, hogy a hatás gyorsan elmúlik. Továbbá, ha egy gyógyszer nagy dózisát kizárólag bukkálisan juttatjuk be (pl. 100 mg felett), a helyi szöveti koncentráció túl magas lehet, és károsíthatja a szövetet. Az egyrétegű megközelítés előnyösebb, mivel minimalizálja a költségeket és a felhasználói hibákat.
A bukkális CUREfilm létrehozásához polimerek, permeációfokozók és lipidek gondosan kiválasztott keverékét kombinálják a tapadás, a gyógyszer diffúzió és a nyálkahártyán keresztüli permeáció optimalizálása érdekében. A lipidek döntő szerepet játszanak a hatóanyagok szolubilizációjában és stabilitásában. Segítenek a hidrofil vegyületek átvezetésében a nyálkahártya hámján, és elősegítik a lipofil vegyületek transzcelluláris transzportját a hámon keresztül az erekbe. A hatóanyag nano-partikulációja egy további nyílvesszőt jelenthet a formulálónak a felszívódási sebesség növelésére.
A lenyelt hatóanyagrész megfelelő gyomorvédelme és hatékony bélrendszeri felszabadulása érdekében a gyógyszerrészecskéket a filmmátrixba való beépítés előtt teljesen vagy részben kapszulázzák, bélbevonattal látják el, vagy polimerekkel, például kitozánnal keresztkötik őket. Más stratégiák közé tartozik a liposzómás vagy micelláris képződés, a ko-kristályosítás és a zselésedő vagy duzzadó polimerek használata.
Ez a kettős stratégia nagyon hasznos lehet különböző metabolikus profilú kombinált gyógyszerek esetében, ahol az egyik hatóanyagot bukkális felszívódásra készítik (azaz, ha magas first pass hatású), a másikat pedig a GI-ben történő felszabadulásra készítik.
Összefoglaló
A hatékony terápiás beadásra képes orális film tényleges megtervezése és előállítása kihívást jelenthet, és új technológiák létrehozását igényli. Ezen innovációk eredményeként a bukkális filmek ma már olyan kereskedelmi szempontból életképes adagolási formát jelentenek, amely a gyógyszeripar, a betegek és ápolóik számos problémáját képes megoldani. Képesek lesznek helyettesíteni a napi injekciókat, például a Parkinson-kórban szenvedő betegek által szedett apomorfin injekciókat. Javíthatják a gyógyszerek, például a kannabinoidok biológiai hozzáférhetőségét, potenciálisan csökkentve azok dózisát és pszichoaktív mellékhatásait. Ha gyors tünetmentesítésre van szükség, bólushatást biztosíthatnak. A gyermekek számára kényelmes alternatívát jelentenek az élvezhetetlen folyadékok és az idősek számára a nehezen lenyelhető tabletták helyett.
Az általuk kielégített fontos, kielégítetlen piaci igények miatt az orális filmek elterjedési aránya magas. Valóban, a globális piac értéke 2017-ben 2,1 milliárd dollár volt, és várhatóan 13%-os CAGR-rel fog növekedni a 2018 és 2026 közötti előrejelzési időszakban.14 Az orális filmek, köztük a bukkális filmek ilyen mértékű kereskedelmi növekedése azt tükrözi, hogy a gyógyszeripar egyre nagyobb hangsúlyt fektet a betegközpontú innovációra az új gyógyszerek kifejlesztése és a régi gyógyszerek fejlesztése során – ahol a betegek tapasztalata határozza meg a gyógyszeradagolás tervezését, ami viszont javítja a betegek eredményeit.
- Curatolo W. The lipoidal permeability barriers of the skin and alimentary tract. Pharm Res. 1987;4(4):271-277.
- Colombo P, Cagnani S, Buttini F, Santi P, et al. Biological In Vitro Models for Absorption by Non-Oral Routes, Reference Module in Chemistry, Molecular Sciences and Chemical Engineering, Elsevier. 2013.
- Kulkarni U, Mahalingam R, Pather SI, Li X, Jasti B. Porcine buccal mucosa as an in vitro model: relative contribution of epithelium and connective tissue as permeability barriers. J Pharm Sci. 2009;98(2):471-483. doi: 10.1002/jps.21436.
- Gandhi RB, Robinson JR. Oral cavity as a site for bioadhesive drug delivery Adv Drug Deliv Rev. 1994;13:43-74.
- Rathbone MJ, Drummond BK, Tucker IG. The oral cavity as a site for systemic drug delivery Adv Drug Deliv Rev. 1994;13:1-22.
- Squier CA, Wertz PW. Structure and Function of the Oral Mucosa and Implications for Drug Delivery M.J. Rathbone (Ed.), Oral Mucosal Drug Delivery, Marcel Dekker, New York. 1996:1-26.
- Madhav NVS, Shakya AK, Shakya P, Singh K. Orotransmucosal drug delivery systems: a review. J Control Release. 2009;140:2-11.
- Madhav NVS, Shakya AK, Shakya P, Singh K. Orotransmucosal drug delivery systems: a review J Control Release. 2009;140:2-11.
- Morales JO, Brayden DJ. Kis molekulák és biológiai szerek bukkális szállítása: a mukoadhezív polimerek, filmek és nanorészecskék. Current Opinion Pharmacol. 2017;36:22-28.
- Kraisit P, Limmatvapirat S, Nunthanid J, et al. Hidroxipropil-metilcellulóz/polikarbofil mukoadhezív keverékfilmek előállítása és jellemzése keveréktervezési megközelítéssel Chem Pharm Bull. 2017;65(3):284-294.
- Giovino C, Ayensu I, Tetteh J, et al. Inzulinnal töltött PEGb-PLA nanorészecskékkel (NP-k) impregnált kitozán filmek fejlesztése és jellemzése: potenciális megközelítés makromolekulák bukkális adagolására. Int J Pharm. 2012;428(1-2):143-151.
- Abruzzo A, Bigucci F, Cerchiara T, et al. Mucoadhesive chitosan/gelatin films for buccal delivery of propranolol hydrochloride. Carbohydr Polym. 2012;87(1):581-588.
- Tejada G, Lamas MC, Svetaz L, Salomón CJ, Alvarez VA, et al. Effect of drug incorporation technique and polymer combination on the performance of biopolymeric antifungal buccal films. Int J Pharmaceut. 2018;548(1):431-442.
- Transparency Market Research (TMR) jelentés. Oral Thin Films Market – Global Industry Analysis, Size, Share, Growth, Trends, and Forecast, 2018-2026.

Robert Davidson a CURE vezérigazgatója és az igazgatótanács karigazgatója. A CURE Pharmaceuticalnál betöltött szerepét megelőzően az InnoZen Inc. elnök-vezérigazgatója, a Gel Tech LLC vezérigazgatója, a Bio Delivery Technologies Inc. vezérigazgatója volt, és több vállalati igazgatótanácsban is tevékenykedett. Davidson úr felelős volt számos gyógyszeradagolási technológia és kereskedelmi márkabővítés fejlesztéséért. A Villanova Egyetemen szerzett mesterdiplomát alkalmazott projektmenedzsmentből, a virginiai American Military University-n közegészségügyi mesterdiplomát, valamint a virginiai Liberty University-n egészségügyi és wellness mesterképzést. Davidson posztgraduális tanulmányait a Cambridge-i Egyetemen is elismerő oklevéllel zárta.

Jessica Rousset a CURE operatív igazgatója. Rousset asszony felügyeli a működést, és irányítja a vállalati stratégiát és növekedést. Rousset asszony korábban a Los Angeles-i Gyermekkórház innovációs vezetőjeként dolgozott, ahol tíz éven keresztül segített terápiás és orvostechnikai eszközöket gyártó cégek elindításában, valamint megalapított és működtetett egy országos gyermekgyógyászati technológiai gyorsítót. Ezt megelőzően Rousset asszony a The Scripps Research Institute-nál és a GlaxoSmithkline Biologicalsnál töltött be laboratóriumi, klinikai kutatási és üzletfejlesztési pozíciókat. Biokémiai mérnöki képesítést szerzett a lyoni Institut National des Sciences Appliquées-ben (Franciaország).
Vélemény, hozzászólás?