ORIGINAL PAPERS
Hepatitis B surface antigen detection using pooled sera. Egy költség-haszon elemzés
E. Fernández, L. Rodrigo1, S. García, S. Riestra1 és C. Blanco
Biokémiai Szolgálat. Hospital de Cabueñes. Gijón. 1Gasztroenterológiai szolgálat. Hospital Central de Asturias. Oviedo. Spanyolország
Korrespondencia
ABSZTRAKT
Célkitűzések: a hepatitis B felszíni antigén (HBsAg) szűrésére szolgáló enzim immunoassay (EIA) segítségével történő 5 mintás pooling stratégia megvalósíthatóságának vizsgálata és költség-haszon elemzésének elvégzése.
Anyag és módszerek: A pooling módszer érzékenységének és specificitásának felmérése érdekében a 40 pozitív szérum (a gyengétől az intenzíven HBsAg-pozitívig) és 250 negatív szérum mindegyikét 4 HBsAg-negatív szérummal egy poolban vizsgálták. A HBsAg/ad és HBsAg/ay kimutatási határát tisztított altípusok szérumainak felhasználásával értékelték. Valós körülmények között 340 terhes nőből származó poolok felhasználásával végeztek vizsgálatot.
Eredmények: A technika érzékenysége és specificitása 100%-os volt. Az egyedi és összevont körülmények között vizsgált 40 minta minta/kivágás aránya közötti korrelációs együttható 0,792 volt (p < 0,005). Az összevont módszerrel a HBsAg/ad és HBsAg/ay kimutatási szintje alacsonyabb, 0,20 ng/ml és 0,12 ng/ml, míg az egyszeri módszerrel 0,34 ng/ml és 0,29 ng/ml. Az összevonásos módszer nem veszít érzékenységéből a pozitív szérummal kevert négy szérumban lévő anti-HBs 100 IU/L értékekig. A költség-haszon elemzés azt mutatta, hogy a pooling módszerrel a HBsAg-meghatározás költségeinek 30%-tól 75%-ig terjedő megtakarítást lehet elérni, attól függően, hogy a szeroprevalencia 10% vagy 1% volt.
Következtetések: Az összevont HBsAg EIA nem hozott rosszabb eredményt, mint az egyszeri EIA-vizsgálat, és költséghatékony és érvényes stratégiát jelentett a magas, közepes vagy alacsony prevalenciájú területeken.
Kulcsszavak: Hepatitis B felszíni antigén. Szérumok összevonása. Költség-haszon elemzés.
Rodrigo L, Fernández E, García S, Riestra S, Blanco C. Hepatitis B felszíni antigén kimutatása összevont szérumok felhasználásával. Költség-haszon elemzés. Rev Esp Enferm Dig 2006; 98: 112-121.
Bevezetés
A hepatitis B vírus (HBV) fertőzés világszerte emberek millióit érintő betegség. Fő rezervoárja a krónikus HBV-hordozóké. Becslések szerint világszerte mintegy 300 millió ember fertőzött ezzel a vírussal (1). A HBV-fertőzés orvosi következményei változóak és kiszámíthatatlanok, olyan tényezőktől függően, mint a beteg életkora és immunstátusa. A HBV a krónikus hepatitis, a májcirrózis és a hepatocelluláris karcinóma jól ismert etiológiai kórokozója.
A fertőzés gyakoriságában azonban nagy különbségek vannak, és ez vezetett a magas, közepes és alacsony endémiájú három fő terület felállításához (2). A legtöbb fejlett országban a krónikus HBV-hordozók prevalenciája kevesebb, mint 2%, és a fertőzés átadása mindenekelőtt bizonyos rizikócsoportokhoz tartozó felnőttek (kábítószer-használók, homoszexuális férfiak, promiszkuózus heteroszexuálisok, egészségügyi dolgozók) körében történik (3). Spanyolországban a HBV-hordozók 1,2%-os prevalenciáját találták (4), és a HBsAg azonosítása véradóknál, terhes nőknél és autotranszfúziós programban részt vevő személyeknél kötelező.
A szérum pooling technika a költségek csökkentésére törekszik a hatékonyság elvesztése nélkül, és elsősorban a fejlődő országokban alkalmazzák a humán immundeficiencia vírus (HIV) (5-14) és a hepatitis C vírus (HCV) (15-19) elleni antitestek keresésére. Az ezzel a módszerrel elért eredmények rendkívül ígéretesnek bizonyultak, mivel jelentősen csökkentették a laboratóriumi vizsgálatok költségeit anélkül, hogy azok érzékenysége jelentősen romlott volna.
A jelen tanulmány megkísérli felmérni, hogy a szérum pooling technika alkalmazható-e a HBsAg kimutatására, hogy megvilágítsa azokat a tényezőket, amelyek módosíthatják az érzékenységét, és hogy elvégezze e diagnosztikai technika költség-haszon elemzését.
Anyag és módszerek
HBsAg-meghatározás
A HBsAg-meghatározáshoz az Imx HBsAg-tesztet (Abbott Laboratories, Abbott Park, IL) használták, amely egy minőségi, harmadik generációs mikropartikuláris enzimimmunpróba (EIA). A HBsAg jelenlétét vagy hiányát úgy határozzák meg, hogy a fluoreszcens termékképződés sebességét összehasonlítják egy határértékkel, amelyet a negatív kalibrátor (N) arányból (HBsAg-ra nem reagáló emberi plazma) számítanak ki. Az Imx HBsAg-teszt kiszámítja a minta (S) és a negatív kalibrátor arányát. A határértéket (S/N) 2-ben állapították meg az egyszérumos EIA esetében.
A pooling technikát 200 mcL hozzáadásával végezzük, azaz a pool-t alkotó 5 szérum mindegyikéből 40 mcL keveréket kapunk (1/5 hígítás). A határértéket a negatív minták átlaga plusz 3 standard eltérésként határoztuk meg, így 1 értéket kapunk. Ezért úgy tekintjük, hogy ebben az 5 fős csoportban egy nem reaktív minta van, ha az S/N együttható < határérték, míg egy > S/N pool > határérték legalább egy reaktív minta jelenlétére utalhat. Ebben az esetben újra kell vizsgálni az egyes mintákat a reaktív minta(k) azonosítása érdekében. Minden vizsgálatot két példányban végzünk.
A fentiekkel összhangban a specificitást 250 negatív szérum 50 pooljának HBsAg értékelésével értékeltük. Az érzékenység kiszámításához 40 olyan szérumot vizsgáltak egy 4 negatív szérumot tartalmazó poolban, amelyek koncentrációeloszlása megegyezett az általános populációéval, amelyből a mintát vették.
HBsAg altípusok (ad és ay)
Az Imx HBsAg kimutatási határát az ad és ay esetében a tisztított HBsAg altípusok paneléből (hepatitis HBsAg sensitivity panel, Abbott Laboratories) származó szérumok felhasználásával értékelték. A HBsAg/ad és HBsAg/ay koncentráció 0,13 és 2,32 ng/ml, illetve 0,21 és 2,24 ng/ml között mozgott. A kimutatási határértéket egyedileg és 4 HBsAg-negatív szérumot tartalmazó poolban határozták meg.
A HBsellenes szint befolyása
Annak megállapítására, hogy az összevont teszttel vizsgált szérumokban lévő HBsellenes antitestek semlegesíthetik-e a HBsAg-ot és befolyásolhatják-e a technika érzékenységét, azt a módszert alkalmaztuk, hogy egy ismert HBsAg/ad és HBsAg/ay koncentrációjú szérumot négy ismert HBsellenes titerrel rendelkező szérummal összevontunk.
Az anti-HBs mennyiségi meghatározását mikropartikuláris enzim immunoassay (mEIA) módszerrel végeztük AxSYm autoanalizátorral (AxSYmTM AUSAB, Abbott Laboratories, Abbott Park, IL). A magas anti-HBs titerrel rendelkező szérumokat oltás utáni HBV kontrolloktól és hepatitis B-ből felépült betegektől nyertük.
Pool-teszt a HBsAg szűrésében
A pool-teszt érvényességének felmérése érdekében a fenti módszerrel a terepi műveletek szimulációját végeztük el 1525 szérummintán, amelyeket egy korábbi, általunk a HCV-fertőzés prevalenciájának becslésére végzett vizsgálat során terhes nőktől nyertünk, és amelyek mintáit a gyűjtés óta -20 ºC-on tároltuk. Ezek közül véletlenszerűen kiválasztottunk 300 negatív HBsAg és 14 pozitív HBsAg mintát. A meghatározásokat a poolok összetételének előzetes ismerete nélkül végeztük.
A vizsgálatok számának csökkentése
Ha egy pool pozitív eredményt ad, minden egyes komponenst külön-külön újra kell vizsgálni annak érdekében, hogy azonosítani lehessen a HBsAg-pozitív mintát vagy mintákat. Ezért minél nagyobb a pozitív poolok száma (azaz a HBsAg prevalenciája), annál kisebb az elvégzett tesztek számának csökkenése.
Ennek alapján a tesztek számának százalékos csökkenését a HBsAg-ra szűrő összevont szérumok használata esetén a legkedvezőtlenebb és legvalószínűtlenebb feltételek (alacsony prevalencia) mellett számították ki, azaz amikor a poolok egyikében sem volt egynél több pozitív szérum. Például 2%-os HBsAg-szeroprevalencia esetén, ha 20 poolban 100 szérumot elemeznek, ezek közül 2 lesz pozitív. Tehát a 20 eredeti meghatározáshoz (20 pool) hozzá kell adni 10 meghatározást (10 egyenként újravizsgált szérum), ami összesen 30 meghatározást eredményez. Ebben a példában a költségek 70%-át lehet megtakarítani. A költség-haszon elemzés elvégzése érdekében a HBsAg-vizsgálat árát mintánként 3 USA-dollárra becsülték. Ez a kórházunkban a kereskedelmi készlet tényleges átlagárán alapul.
Statisztikai elemzés
Az adatokat adatbázisba gyűjtöttük, majd később az SPSS for Windows, Release 10.0 statisztikai csomag segítségével elemeztük. Spearman nem parametrikus lineáris korrelációt alkalmaztunk. Az eredményeket átlag ± SD-ben fejeztük ki. A p < 0,05 szintet statisztikailag szignifikánsnak tekintettük.
Eredmények
A HBsAg-negatív szérumok 50 poolja közül egy sem volt pozitív (S/N pool > 1), és a következő S/N pool értékeket kaptuk: 0,767 ± 0,076 (tartomány 0,67-0,88). Ennél a mintánál az összevonási technika specificitása tehát 100%-os volt. Másrészt mind a 40 HBsAg-pozitív szérum, amikor összevont formában határozták meg, 1-nél nagyobb S/N értékeket mutatott (az érzékenység szintén 100% volt). Az S/N-arányok közötti korrelációs együttható e 40 minta esetében, ahogyan azt egyenként és poolban vizsgálták, 0,792 volt (p < 0,05).
A magas HBsAg-titerrel rendelkező mintákat tartalmazó poolok 26,6 százalékának S/N-aránya még nagyobb volt, mint az egyetlen mintáé. Az alacsony HBsAg-titerrel rendelkező minták (S/N egyszeres < 25, n = 12) korrelációs együtthatója azonban kiváló volt (R = 0,9739, p < 0,05), amint az látható (1. ábra).

A kimutatási határ az egyszeres módszerrel 0 volt.34 ng/ml az ad altípusra és 0,29 ng/ml az ay altípusra, míg az összevonásos módszerrel alacsonyabb antigénszinteket mutattak ki: 0,20 ng/ml és 0,12 ng/ml. A HBsAg/ad és HBsAg/ay különböző koncentrációjú szérumokra alkalmazott egyedi és összevont technika eredményei láthatóak (2. ábra).

Amikor az anti-HBs-titer a poolban kevesebb, mint 100 IU/L, a technika nem veszít érzékenységéből; még akkor is, ha az anti-HBs-titer eléri a 10 000 IU/L-t, a technika képes akár 1,5 ng/ml HBsAg-koncentrációt is kimutatni. Bemutatjuk a különböző anti-HBs-koncentrációk hatását a HBsAg altípusok kimutatási határára a pooling módszer alkalmazása esetén (2 meghatározás átlaga) (3. ábra).
A terhes nők szérumán valós körülmények között végzett vizsgálatban a pooling módszer az összes elemzett minta helyes osztályozását eredményezte. Következésképpen az érzékenység és a specificitás 100%-os volt.
A HBsAg szeroprevalenciájának növekedésével csökken a pooling módszerrel elért vizsgálati szám százalékos csökkenése. Látható, hogy még a vizsgált mintában 10%-os HBsAg-prevalencia esetén is legalább 30%-os minimális megtakarítás érhető el (4. ábra).

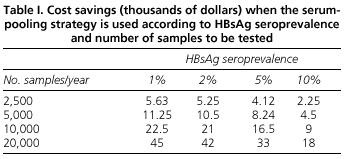
A szérum-összevonási stratégia gazdasági előnyeinek elemzése azt mutatja, hogy az elért megtakarítás a HBsAg prevalenciájától és az elvégzendő meghatározások számától egyaránt függ. Így az olyan alacsony prevalenciájú országokban, mint a miénk, a pooling módszer csökkenti a HBsAg vizsgálatának költségeit. Becsléseink szerint például egy laboratóriumban egy év alatt elvégzett 2500 meghatározás esetén a pooling-módszer alkalmazásával a megtakarítás 5630 USA-dollárt tesz ki, egy nagyon forgalmas, évente 20 000 meghatározást végző kórház esetében pedig a megtakarítás eléri a 45 000 USA-dollárt (I. táblázat).
Diszkusszió
A pooling módszer egyik megközelítése, hogy az egyes pooling tesztekben a hígítás és a reakcióelegy végső térfogatát meg kell tartani annak érdekében, hogy ne veszítsen az érzékenységéből, amihez a hígítót csökkentik, és részben a további szérumokkal helyettesítik. Ily módon nem szükséges módosítani a határértéket a standard módszerhez képest az individualizált mintákban. A vizsgálatunkban alkalmazott módszer azonban automatizált volt, és a minták hígítását autoanalizátorral végeztük. Emiatt minden minta 1:5 arányú hígítást mutat a másik 4 szérummal való keveréskor. Ezért vizsgálatunkban szükség volt a határérték módosítására és a poolban lévő szérumok számának korlátozására annak érdekében, hogy az érzékenység ne csökkenjen.
A specificitás tekintetében meg kell jegyezni, hogy a poolok átlagértéke csak alig több mint 3 szórásnyira volt a határértéktől. Így az esetek körülbelül 1%-ában lehet hamis pozitív eredményre számítani. Úgy gondoljuk, hogy ez elfogadható, mivel a specificitás közel 100%-os (99,9%). Nagyszámú különböző egyéntől származó nagyobb számú negatív mintát tartalmazó vizsgálatra lesz szükség ahhoz, hogy megállapíthassuk a vizsgálat valódi specificitását.
Bár az egyedi és az összevont minták vizsgálata közötti korreláció jó, a regressziós egyenes az X tengelyt 3 S/N aránynál metszi (a megfelelő Y érték 1). Ez azt jelentheti, hogy minden olyan minta, amelynek S/N-aránya 2 és 3 között van az egyedi mintás vizsgálatban, 1 alatti értéket kapna, és ezért nem lenne kimutatható az összevont vizsgálatban.
A HBsAg-pozitív szérumok 1%-os prevalenciája esetén a Liu és munkatársai (19) által leírt matematikai modell 11 szérumos poolméret esetén érte el a tesztek számának maximális csökkentését (80,5%). Véleményünk szerint azonban probléma merülhet fel a specificitással kapcsolatban a poolingnak a hamis-pozitív arányra gyakorolt hatása miatt. A szérumok keveredéséből adódóan a nem specifikus fehérjék számának növekedése a háttérszín növekedéséhez vezethet. A vizsgálatunkhoz választott 5 fős pool méret és a cutoff érték 2-ről 1-re történő módosítása mellett nem tapasztaltunk veszteséget az érzékenységben (hamis negatív eredmények) vagy a specificitásban (hamis pozitív eredmények).
A jelen vizsgálat eredményei azt mutatják, hogy a HBsAg kimutatására szolgáló szérumok összevonásának technikája rendkívül érzékeny és specifikus, és jelentős gazdasági megtakarítást is lehetővé tesz. Ezek az eredmények hasonlóak más kutatók eredményeihez, akik az összevonás módszerét a HCV- és HIV-fertőzés vizsgálatára alkalmazták (5-19). Eddig csak két tanulmány (20,21) számolt be a pooling-módszer HBV-fertőzés vizsgálatára történő alkalmazásáról. Ezek közül az egyikben (20), amelyet a hepatitis B rutinszerű, születés előtti szűrése során végeztek 10 minta pooljának vizsgálatával, a szerzők a krónikus hordozók alacsony prevalenciáját találták (0,43%), és arra a következtetésre jutottak, hogy ez költséghatékony módszer és érvényes stratégia az alacsony szeroprevalenciájú területeken, az érzékenység 4,2%-ra becsült csökkenése mellett. A mi vizsgálatunkban a pooling módszer alkalmazása terhes nőkre, akik között a HBsAg krónikus hordozóinak prevalenciája 0,93%, 100%-os érzékenységet és specificitást mutatott.
A HBsAg két fő altípusának (ad és ay) eloszlása a mi környezetünkben mindkét altípusra körülbelül 50%, az ay gyakoribb a parenterális utat használó kábítószerfüggőknél (22). Kimutattuk, hogy a pooling módszer javítja az érzékenységet, azaz csökkenti a két fő HBsAg altípus meghatározására használt immunpróba kimutatási határát. Az általunk alkalmazott pooling-technika lehetővé teszi a HBsAg/ad 0,20 ng/ml-es, illetve a HBsAg/ay 0,12 ng/ml-es mennyiségének kimutatását, ami még a standard módszerrel kapott értékeknél is alacsonyabb. A pool-teszteléssel megnövekedett érzékenység megállapítása nem meglepő, mivel erről már más szerzők is beszámoltak (16). Fontos felmérni a poolvizsgálathoz használt EIA-készlet érzékenységét, mert nem minden készlet alkalmas a poolok szűrésére, amint azt a hepatitis C vírus elleni antitestek esetében is kimutatták (23,24).
A poolszérumokban lévő anti-HB-k jelenléte módosíthatja a technika érzékenységét, de csak a 10 000 IU/ml-nél magasabb titerek esetén, ami csak az oltás utáni kontrollvizsgálatokból származó mintákban figyelhető meg; ebben a helyzetben a HBsAg meghatározása nem indokolt. Valójában Cunninghan és munkatársai (20) azt találták, hogy a terhes nők szérumaiból összeállított poolok mindössze 4,5%-ában volt 7500 IU/L-nél nagyobb anti-HBs-titer. Figyelembe véve a pooling módszer érzékenységének ezt a korlátozását, úgy találták, hogy az érzékenység és a specificitás is 100% körüli. Eredményeink más, alacsony prevalenciájú területeken is reprodukálhatók lehetnek, de a HBV szempontjából magas endémiájú területeken előzetesen bizonyítani kell őket. Ezeken a területeken a lakosság nagy része már immunizált e vírus ellen, és lehetséges, hogy a szérumokban talált anti-HBs-titerek kissé emelkedettek.
Rabenau és munkatársai (21) a miénkhez hasonló EIA-rendszerrel vizsgálták a plazmapoolokban végzett HBsAg-szerológiai vizsgálatok biztonságosságát. Vizsgálatukban a HBsAg kimutatását befolyásolta az alacsony anti-HBs-titerek jelenléte 5 óra inkubáció után. Az immunkomplex disszociációt követően azonban a HBsAg még magas anti-HBs-tartalom jelenlétében is kimutatható volt a poolban. Vizsgálatunkban kimutattuk, hogy csak 10 000 IU/L-nél magasabb anti-HBs-titerek esetén következik be jelentős érzékenységcsökkenés. Ezek a különbségek annak tudhatók be, hogy esetünkben a mintákat előzetes inkubáció nélkül vizsgáltuk. Ez megakadályozhatja az antigén semlegesítését az immunkomplexképződés által.
Ezért úgy gondoljuk, hogy mind a szérum anti-HBs titer, mind a minták EIA-val történő vizsgálat előtti feldolgozása befolyásolhatja az összevonásos módszer érzékenységét. Minden laboratóriumnak, amely ezt a technikát használni kívánja, szem előtt kell tartania ezt a két tényezőt, mielőtt általános használatba venné.
A WHO a szérum pooling módszer alkalmazását javasolja HIV-fertőzés esetén, ha a betegség prevalenciája kevesebb, mint 2%, és legfeljebb 5 szérum poolingjával (25). Ezeket az útmutatásokat követve a legtöbb tanulmány az alacsony szeroprevalenciájú területeken a pooling technikát alkalmazza és ajánlja. Tanulmányunkban bemutatjuk, hogy a szérumok összevonása költséghatékony lehet a HBsAg-hordozók magas prevalenciájával rendelkező populációkban is. Ez lehetővé teheti alkalmazását a HBV-fertőzés közepes és magas endémiájú területeihez tartozó országokban, ami általában egybeesik az elmaradott vagy fejlődő országokkal, vagyis azokkal, amelyeknek nagyobb szükségük van a laboratóriumi vizsgálatokkal járó gazdasági költségek csökkentésére. Mindazonáltal hasonló vizsgálatokat kell végezni ezeken a területeken, hogy megerősítsük eredményeinket. Azt azonban már kimutatták, hogy az olyan országokban, mint Kenya, ahol magas a HIV-fertőzés gyakorisága (7,3%), a kimutatására szolgáló pooling alkalmazása 62%-os gazdasági megtakarítást tenne lehetővé, a biztonság jelentős csökkenése nélkül (14). Spanyolországban, amely a HBV-fertőzés szempontjából alacsony endémiájú területhez tartozik, és ahol a HBsAg-hordozók gyakorisága az általános népességben 1,2% (4), az összes olyan csoportban alkalmazható, ahol a HBsAg-szűrés jelenleg kötelező (például véradók, autotranszfúziós programban részt vevő személyek, terhes nők szűrése).
A krónikus HBV-hordozók kimutatására szolgáló technikák alkalmazásának költség-haszon vizsgálata lehetővé teszi annak kimutatását, hogy a gazdasági megtakarítás nagyobb, ha nagyszámú meghatározás történik alacsony szeroprevalenciájú csoportokban, és alkalmazása költséghatékony lehet a fertőzés magas prevalenciájával rendelkező területeken is, sőt még a kisszámú meghatározást végző laboratóriumokban is. Kimutattuk a gazdasági költségmegtakarítást mind a különböző HBsAg-prevalenciák, mind az évente elvégzendő vizsgálatok száma szerint. A mi területünkön a pooling módszer alkalmazásával a teljes gazdasági költség mintegy 74%-át lehetett megtakarítani az egyedi módszerhez képest.
Néhány kutató a közelmúltban kezdte el gyakorolni a vírusnukleinsavak véradókban polimeráz láncreakció (PCR) segítségével történő kimutatására irányuló stratégiákat a vérkészítmények transzfúziójával járó biztonság növelése érdekében (26-29). Mivel a gazdasági problémák és az ezzel járó munka mennyisége miatt nem lehet egyéni szűrővizsgálatokat végezni, jelenleg a szerológiailag negatív vérminták összevonásának módszerét alkalmazzák. Ez az eljárás a véradások szisztematikus szűrése révén viszonylag alacsony költséggel növelheti a vérbiztonságot. Mivel e módszerek gyakorlásának egyik fő korlátja a gazdaságosság, úgy gondoljuk, hogy tanulmányunkkal elméleti alapja lehet annak, hogy a HBV-, HCV- és HIV-fertőzések szűrését két lépcsőben, viszonylag alacsony gazdasági költséggel végezzük. Az első fázisban egy kereskedelmi forgalomban kapható EIA-t lehetne alkalmazni a donorszérumok egy csoportjára; a második fázisban a PCR-technikák alkalmazása a szeronegatív minták egy csoportjára növelhetné az elemzés biztonságát. Amíg a jövőbeni vizsgálatok nem tudják bizonyítani ennek a technikának az értékét véradókon, úgy gondoljuk, hogy ez csak diagnosztikai és járványügyi vizsgálatokra alkalmazható.
Arra a következtetésre jutottunk, hogy az EIA alkalmazása összevont szérumokon érzékeny és specifikus módszer a két fő HBsAg altípus kimutatására egy alacsony szeroprevalenciájú területen. Az érzékenység csak akkor csökken, ha az összevont szérumokban nagyon magas anti-HBs-titerek vannak. Az összevonási technika olyan módszer, amely pénzügyi megtakarítást is lehetővé tehet, ha olyan populációk vizsgálatában alkalmazzák, ahol a HBsAg-hordozók előfordulási gyakorisága magas. Úgy véljük, hogy további vizsgálatok szükségesek ezen eredmények megerősítéséhez.
Köszönet
Megköszönjük David H. Wallace-nak (a European Association of Science Editors és a Council of Biological Editors tagja) a kézirat angol nyelvű fordítását.
1. Maynard JE. Hepatitis B: globális jelentőség és az ellenőrzés szükségessége. Vaccine 1990; 8 (Supl.): 18s-20s.
2. Margolis HS, Alter MJ, Hadler SC. Hepatitis B: fejlődő epidemiológia és a védekezés következményei. Sem Liver Dis 1991; 11: 84-92.
3. Alter MJ, Mast EE. A vírusos hepatitis epidemiológiája az Egyesült Államokban. Gastroenterol Clin North Am 1994; 23: 437-55.
4. Suárez A, Riestra S, Navascués CA, et al. Pozitív HBsAg véradók Asztúriában (Spanyolország): jelenlegi prevalencia és jelentősége. (angol nyelvű absztrakt). Med Clin (Barcelona) 1994; 102: 329-32.
5. Emmanuel JC, Basset MT, Smith HJ, Jacobs JA. Szérumok összevonása humán immundeficiencia vírus (HIV) vizsgálatához: gazdaságos módszer a fejlődő országokban történő felhasználásra. J Clin Pathol 1988; 41: 582-5.
6. Kline RL, Brothers TA, Brookmeyer R, et al. Evaluation of human immunodeficiency virus seroprevalence in population surveys using pooled sera. J Clin Microbiol 1989; 27: 1449-52.
7. Cahoon-Young B, Chandler A, Livermore T, et al. Sensitivity and specificity of pooled versus individual sera in a human immunodeficiency virus antibody prevalence study. J Clin Microbiol 1989; 27: 1893-5.
8. Frosner GG, Dobler G, von Sonnenburg FJ. A HIV-ellenes antitestek nem kapcsolt vizsgálatának költségcsökkentése összevont szérumok vizsgálatával. AIDS 1990; 4: 73-5.
9. Behets F, Bertozzi S, Kasali M, et al. Az összevont szérumok sikeres alkalmazása a HIV-1 szeroprevalencia meghatározására Zaire-ben, költséghatékonysági modellek kidolgozásával. AIDS 1990; 4: 737-41.
10. Monzon OT, Paladin FJ, Dimaandal E, et al. Az antitesttartalom és a tesztformátum jelentősége az összevont szérumok HIV-vizsgálatában. AIDS 1992; 6: 43-8.
11. Tamashiro H, Maskill W, Emmanuel J, et al. A HIV-antitestek vizsgálatának költségcsökkentése. Lancet 1993; 342: 87-90.
12. Perriens JH, Magazani K, Kapila N, et al. Gyorsteszt és ELISA használata összevont szérumminták HIV-antitest-szűrésére Lubumbashiban, Zaire-ben. J Virol Methods 1993; 41: 213-21.
13. McMahon EJ, Fang C, Layug L, Sandler SG. Véradó vérminták összevonása a HIV-1 antitestvizsgálat költségeinek csökkentése érdekében. Vox Sang 1995; 68: 215-9.
14. Verstraeten T, Farah B, Duchateau L, Matu R. Pooling sera to reduce the cost of HIV surveillance: a feasibility study in a rural Kenyan district. Trop Med Int Health 1998; 3: 747-50.
15. Kamel MA, Ghaffar YA, Wasef MA, et al. High HCV prevalence in Egyptian blood donors. Lancet 1992; 340: 427.
16. Neil AGS, Conradie JD. A véradók alacsony költségű HCV-ellenes szűrése. Lancet 1992; 340: 1096.
17. Fernández E, Riestra S, García S, Rodríguez S. Pool tesztek a hepatitis C vírusfertőzés kimutatására. J Hepatol 1995; 23: 236.
18. García Z, Taylor L, Ruano A, et al. A véradók rutinszerű anti-HCV-szűrésének pooling módszerének értékelése a vérbankok költségterheinek csökkentése érdekében a fejlesztés alatt álló országokban. J Med Virol 1996; 49: 218-22.
19. Liu P, Shi ZX, Zhang YC, et al. A prospektív vizsgálat a szérum-pooling stratégiáról a véradók hepatitis C vírus elleni antitestek szűrésében. Transfusion 1997; 37: 732-6.
20. Cunningham R, Northwood JL, Kelly CD, et al. Hepatitis B rutinszerű antenatalis szűrése összevont szérumokkal: validálás és 10 év tapasztalatainak áttekintése. J Clin Pathol 1998; 51: 392-5.
21. Rabenau H, Schutz R, Berger A, et al. How accurate is serologic testing of plasma pools for hepatitis B virus surface antigen, anti-human immunodeficiency virus 1 and 2, and anti-hepatitis C virus? (angol nyelvű összefoglaló). Infus Transfus 1996; 23: 124-30.
22. Echevarría JE, León P, López JA, et al. HBsAg altípusok eloszlása a HBsAg-hordozók különböző populációi között Spanyolországban. Eur J Epidemiol 1995; 11: 39-45.
23. Neill AGS, Conradie JD. A hepatitis C-vírus pool-tesztjei. Lancet 1994; 343: 738.
24. Liu P, Shi ZX, Zhang YC, Zhang XY. Összehasonlító tanulmány 4 EIA-készletről a hepatitis C-vírus elleni antitest szűrésére összevont szérumokban. Biomed Environ Sci 1998; 11: 75-80.
25. Ajánlások a HIV-antitestek vizsgálatára szérumpoolban. WHO Weekly Epidemiol Rec 1991; 44: 316-27.
26. Lefrere JJ, Coste J, Defer C, et al. Véradományok szűrése vírusgenomokra: multicentrikus tanulmány az összevont mintákon végzett valós idejű szimulációról a hepatitis C vírus RNS kimutatásának modelljén. Transfusion 1998; 38: 915-23.
27. Yerly S, Pedrocchi M, Perrin L. A polimeráz láncreakció alkalmazása plazmapoolokban a hepatitis C vírus és a HIV 1-es típusú RNS egyidejű kimutatására. Transfusion 1998; 38: 908-14.
28. Schottstedt V, Tuma W, Bunger G, Lefevre H. PCR a HBV, HCV és HIV-1 kimutatására egy nagy vérátömlesztő szolgálat rutinszerű szűrőprogramjának tapasztalatai és első eredményei. Biologicals 1998; 26: 101-4.
29. Morandi PA, Schockmel GA, Yerly S, et al. Az 1-es típusú humán immundeficiencia vírus (HIV-1) RNS kimutatása HIV-1 és HIV-2 antitestekre negatív szérumokból álló poolokban. J Clin Microbiol 1998; 36: 1534-8.
Vélemény, hozzászólás?