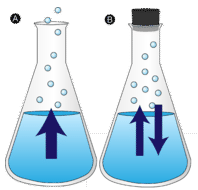
Párolgás
Az érintetlenül hagyott víztócsa végül eltűnik. A folyadékmolekulák a gázfázisba lépve vízgőzzé válnak. A párolgás az a folyamat, amelynek során egy folyadék gázzá alakul. A párolgás egy folyadéknak a folyadék forráshőmérséklete alatti gőzzé alakulása. Ha a vizet ehelyett egy zárt tartályban tartjuk, a vízgőzmolekuláknak nincs esélyük a környezetbe távozni, így a vízszint nem változik. Ahogy néhány vízmolekula gőzzé válik, ugyanennyi vízgőzmolekula visszasűrűsödik a folyékony állapotba. A kondenzáció a gázból folyadékba történő állapotváltozás.
Hogy egy folyadékmolekula gázállapotba léphessen, a molekulának elegendő mozgási energiával kell rendelkeznie ahhoz, hogy legyőzze a folyadékban lévő molekulák közötti vonzóerőket. Emlékezzünk vissza, hogy egy adott folyadékmintában sokféle kinetikus energiájú molekula található. Azok a folyadékmolekulák, amelyek rendelkeznek ezzel a bizonyos küszöb kinetikus energiával, kiszabadulnak a felületről, és gőzzé válnak. Ennek eredményeképpen a megmaradó folyadékmolekuláknak már kisebb a kinetikus energiájuk. A párolgás során a megmaradó folyadék hőmérséklete csökken. Megfigyelted a párolgó hűtés hatásait. Egy forró napon az izzadságodban lévő vízmolekulák elnyelik a testhőt, és elpárolognak a bőröd felületéről. A párolgás következtében a megmaradt izzadság hűvösebb marad, ami viszont több hőt vesz fel a testedből.
Egy adott folyadék gyorsabban párolog, ha felmelegszik. Ez azért van így, mert a melegítés hatására a folyadék molekuláinak nagyobb hányada rendelkezik a folyadék felszínéről való kilépéshez szükséges mozgási energiával. Az alábbi ábra a folyadékmolekulák mozgási energiájának eloszlását mutatja két hőmérsékleten. Az elpárolgáshoz szükséges mozgási energiával rendelkező molekulák számát a jobb oldali görbe alatti árnyékolt terület mutatja. A magasabb hőmérsékletű folyadékban \(\balra( T_2 \jobbra)\) több olyan molekula van, amely képes a gőzfázisba távozni, mint az alacsonyabb hőmérsékletű folyadékban \(\balra( T_1 \jobbra)\).
Vélemény, hozzászólás?