|
|
Tento článek má více problémů. Pomozte jej prosím vylepšit nebo diskutujte o těchto problémech na diskusní stránce. (Naučte se, jak a kdy odstranit tyto šablony)
(Naučte se, jak a kdy odstranit tuto zprávu ze šablony) |
Monosacharidy (z řeckého monos: jediný, sachar: cukr), nazývané také jednoduché cukry, jsou nejjednodušší formou cukru a nejzákladnějšími jednotkami (monomery) sacharidů. Obecný vzorec je C
nH
2nO
n, i když ne všechny molekuly odpovídající tomuto vzorci (např. kyselina octová) jsou sacharidy. Jsou to obvykle bezbarvé, ve vodě rozpustné a krystalické pevné látky. V rozporu se svým názvem (cukry) mají pouze některé monosacharidy sladkou chuť.
Příkladem monosacharidů jsou glukóza (dextróza), fruktóza (levulóza) a galaktóza. Monosacharidy jsou stavebními kameny disacharidů (např. sacharózy a laktózy) a polysacharidů (např. celulózy a škrobu). Každý atom uhlíku, který podporuje hydroxylovou skupinu, je chirální, s výjimkou těch na konci řetězce. Vzniká tak řada izomerních forem, které mají stejný chemický vzorec. Například galaktóza a glukóza jsou obě aldohexózy, ale mají odlišnou fyzikální strukturu a chemické vlastnosti.
Monosacharid glukóza hraje klíčovou roli v metabolismu, kde se prostřednictvím glykolýzy a cyklu kyseliny citronové získává chemická energie, která poskytuje energii živým organismům. Některé další monosacharidy mohou být v živém organismu přeměněny na glukosu.
Struktura a názvosloví
Až na několik výjimek (např. deoxyribosa) mají monosacharidy tento chemický vzorec: (CH2O)x, kde x ≥ 3. Monosacharidy lze klasifikovat podle počtu x atomů uhlíku, které obsahují: trióza (3), tetróza (4), pentóza (5), hexóza (6), heptóza (7) atd.
Glukóza, která se používá jako zdroj energie a pro syntézu škrobu, glykogenu a celulózy, je hexóza. Ribóza a deoxyribóza (v RNA, resp. DNA) jsou pentózové cukry. Příkladem heptóz jsou ketózy, mannoheptulóza a sedoheptulóza. Monosacharidy s osmi a více uhlíky se vyskytují zřídka, protože jsou poměrně nestabilní. Ve vodných roztocích existují monosacharidy jako kruhy, pokud mají více než čtyři uhlíky.
Monosacharidy s lineárním řetězcem
Jednoduché monosacharidy mají lineární a nerozvětvený uhlíkový skelet s jednou karbonylovou (C=O) funkční skupinou a jednou hydroxylovou (OH) skupinou na každém ze zbývajících atomů uhlíku. Proto lze molekulární strukturu jednoduchého monosacharidu zapsat jako H(CHOH)n(C=O)(CHOH)mH, kde n + 1 + m = x; takže jeho elementární vzorec je CxH2xOx.
Podle konvence jsou atomy uhlíku číslovány od 1 do x podél páteře, počínaje koncem, který je nejblíže skupině C=O. Monosacharidy jsou nejjednoduššími jednotkami sacharidů a nejjednodušší formou cukru.
Pokud je karbonyl v poloze 1 (tj. n nebo m je nula), molekula začíná formylovou skupinou H(C=O)- a technicky se jedná o aldehyd. V takovém případě se sloučenina označuje jako aldóza. V opačném případě má molekula mezi dvěma uhlíky keto skupinu, karbonyl -(C=O)-; pak se formálně jedná o keton a označuje se jako ketóza. Biologicky zajímavé ketózy mají obvykle karbonyl v poloze 2.
Různé výše uvedené klasifikace lze kombinovat, což vede k názvům jako „aldohexóza“ a „ketotrióza“.
Obecnější nomenklatura pro monosacharidy s otevřeným řetězcem kombinuje řeckou předponu označující počet uhlíků (tri-, tetr-, pent-, hex- atd.) s příponami „-osa“ pro aldosy a „-ulosa“ pro ketosy. V druhém případě, pokud se karbonyl nenachází v poloze 2, je jeho poloha označena číselným infixem. Tak například H(C=O)(CHOH)4H je pentóza, H(CHOH)(C=O)(CHOH)3H je pentulóza a H(CHOH)2(C=O)(CHOH)2H je pent-3-ulóza.
Stereoizomery s otevřeným řetězcem
Dva monosacharidy s ekvivalentními molekulovými grafy (stejná délka řetězce a stejná poloha karbonylu) mohou být přesto odlišnými stereoizomery, jejichž molekuly se liší prostorovou orientací. K tomu dochází pouze v případě, že molekula obsahuje stereogenní centrum, konkrétně atom uhlíku, který je chirální (spojený se čtyřmi různými molekulovými substrukturami). Tyto čtyři vazby mohou mít v prostoru libovolnou ze dvou konfigurací, které se liší ručičkovitostí. V jednoduchém monosacharidu s otevřeným řetězcem je chirální každý uhlík kromě prvního a posledního atomu řetězce a (u ketos) uhlíku s keto skupinou.
Například triketosa H(CHOH)(C=O)(CHOH)H (glyceron, dihydroxyaceton) nemá stereogenní centrum, a proto existuje jako jediný stereoizomer. Jiná trióza, aldóza H(C=O)(CHOH)2H (glyceraldehyd), má jeden chirální uhlík – centrální, číslo 2 – který je vázán na skupiny -H, -OH, -C(OH)H2 a -(C=O)H. Proto existuje jako dva stereoizomery, jejichž molekuly jsou navzájem zrcadlovými obrazy (jako levá a pravá rukavice). Monosacharidy se čtyřmi a více uhlíky mohou obsahovat více chirálních uhlíků, takže obvykle mají více než dva stereoizomery. Počet různých stereoizomerů se stejným diagramem je omezen číslem 2c, kde c je celkový počet chirálních uhlíků.
Fischerova projekce je systematický způsob kreslení kosterního vzorce acyklického monosacharidu tak, aby byla dobře specifikována ručičkovitost každého chirálního uhlíku. Každý stereoizomer jednoduchého monosacharidu s otevřeným řetězcem lze identifikovat podle polohy (vpravo nebo vlevo) chirálních hydroxylů (hydroxyly připojené k chirálním uhlíkům) ve Fischerově diagramu.
Většina stereoizomerů je sama o sobě chirální (liší se od svých zrcadlových obrazů). Ve Fischerově projekci se dva zrcadlové izomery liší tím, že mají polohy všech chirálních hydroxylů obrácené zprava doleva. Zrcadlové izomery jsou chemicky identické v nechirálním prostředí, ale obvykle mají velmi odlišné biochemické vlastnosti a výskyt v přírodě.
Ačkoli většinu stereoizomerů lze uspořádat do dvojic zrcadlových obrazů, existují některé nechirální stereoizomery, které jsou identické se svými zrcadlovými obrazy, přestože mají chirální centra. K tomu dochází vždy, když je molekulový graf symetrický, jako v případě 3-ketopentózy H(CHOH)2(CO)(CHOH)2H, a obě poloviny jsou navzájem zrcadlovými obrazy. V takovém případě je zrcadlení ekvivalentní otočení o polovinu. Z tohoto důvodu existují pouze tři odlišné stereoizomery 3-ketopentosy, přestože molekula má dva chirální uhlíky.
Odlišné stereoizomery, které nejsou navzájem zrcadlovými obrazy, mají obvykle odlišné chemické vlastnosti, a to i v nechirálním prostředí. Proto může mít každý zrcadlový pár a každý nechirální stereoizomer specifický název monosacharidu. Například existuje 16 různých stereoizomerů aldohexosy, ale název „glukosa“ znamená konkrétní dvojici zrcadlových obrazů aldohexosy. Ve Fischerově projekci má jeden ze dvou izomerů glukózy hydroxyl vlevo na C3 a vpravo na C4 a C5, zatímco druhý izomer má obrácený vzorec. Tyto specifické názvy monosacharidů mají konvenční třípísmenné zkratky, například „Glu“ pro glukosu a „Thr“ pro threosu.
Obecně má monosacharid s n asymetrickými uhlíky 2n stereoizomerů. Počet stereoizomerů otevřeného řetězce je u monosacharidu aldózy o jedna větší než u monosacharidu ketózy stejné délky. Každá ketóza bude mít 2(n-3) stereoizomerů, kde n > 2 je počet uhlíků. Každá aldóza bude mít 2(n-2) stereoizomerů, kde n > 2 je počet uhlíků. tyto se také označují jako epimery, které mají různé uspořádání skupin -OH a -H na asymetrických nebo chirálních atomech uhlíku (to neplatí pro ty uhlíky, které mají karbonylovou funkční skupinu).
Konfigurace monosacharidů
Stejně jako mnoho chirálních molekul, i dva stereoizomery glyceraldehydu při průchodu lineárně polarizovaným světlem postupně otáčejí směr jeho polarizace, a to i v roztoku. Oba stereoizomery se označují předponami D- a L- podle smyslu rotace: D-glyceraldehyd je dextrorotační (otáčí osu polarizace ve směru hodinových ručiček), zatímco L-glyceraldehyd je levorotační (otáčí ji proti směru hodinových ručiček).

Předpony D- a L se používají také u jiných monosacharidů, aby se odlišily dva konkrétní stereoizomery, které jsou navzájem zrcadlovými obrazy. Pro tento účel se uvažuje chirální uhlík, který je nejvíce vzdálen od skupiny C=O. Jeho čtyři vazby se musí spojit s -H, -OH, -C(OH)H a zbytkem molekuly. Pokud lze molekulu otočit v prostoru tak, aby směry těchto čtyř skupin odpovídaly směrům analogických skupin v D-glyceraldehydu C2, pak isomer obdrží předponu D-. V opačném případě obdrží předponu L-.
Ve Fischerově projekci předpony D- a L- určují konfiguraci na atomu uhlíku, který je druhý zdola: D-, pokud je hydroxyl na pravé straně, a L-, pokud je na levé straně.
Všimněte si, že předpony D- a L- neoznačují směr otáčení polarizovaného světla, což je kombinovaný efekt uspořádání ve všech chirálních centrech. Oba enantiomery však budou vždy otáčet světlo v opačných směrech, a to o stejnou hodnotu. Viz také systém D/L.
Cyklizace monosacharidů
Monosacharid často přechází z acyklické formy (otevřeného řetězce) na cyklickou formu, a to nukleofilní adiční reakcí mezi karbonylovou skupinou a jedním z hydroxylů téže molekuly. Reakcí vzniká kruh z atomů uhlíku uzavřený jedním přemosťujícím atomem kyslíku. Výsledná molekula má hemiacetalovou nebo hemiketalovou skupinu, podle toho, zda lineární forma byla aldosa nebo ketosa. Reakci lze snadno zvrátit a získat původní formu s otevřeným řetězcem.
V těchto cyklických formách má kruh obvykle pět nebo šest atomů. Tyto formy se nazývají furanosy, respektive pyranosy – analogicky k furanu a pyranu, nejjednodušším sloučeninám se stejným kruhem uhlíku a kyslíku (ačkoli postrádají dvojné vazby těchto dvou molekul). Například aldohexosa glukosa může tvořit hemiacetalovou vazbu mezi hydroxylem na uhlíku 1 a kyslíkem na uhlíku 4, čímž vzniká molekula s pětičlenným kruhem, nazývaná glukofuranosa. Stejná reakce může proběhnout mezi uhlíky 1 a 5 za vzniku molekuly se šestičlenným kruhem, nazývané glukopyranosa. Cyklické formy se sedmiatomovým kruhem (stejným jako u oxepanu), které se vyskytují zřídka, se nazývají heptózy.


.

Pro mnoho monosacharidů (včetně glukózy), v pevném stavu i v roztocích převažují cyklické formy, a proto se pro izomery s otevřeným i uzavřeným řetězcem běžně používá stejný název. Tak například termín „glukosa“ může označovat glukofuranosu, glukopyranosu, formu s otevřeným řetězcem nebo směs těchto tří forem.
Cyklizací vzniká nové stereogenní centrum na uhlíku nesoucím karbonyl. Skupina -OH, která nahrazuje kyslík karbonylu, může skončit ve dvou různých polohách vzhledem ke středové rovině kruhu. Každý monosacharid s otevřeným řetězcem tak poskytuje dva cyklické izomery (anomery), označované předponami α- a β-. Molekula může mezi těmito dvěma formami přecházet procesem zvaným mutarotace, který spočívá v obrácení reakce tvorby kruhu a následné tvorbě dalšího kruhu.
Haworthova projekce
Streochemickou strukturu cyklického monosacharidu lze znázornit v Haworthově projekci. V tomto diagramu má α-izomer pro pyranosovou formu D-aldohexosy -OH anomerního uhlíku pod rovinou atomů uhlíku, zatímco β-izomer má -OH anomerního uhlíku nad rovinou. Pyranosy obvykle zaujímají křesadlovou konformaci podobnou konformaci cyklohexanu. V této konformaci má α-izomer -OH anomerního uhlíku v axiální poloze, zatímco β-izomer má -OH anomerního uhlíku v ekvatoriální poloze (s ohledem na D-aldohexosové cukry).
-
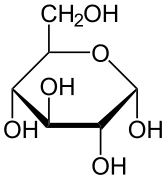
α-D-glukopyranosa
-

β-D-glukopyranóza
Deriváty
Existuje velké množství biologicky významných modifikovaných monosacharidů:
- Aminocukry, jako jsou:
- galaktosamin
- glukosamin
- kyselina sialová
- N-acetylglukosamin
- Sulfocukry, jako např:
- sulfoquinovose
- Další, jako např:
- kyselina askorbová
- mannitol
- kyselina glukuronová
Viz také
- Monosacharidová nomenklatura
- Redukční cukr
- Cukrová kyselina
- Cukrový alkohol
- Disacharid
.
Poznámky
- ^ „Sacharidy“. Chemie pro biology. Královská chemická společnost. Získáno 10. března 2017.
- ^ NCERT TEXT BOOK CLaSS-12
- ^ „Carbohydrates“ (Sacharidy). Chemie pro biology. Královská chemická společnost. Staženo 10. března 2017.
- ^ Pigman, William Ward; Anet, E. F. L. J. (1972). „Chapter 4: Mutarotations and Actions of Acids and Bases“ (Kapitola 4: Mutace a působení kyselin a zásad). In Pigman and Horton (ed.). The Carbohydrates: Chemistry and Biochemistry. 1A (2. vyd.). San Diego: Academic Press. s. 165-194.
- ^ IUPAC, Compendium of Chemical Terminology, 2. vyd. („Zlatá kniha“) (1997). Online opravená verze: (2006-) „Haworth representation“. doi:10.1351/goldbook.H02749
.


Napsat komentář