Introduktion
Lungemboli (PE) är en vanlig sjukdom med en årlig incidens på 110 fall per 100 000 vuxna,1 som har ökat under de senaste åren.1,2 Symtomen kan variera, från symtomlösa till obstruktiv chock efter cirkulationskollaps.3 Den totala mortaliteten är inte bara hög, utan varierar också kraftigt. I en nyligen genomförd studie var den totala dödligheten 8,65 % efter tre månader.4 Centrala artärer är oftast involverade,5,6 medan subsegmentell PE står för 4-7 % av fallen.7-9 Ett antal studier rapporterar dock om subsegmentell involvering hos upp till 30 % av patienterna.9
Den kliniska relevansen av omfattningen av PE är fortfarande omdiskuterad, och antikoagulationens roll hos patienter med subsegmentell involvering har ifrågasatts i ett antal studier.10,11
Syftet med vår studie var att beskriva de kliniska särdragen hos patienter med PE på vårt sjukhus och att analysera deras prognos baserat på sjukdomens utbredning.
Metoder
Vi genomförde en retrospektiv studie av alla patienter över 18 år med bekräftad CT-bröstskiktsdiagnos av PE12 vid sjukhuskomplexet i Pontevedra i Spanien mellan januari 2005 och december 2010. Uppföljningen avslutades den 31 januari 2012, överlevnadsgränsen. Den minsta uppföljningen var således 14 månader. Administrativa uppgifter från kodade sjukhusutskrivningar användes för patienturvalet. De patienter med ofullständiga uppgifter och/eller diagnoser som ställdes med andra metoder än CT-scanning av bröstkorgen uteslöts från det ursprungliga urvalet på 470 patienter. Således ingick 313 fall i studien.
Följande uppgifter analyserades:
-
Personuppgifter: ålder, kön, aktiv rökning och fetma (kroppsmasseindex >30).
-
Kliniska uppgifter, uppgifter om fysisk undersökning och ytterligare test: nyligen genomförd operation, anestesi, trauma, cancer, långvarig resa och/eller immobilisering; förlamning av nedre extremiteter; insättning av central kateter, trombofili eller antifosfolipidsyndrom; tidigare venös tromboembolisk sjukdom (VTE); åderbråck i nedre extremiteterna; graviditet, preventivmedel eller hormonbehandling. Takypné, crepitant rale, tecken på DVT i nedre extremiteter; vitala tecken, systolisk hypotoni (SBP
100mmHg), diastolisk hypotoni (DBP60mmHg) och takykardi (hjärtfrekvens>100).13,14 Arteriella blodgasanalyser, hemoglobin, hematokrit, trombocytantal, leukocytos, neutrofili, glukos, urea, kreatinin, natrium, kalium och fibrinogen, stratifierade som normala eller onormala enligt laboratoriereferensvärdena på vårt sjukhus. D-dimernivåerna bestämdes med högkänslig turbidimetrisk immunoassay. D-dimernivåer över 500ng/ml betraktades som patologiska. Njurfunktionen ansågs vara normal om den glomerulära filtrationshastigheten enligt den förkortade MDRD-ekvationen var högre än 60 ml/min/1,73 m2.15 Elektrokardiografiska och bilddiografiska fynd: vanlig lungröntgen, ekodoppler i de nedre extremiteterna (fullständig eller distal) utfördes enligt radiologens bedömning, baserat på patientens kliniska presentation. PE samlades in och klassificerades i tre grupper med hjälp av CT-skanning av bröstkorgen: centrala (huvudstam, höger eller vänster lungartär, intermediära artärer eller lobära artärer), segmentala och subsegmentala. Trombosens läge bestämdes enligt den största involverade artären. Komorbiditet mätt med Charlson-index (CCI), kategoriserat i ”0”, ”1-2” och ”≥3”.16
Klinisk sannolikhet bestämdes med Wells17- och Geneva18-poäng.
Dödsorsaken tillskrevs av huvudundersökaren baserat på tillgängliga journaler och kategoriserades i tre grupper: PE-relaterad, PE-orelaterad och okänd. Diskrepans mellan data och osäkra slutdiagnoser löstes genom diskussion med datainsamlare.
Statistisk analys
Kategoriska variabeldata presenteras som frekvenser (procent); kontinuerliga variabeldata presenteras som medianer och interkvartilintervall.
Fishers exakta och Chi-kvadrat-test användes för att jämföra kategoriska variabler. Mellan grupper jämfördes kontinuerliga variabler med ANOVA eller Kruskal-Wallis-testet vid icke-normala fördelningar.
Överlevnadskurvor och ökningar av sannolikheten för dödsfall beräknades respektive med Kaplan-Meier-testet och Cox-regression. Skillnader ansågs vara signifikanta vid p
0,05. Data analyserades med SPSS 15 för Windows. resultat
Studien omfattade 313 PE-patienter. 56 % var kvinnor och medianåldern var 70 år (interkvartilintervall 53-78 år). Central PE stod för 68 % av fallen; segmentell och subsegmentell PE, för 25 % och 7 %. Patienter med subsegmentell PE var yngre, hade lägre komorbiditet och ingen av dem hade proximal DVT (tabell 1). Patienterna i gruppen med subsegmentell PE omfattade 10 (45 %) med enkel PE och 12 (55 %) med multipel PE.
När det gäller symtom är dyspné det vanligaste hos patienter med central PE, och även smärta är vanligt förekommande vid segmentell och subsegmentell PE (tabell 1). Komorbiditet mätt med CCI förekom i 78 % av fallen och var vanligare vid central PE (tabell 1). 22 % av patienterna hade diagnostiserats med cancer före PE (data visas inte). När det gäller förekomsten av riskfaktorer och den kliniska sannolikheten för PE enligt Wells och Geneva-poängen hittades inga skillnader när det gäller sjukdomens omfattning (tabell 1). När det gäller de ytterligare testerna uppvisade patienter med involvering av centrala artärer signifikant högre D-dimervärden och presterade sämre vid blodgasanalyser. Ingen signifikant skillnad hittades för någon av de övriga parametrarna (tabell 2). Alla patienter togs in på sjukhus och behandlades med antikoagulantia.
Den 30-dagars mortaliteten var 7 %, hänförlig till PE i 3,5 % av fallen. Patienter med subsegmentell PE uppvisade signifikant högre överlevnadsfrekvens både efter 30 dagar och i slutet av uppföljningen (fig. 1). Ingen skillnad observerades i dödsorsak baserat på omfattningen av PE (fig. 2). Faktorer som var oberoende relaterade till en högre sannolikhet för dödlighet var cancerdiagnos och högre komorbiditet mätt med Charlson-index (tabell 3).
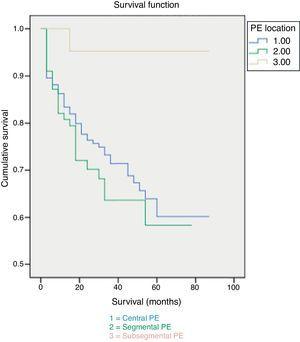
Allmän överlevnad och utbredning av PE.

Dödsorsaker och utvidgning av PE.
Förutsägelser för dödlighet. Multivariat analys.
| Faktorer | OR | CI 95% |
|---|---|---|
| PE location | ||
| Central | 1 | |
| Segmental | 1.28 | 0,79-2,09 |
| Subsegmental | 0,29 | 0,03-2.23 |
| Cancer | ||
| Nej | 1 | |
| Ja | 3.72 | 2.30-6.03 |
| Charlson | ||
| 0 | 1 | |
| 1-2 | 2.81 | 0.82-9.59 |
| ≥3 | 8.61 | 2.58-28,69 |
Ajusterat för ålder, kön, njurfunktion och blodgasparametrar.
Diskussion
Frekvensen av subsegmentell PE var 7 %, vilket är likvärdigt med det som rapporterats av andra författare.5 Ingen signifikant könsskillnad hittades när det gäller sjukdomens omfattning; andelen kvinnor är dock något högre i vårt urval. Åldern hos patienter med subsegmentell PE var lägre än hos patienter med central och segmentell PE. Skillnaden kan vara relaterad till hyperkoagulation och de förändringar i det vaskulära endotelet som följer med åldrandet19: dessa skulle kunna underlätta omfattningen av tromber hos äldre patienter, särskilt med tanke på att ingen åldersskillnad hittades när det gäller förekomsten av riskfaktorer för PE.
Men även om symtomen på PE är ospecifika och presentationen vanligen är likartad hos vuxna fann vi bröstsmärta hos yngre patienter och ett positivt samband mellan ålder och dyspné.19 I vår studie rapporterades oftast bröstsmärta hos yngre patienter med perifer PE och dyspné hos äldre patienter med central PE och högre nivåer av hypoxi. I allmänhet förekom dyspné mindre ofta hos patienter med subsegmentell PE.10 Dessa presterade bättre vid blodgasanalys och hade en totalt sett mindre allvarlig klinisk presentation,20 inklusive lägre proximal DVT.5,10
D-dimernivåerna hos patienter med PE tycks vara förknippade med trombusstorlek, är relaterade till PE:s allvarlighetsgrad och har ett värde som prognostisk markör.21 Vi fann lägre serumnivåer hos patienter med subsegmentell PE, som hade en mer godartad klinisk presentation och ett bättre resultat på medellång sikt. D-dimertestning utfördes dock endast i 30 % av fallen. Våra resultat är således inte entydiga.
I vår studie var 30-dagarsdödligheten högre än i andra studier,22 även om andelen PE-relaterade dödsfall var liknande.4 Ingen av patienterna avled till följd av subsegmentell PE. Skillnader i mortalitet kan bero på olika orsaker: Medelåldern hos våra patienter är högre, många har medföljande kroniska sjukdomar som kan betingas av det dåliga utfallet av PE, och antalet dödsfall på grund av komorbiditet är också högt. Faktum är att den viktigaste bestämmande faktorn för dödlighet är komorbiditet, särskilt cancer. Patienter med cancer och PE har inte bara en dålig prognos, utan även en sämre prognos än patienter med enbart cancer eller PE.23 Symtom på PE kan förväxlas med symtom på exacerbationer av tidigare hjärt- och lungsjukdomar,24 vilket leder till försenad diagnos och behandling, sämre prognos och högre dödlighet. Äldre patienter är mer komplexa och kan ha högre komorbiditet och fördröjd diagnos24; komorbiditet har också föreslagits som en riskfaktor för PE hos dessa patienter.25,26
Den kliniska betydelsen av subsegmentell PE är okänd. Den kan dock ha klinisk relevans och långsiktiga konsekvenser hos patienter med låg kardiopulmonell reserv.2 Den har vanligtvis låg mortalitet2,27 och en god prognos.5,28 Ett antal författare har därför föreslagit att vissa patienter inte skulle behöva antikoagulantiabehandling.29,30
Våra data tyder på att patienter med subsegmentell PE kliniskt skiljer sig i hög grad från patienter med mer proximal PE. Prognosen påverkas av förekomsten av medföljande störningar snarare än av sjukdomens omfattning.
Etiska upplysningarSkydd av människor och djur
Författarna förklarar att de förfaranden som följdes var i enlighet med bestämmelserna i den relevanta etiska kommittén för klinisk forskning och med bestämmelserna i Världsmedicinska föreningens etiska kod (Helsingforsdeklarationen).
Dataintegritet
Författarna förklarar att de har följt sitt arbetscentrums protokoll om offentliggörande av patientuppgifter och att alla patienter som ingick i studien fick tillräcklig information och gav sitt skriftliga informerade samtycke till att delta i studien.
Rätt till personlig integritet och informerat samtycke.
Lämna ett svar