|
|
Denna artikel har flera problem. Hjälp till att förbättra den eller diskutera dessa problem på diskussionssidan. (Lär dig hur och när du tar bort dessa mallmeddelanden)
(Lär dig hur och när du tar bort det här mallmeddelandet) |
Monosackarider (från grekiskans monos: enstaka, sacchar: socker), även kallade enkla sockerarter, är den enklaste formen av socker och de mest grundläggande enheterna (monomerer) bland kolhydrater. Den allmänna formeln är C
nH
2nO
n, även om inte alla molekyler med denna formel (t.ex. ättiksyra) är kolhydrater. De är vanligtvis färglösa, vattenlösliga och kristallina fasta ämnen. I motsats till deras namn (sockerarter) är det bara vissa monosackarider som har en söt smak.
Exempel på monosackarider är glukos (druvsocker), fruktos (levulos) och galaktos. Monosackarider är byggstenarna i disackarider (t.ex. sackaros och laktos) och polysackarider (t.ex. cellulosa och stärkelse). Varje kolatom som bär en hydroxylgrupp är chiral, utom de i slutet av kedjan. Detta ger upphov till ett antal isomera former, alla med samma kemiska formel. Till exempel är galaktos och glukos båda aldohexoser, men har olika fysiska strukturer och kemiska egenskaper.
Monosackariden glukos spelar en central roll i ämnesomsättningen, där den kemiska energin utvinns genom glykolysen och citronsyracykeln för att ge energi till levande organismer. Vissa andra monosackarider kan i den levande organismen omvandlas till glukos.
Struktur och nomenklatur
Med några få undantag (t.ex. deoxyribose) har monosackarider denna kemiska formel: (CH2O)x, där x vanligtvis är ≥ 3. Monosackarider kan klassificeras efter antalet x kolatomer de innehåller: trios (3), tetros (4), pentos (5), hexos (6), heptos (7) och så vidare.
Glukos, som används som energikälla och för syntesen av stärkelse, glykogen och cellulosa, är en hexos. Ribos och deoxyribose (i RNA respektive DNA) är pentosocker. Exempel på heptoser är ketoserna, mannoheptulos och sedoheptulos. Monosackarider med åtta eller fler kolväten observeras sällan eftersom de är ganska instabila. I vattenlösningar existerar monosackarider som ringar om de har mer än fyra kolväten.
Linjärkedjiga monosackarider
Enkla monosackarider har ett linjärt och oförgrenat kolskelett med en funktionell karbonylgrupp (C=O) och en hydroxylgrupp (OH) på var och en av de återstående kolatomerna. Därför kan molekylstrukturen för en enkel monosackarid skrivas som H(CHOH)n(C=O)(CHOH)mH, där n + 1 + m = x, så att dess grundformel är CxH2xOx.
Enligt konvention är kolatomerna numrerade från 1 till x längs ryggraden, med början från den ände som är närmast C=O-gruppen. Monosackarider är de enklaste enheterna av kolhydrater och den enklaste formen av socker.
Om karbonylen befinner sig i position 1 (dvs. n eller m är noll) börjar molekylen med en formylgrupp H(C=O)- och är tekniskt sett en aldehyd. I det fallet kallas föreningen för en aldos. I annat fall har molekylen en ketogrupp, en karbonylgrupp -(C=O)- mellan två kolväten; då är den formellt sett en keton och benämns ketos. Ketoser av biologiskt intresse har vanligtvis karbonylgruppen i position 2.
De olika klassificeringarna ovan kan kombineras, vilket resulterar i namn som ”aldohexos” och ”ketotrios”.
En mer allmän nomenklatur för monosackarider med öppen kedja kombinerar ett grekiskt prefix för att ange antalet kolväten (tri-, tetr-, pent-, hex- osv.) med suffixen ”-ose” för aldoser och ”-ulose” för ketoser. I det senare fallet, om karbonylen inte befinner sig i position 2, anges dess position med ett numeriskt infix. H(C=O)(CHOH)4H är till exempel pentos, H(CHOH)(C=O)(CHOH)3H är pentulos och H(CHOH)2(C=O)(CHOH)2H är pent-3-ulos.
Stereoisomerer med öppen kedja
Två monosackarider med likvärdiga molekylgrafer (samma kedjelängd och samma karbonylposition) kan ändå vara olika stereoisomerer, vars molekyler skiljer sig åt i rumslig orientering. Detta sker endast om molekylen innehåller ett stereogent centrum, närmare bestämt en kolatom som är kiral (kopplad till fyra olika molekylära understrukturer). Dessa fyra bindningar kan ha någon av två konfigurationer i rummet som skiljer sig åt genom sin handledighet. I en enkel monosackarid med öppen kedja är varje kolatom kiral utom kedjans första och sista atom och (i ketoser) kolet med ketogruppen.
Triketosen H(CHOH)(C=O)(CHOH)H (glyceron, dihydroxyaceton) har till exempel inget stereogent centrum och existerar därför som en enda stereoisomer. Den andra triosen, aldosen H(C=O)(CHOH)2H (glyceraldehyd), har ett kiralt kol – det centrala kolet, nummer 2 – som är bundet till grupperna -H, -OH, -C(OH)H2 och -(C=O)H. Därför finns den som två stereoisomerer vars molekyler är spegelbilder av varandra (som en vänster och en höger handske). Monosackarider med fyra eller fler kolväten kan innehålla flera kirala kolväten, så de har vanligtvis mer än två stereoisomerer. Antalet distinkta stereoisomerer med samma diagram begränsas av 2c, där c är det totala antalet chirala kolväten.
Fischerprojektionen är ett systematiskt sätt att rita skelettformeln för en acyklisk monosackarid så att varje chiralt kolväte är väl specificerat. Varje stereoisomer av en enkel monosackarid med öppen kedja kan identifieras genom positionerna (höger eller vänster) i Fischer-diagrammet för de chirala hydroxylerna (de hydroxyler som är knutna till de chirala kolvätena).
De flesta stereoisomerer är i sig själva chirala (skilda från sina spegelbilder). I Fischer-projektionen skiljer sig två spegelbildsisomerer åt genom att positionerna för alla chirala hydroxyler är omvända från höger till vänster. Spegelbildsisomerer är kemiskt identiska i icke-kirala miljöer, men har vanligen mycket olika biokemiska egenskaper och förekomster i naturen.
Men även om de flesta stereoisomerer kan arrangeras i par av spegelbildsformer finns det vissa icke-kirala stereoisomerer som är identiska med sina spegelbilder, trots att de har kirala centra. Detta sker när molekylgrafen är symmetrisk, som i 3-ketopentoserna H(CHOH)2(CO)(CHOH)2H, och de två halvorna är spegelbilder av varandra. I det fallet är speglingen likvärdig med en rotation med ett halvt varv. Av denna anledning finns det endast tre distinkta stereoisomerer av 3-ketopentoser, trots att molekylen har två kirala kolväten.
Distinkta stereoisomerer som inte är spegelbilder av varandra har vanligtvis olika kemiska egenskaper, även i icke-kirala miljöer. Därför kan varje spegelpar och varje icke-kiral stereoisomer ges ett specifikt monosackaridnamn. Det finns t.ex. 16 olika stereoisomerer av aldohexos, men namnet ”glukos” avser ett specifikt par av spegelbildliga aldohexoser. I Fischer-projektionen har den ena av de två glukosisomererna hydroxeln till vänster på C3 och till höger på C4 och C5, medan den andra isomeren har det omvända mönstret. Dessa specifika monosackaridnamn har konventionella förkortningar på tre bokstäver, som ”Glu” för glukos och ”Thr” för threos.
Generellt har en monosackarid med n asymmetriska kolväten 2n stereoisomerer. Antalet stereoisomerer med öppen kedja för en aldosemonosackarid är större med en än för en ketosemonosackarid av samma längd. Varje ketos kommer att ha 2(n-3) stereoisomerer där n > 2 är antalet kolväten. Varje aldos kommer att ha 2(n-2) stereoisomerer där n > 2 är antalet kolväten Dessa kallas också epimerer som har olika arrangemang av -OH- och -H-grupper vid de asymmetriska eller kirala kolatomerna (detta gäller inte de kolväten som har den funktionella karbonylgruppen).
Konfiguration av monosackarider
Likt många kirala molekyler kommer de två stereoisomererna av glyceraldehyd att gradvis rotera polarisationsriktningen för linjärt polariserat ljus när det passerar genom den, även i lösning. De två stereoisomererna identifieras med prefixen D- och L-, beroende på rotationsriktningen: D-glyceraldehyd är dextrorotatoriskt (roterar polarisationsaxeln medurs), medan L-glyceraldehyd är levorotatoriskt (roterar den moturs).

D- och L-prefixen används också med andra monosackarider, för att särskilja två särskilda stereoisomerer som är spegelbilder av varandra. För detta ändamål tar man hänsyn till det chirala kol som ligger längst bort från C=O-gruppen. Dess fyra bindningar måste ansluta till -H, -OH, -C(OH)H och resten av molekylen. Om molekylen kan roteras i rummet så att riktningarna för dessa fyra grupper stämmer överens med riktningarna för de analoga grupperna i D-glyceraldehyds C2, får isomeren prefixet D-. I annat fall får den L-prefixet.
I Fischer-projektionen anger D- och L-prefixen konfigurationen vid den kolatom som är näst längst ner: D- om hydroxylgruppen är på höger sida och L- om den är på vänster sida.
Bemärk att D- och L-prefixen inte anger rotationsriktningen för polariserat ljus, vilket är en kombinerad effekt av arrangemanget vid alla chirala centra. De två enantiomererna kommer dock alltid att rotera ljuset i motsatt riktning, med samma mängd. Se även D/L-systemet.
Cyklisering av monosackarider
En monosackarid övergår ofta från den acykliska (öppen kedja) formen till en cyklisk form, genom en nukleofil additionsreaktion mellan karbonylgruppen och en av hydroxylgrupperna i samma molekyl. Reaktionen skapar en ring av kolatomer som är sluten med en överbryggande syreatom. Den resulterande molekylen har en hemiacetal- eller hemiketalgrupp, beroende på om den linjära formen var en aldos eller en ketos. Reaktionen är lätt att vända och ger den ursprungliga öppna kedjeformen.
I dessa cykliska former har ringen vanligtvis fem eller sex atomer. Dessa former kallas furanoser respektive pyranoser – i analogi med furan och pyran, de enklaste föreningarna med samma kol-oxygenring (även om de saknar dubbelbindningar hos dessa två molekyler). Aldohexosen glukos kan till exempel bilda en hemiacetalbindning mellan hydroxyl på kol 1 och syre på kol 4, vilket ger en molekyl med en femledad ring som kallas glukofuranos. Samma reaktion kan äga rum mellan kolvätena 1 och 5 för att bilda en molekyl med en 6-membrig ring, kallad glukopyranos. Cykliska former med en sjuatomig ring (samma som oxepan), som sällan förekommer, kallas heptoser.



För många monosackarider (inklusive glukos), de cykliska formerna dominerar i fast tillstånd och i lösningar, och därför används ofta samma namn för isomerer med öppen och sluten kedja. Således kan till exempel termen ”glukos” beteckna glukofuranos, glukopyranos, den öppna kedjeformen eller en blandning av de tre.
Cyklitisering skapar ett nytt stereogent centrum vid det karbonylbärande kolet. Den -OH-grupp som ersätter karbonylens syre kan hamna i två olika positioner i förhållande till ringens mittplan. Således ger varje monosackarid med öppen kedja två cykliska isomerer (anomerer) som betecknas med prefixen α- och β-. Molekylen kan växla mellan dessa två former genom en process som kallas mutarotation, som består i en omvändning av den ringbildande reaktionen följt av en annan ringbildning.
Haworthprojektion
Den stereokemiska strukturen hos en cyklisk monosackarid kan representeras i en Haworthprojektion. I detta diagram har α-isomeren för pyranosformen av en D-aldohexos -OH för det anomeriska kolet under kolatomernas plan, medan β-isomeren har -OH för det anomeriska kolet ovanför planet. Pyranoser antar vanligtvis en stolskonformation, liknande den för cyklohexan. I denna konformation har α-isomeren det anomeriska kolets -OH i axiell position, medan β-isomeren har det anomeriska kolets -OH i ekvatorial position (med tanke på D-aldohexos-socker).
-
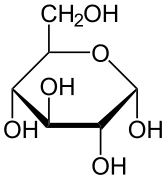
α-D-Glukopyranos
-

β-D-Glucopyranose
Derivat
Det finns ett stort antal biologiskt viktiga modifierade monosackarider:
- Aminosocker såsom:
- galaktosamin
- glukosamin
- sialsyra
- N-acetylglukosamin
- Sulfosocker såsom:
- sulfoquinovos
- Andra ämnen som t.ex:
- askorbinsyra
- mannitol
- glukuronsyra
Se även
- Nomenklatur för monosackarider
- Reducerande socker
- Sockersyra
- Sockeralkohol
- Disackarid
Noter
- ^ ”Kolhydrater”. Kemi för biologer. Royal Society of Chemistry. Hämtad den 10 mars 2017.
- ^ NCERT TEXT BOOK CLaSS-12
- ^ ”Carbohydrates”. Kemi för biologer. Royal Society of Chemistry. Hämtad den 10 mars 2017.
- ^ Pigman, William Ward; Anet, E. F. L. J. (1972). ”Kapitel 4: Mutarotationer och verkan av syror och baser”. I Pigman och Horton (red.). The Carbohydrates: Chemistry and Biochemistry. 1A (2nd ed.). San Diego: Academic Press.
- ^ IUPAC, Compendium of Chemical Terminology, 2nd ed. (”Guldboken”) (1997). Online korrigerad version: (2006-) ”Haworth representation”. doi:10.1351/goldbook.H02749


Lämna ett svar