ORIGINAL PAPERS
Hepatitis B surface antigen detection using pooled sera. A cost-benefit analysis
E. Fernández, L. Rodrigo1, S. García, S. Riestra1 och C. Blanco
Service för biokemi. Hospital de Cabueñes. Gijón. 1Gastroenterologisk avdelning. Hospital Central de Asturias. Oviedo. Spanien
Korrespondens
ABSTRACT
Mål: Att undersöka genomförbarheten och utföra en kostnads-nyttoanalys av en strategi för sammanslagning av fem prover med hjälp av en enzymimmunoassay (EIA) för screening av hepatit B-ytantigen (HBsAg).
Material och metoder: För att bedöma känsligheten och specificiteten hos poolningsmetoden testades var och en av de 40 positiva sera (från svagt till intensivt HBsAg-positiva) och 250 negativa sera i en pool med 4 HBsAg-negativa sera. Detektionsgränsen för HBsAg/ad och HBsAg/ay utvärderades med hjälp av serum från en panel av renodlade subtyper. En studie under verkliga förhållanden genomfördes med pooler från 340 gravida kvinnor.
Resultat: Känsligheten och specificiteten för denna teknik var 100 %. Korrelationskoefficienten mellan förhållandet prov/avklippning av 40 prover som studerats i enskilda och i poolade förhållanden var 0,792 (p < 0,005). Poolingmetoden har lägre detektionsnivåer för HBsAg/ad och HBsAg/ay på 0,20 ng/mL och 0,12 ng/mL, och den enskilda metoden på 0,34 ng/mL respektive 0,29 ng/mL. Poolingmetoden förlorar ingen känslighet för värden upp till 100 IU/L anti-HBs i de fyra serumen som blandas med ett positivt serum. Kostnads-nyttoanalysen visade att poolingmetoden skulle kunna spara 30-75 % av kostnaden för HBsAg-bestämning, beroende på om seroprevalensen var 10 % eller 1 %.
Slutsatser: Den poolade HBsAg EIA gav inte sämre resultat än det enskilda EIA-testet och var en kostnadseffektiv och giltig strategi i områden med hög, medelhög eller låg prevalens.
Nyckelord: Hepatit B ytantigen. Pooling sera. Kostnads-nyttoanalys.
Rodrigo L, Fernández E, García S, Riestra S, Blanco C. Hepatitis B surface antigen detection using pooled sera. En kostnads-nyttoanalys. Rev Esp Enferm Dig 2006; 98: 112-121.
Introduktion
Hepatit B-virus (HBV) är en sjukdom som drabbar miljontals människor världen över. Dess huvudsakliga reservoar är kroniska HBV-bärare. Man uppskattar att cirka 300 miljoner människor i hela världen är infekterade av detta virus (1). De medicinska konsekvenserna av HBV-infektion är både varierande och oförutsägbara, beroende på faktorer som patientens ålder och immunstatus. HBV är ett välkänt etiologiskt agens för kronisk hepatit, levercirros och hepatocellulärt karcinom.
Stora skillnader finns dock i prevalensen av infektionen, och detta har lett till att tre huvudområden med hög, medelhög och låg endemicitet har fastställts (2). I de flesta utvecklade länder är prevalensen av kroniska HBV-bärare mindre än 2 %, och infektionsöverföring sker framför allt hos vuxna som tillhör vissa riskgrupper (narkotikamissbrukare, homosexuella män, promiskuösa heterosexuella, hälso- och sjukvårdspersonal) (3). I Spanien har man funnit en prevalens av HBV-bärare på 1,2 % (4), och det är obligatoriskt att identifiera HBsAg hos blodgivare, gravida kvinnor och personer som genomgår autotransfusionsprogram.
Med serumpooling-tekniken försöker man minska kostnaderna utan att förlora i effektivitet, och den har framför allt använts i utvecklingsländer för att söka efter antikroppar mot humant immunbristvirus (hiv) (5-14) och hepatit C-virus (HCV) (15-19). De resultat som erhållits med denna metod har visat sig vara mycket lovande, eftersom de har minskat kostnaderna för laboratorietesterna avsevärt utan att deras känslighet minskat nämnvärt.
I denna studie försöker man bedöma om tekniken med serumpooling är tillämplig vid påvisande av HBsAg för att belysa de faktorer som kan modifiera dess känslighet och för att utföra en kostnads-nyttoanalys för denna diagnostiska teknik.
Material och metoder
HBsAg-bestämning
Imx HBsAg-assay (Abbott Laboratories, Abbott Park, IL), som är ett kvalitativt tredje generationens mikropartiklar Enzyme Immunoassay (EIA), användes för HBsAg-bestämning. Förekomsten eller frånvaron av HBsAg bestäms genom att jämföra hastigheten för bildning av fluorescerande produkter med ett gränsvärde, som beräknas från den negativa kalibratorns (N) hastighet (human plasma som inte reagerar på HBsAg). Imx HBsAg-analysen beräknar ett förhållande mellan provets (S) hastighet och den negativa kalibratorns hastighet. Gränsvärdet (S/N) fastställdes till 2 för EIA med ett enda serum.
Poolningstekniken utförs genom att 200 mcL tillsätts till poolen, det vill säga genom att få en blandning av 40 mcL av vart och ett av de fem serum som ingår i poolen (utspädning 1/5). Gränsvärdet fastställdes som medelvärdet för negativa prover plus 3 standardavvikelser, vilket ger ett värde på 1. Det anses därför att det finns ett icke-reaktivt prov i denna grupp av 5 när S/N-koefficienten är < gränsvärdet, medan en S/N-pool > gränsvärdet kan tyda på förekomsten av minst ett reaktivt prov. I detta fall måste enskilda prover testas på nytt för att identifiera det eller de reaktiva proverna. Alla tester utförs i två exemplar.
I enlighet med ovanstående utvärderades specificiteten genom HBsAg-bedömning i 50 pooler med 250 negativa serum. För att beräkna känsligheten testades 40 serum med samma koncentrationsfördelning som den allmänna populationen från vilken de provtagits i en pool med 4 negativa serum.
HBBsAg-subtyper (ad och ay)
Detektionsgränsen för Imx HBsAg för ad och ay utvärderades med hjälp av serum från en panel av renodlade HBsAg-subtyper (hepatitis HBsAg sensitivity panel, Abbott Laboratories). Koncentrationerna av HBsAg/ad och HBsAg/ay varierade från 0,13 till 2,32 ng/mL respektive från 0,21 till 2,24 ng/mL. Detektionsgränsen bestämdes i enstaka och i en pool med 4 HBsAg-negativa serum.
Influens av anti-HBs nivå
För att fastställa om förekomsten av anti-HBs antikroppar i de serum som undersökts med hjälp av det sammanslagna testet skulle kunna neutralisera HBsAg och störa teknikens känslighet tillämpade vi metoden med att sammanslagna ett serum med en känd koncentration av HBsAg/ad och HBsAg/ay med fyra serum med kända titrar av anti-HBs.
Den kvantitativa bestämningen av anti-HBs utfördes med en mikropartikelenzymimmunoassay-metod (mEIA) med hjälp av en AxSYm autoanalysator (AxSYmTM AUSAB, Abbott Laboratories, Abbott Park, IL). Sera med höga anti-HBs-titrar erhölls från postvaccinerade HBV-kontroller och patienter som återhämtat sig från hepatit B.
Pool-test vid screening av HBsAg
För att bedöma validiteten av pool-testning genomfördes en simulering av fältverksamhet med ovanstående metod på 1525 serumprover som erhållits från gravida kvinnor i en tidigare studie av oss för att uppskatta prevalensen av HCV-infektion, och vars prover förvarats vid -20 ºC sedan insamlingen. Vi valde slumpmässigt ut 300 negativa HBsAg-prover och 14 positiva HBsAg-prover från dessa. Bestämningarna gjordes utan föregående kunskap om poolens sammansättning.
Reduktion av antalet tester
När en pool ger ett positivt resultat måste varje komponent testas på nytt individuellt för att identifiera det eller de prov som är HBsAg-positiva. Ju större antalet positiva pooler (dvs. prevalensen av HBsAg) är, desto mindre är minskningen av antalet utförda tester.
På grundval av detta beräknades den procentuella minskningen av antalet tester när screening av HBsAg med poolade serum användes under de mest ogynnsamma och osannolika förhållandena (låg prevalens), dvs. när det inte fanns mer än ett positivt serum i någon av poolerna. Om t.ex. en seroprevalens av HBsAg är 2 % och 100 serum analyseras i 20 pooler, kommer 2 av dessa att vara positiva. Det är alltså nödvändigt att lägga till 10 bestämningar (10 serum som testas på nytt individuellt) till de 20 ursprungliga bestämningarna (20 pooler), vilket ger totalt 30 bestämningar. I detta exempel kan 70 % av kostnaden sparas. För att göra en kostnads-nyttoanalys uppskattades priset för HBsAg-testning till 3 US-dollar för varje prov. Detta då det baseras på det genomsnittliga faktiska priset för det kommersiella kitet på vårt sjukhus.
Statistisk analys
Data samlades in i en databas och analyserades senare med hjälp av statistikpaketet SPSS for Windows, Release 10.0. Spearmans icke-parametriska linjära korrelation användes. Resultaten uttrycks som medelvärde ± SD. En nivå på p < 0,05 ansågs vara statistiskt signifikant.
Resultat
Ingen av de 50 poolerna av HBsAg-negativa sera resulterade i positiva resultat (S/N pool > 1), och följande värden för S/N pool erhölls: 0,767 ± 0,076 (intervall 0,67-0,88). Med detta prov var specificiteten för denna poolningsteknik därför 100 %. Å andra sidan gav alla 40 HBsAg-positiva serum, när de bestämdes i poolad form, S/N-värden som var större än 1 (med en känslighet som också var 100 %). Korrelationskoefficienten mellan S/N-talen för dessa 40 prover som undersöktes i enskilt och i pool var 0,792 (p < 0,05).
Tjugosex punkt sex procent av poolerna med prover med höga HBsAg-titrar hade ett S/N-tal som till och med var större än det enskilda provet. Korrelationskoefficienten för prover med låga HBsAg-titrar (S/N singel < 25, n = 12) var dock utmärkt (R = 0,9739, p < 0,05), vilket framgår (fig. 1).

Detektionsgränsen med hjälp av den enskilda metoden var 0.34 ng/mL för ad-subtypen och 0,29 ng/mL för ay-subtypen, medan lägre antigennivåer upptäcktes med poolingmetoden: 0,20 ng/mL respektive 0,12 ng/mL. Resultaten av att tillämpa den enskilda och poolade tekniken på serum med olika koncentrationer av HBsAg/ad och HBsAg/ay visas (fig. 2).

När anti-HBs-titern i poolen är mindre än 100 IU/L förlorar tekniken inte i känslighet; även när anti-HBs-titern når 10 000 IU/L kan tekniken fortfarande detektera HBsAg-koncentrationer som är så låga som 1,5 ng/mL. Inverkan av de olika koncentrationerna av anti-HBs på detektionsgränsen för HBsAg-subtyper vid användning av poolingmetoden presenteras (medelvärde av 2 bestämningar) (fig. 3).
I den undersökning som utfördes under verkliga förhållanden i serum från gravida kvinnor resulterade poolingmetoden i en korrekt klassificering av alla analyserade prover. Följaktligen var sensitiviteten och specificiteten 100 %.
Det finns en minskning av den procentuella minskningen av antalet tester som uppnås med poolingmetoden när seroprevalensen av HBsAg ökar. Man kan se att även med HBsAg-prevalenser så höga som 10 % i det studerade urvalet uppnås en minsta besparing på minst 30 % (fig. 4).

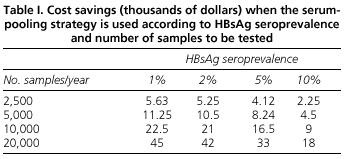
Analysen av de ekonomiska fördelarna med strategin för serumpooling visar att den uppnådda besparingen beror både på HBsAg-prevalensen och på antalet bestämningar som ska göras. För länder med låg prevalens, som vårt land, minskar alltså poolingmetoden testkostnaderna för HBsAg. Vi uppskattade t.ex. att besparingarna för 2 500 bestämningar som utförs i ett laboratorium under ett år med hjälp av poolingmetoden kommer att uppgå till 5 630 US-dollar, och för ett mycket välbesökt sjukhus som utför 20 000 bestämningar per år kommer besparingarna att uppgå till 45 000 US-dollar (tabell I).
Diskussion
En strategi för poolingmetoden är att bibehålla utspädningen och slutvolymen av reaktionsblandningen i varje poolat test för att inte förlora känslighet, för vilket utspädningsmedlet minskas och delvis ersätts av de extra sera. På detta sätt är det inte nödvändigt att ändra gränsvärdet i förhållande till standardmetoden i individualiserade prover. Den metod som användes i vår studie var dock automatiserad och provspädningen utfördes av en autoanalysator. Av denna anledning uppvisar varje prov en utspädning på 1 på 5 när det blandas med de övriga 4 sera. Därför var det i vår studie nödvändigt att ändra gränsvärdet och begränsa antalet sera i poolen för att inte förlora känslighet.
När det gäller specificitet är det nödvändigt att notera att medelvärdet för pooler bara var drygt 3 standardavvikelser från gränsvärdet. Således kan man förvänta sig ett falskt positivt resultat i ungefär 1 % av fallen. Vi anser att detta är acceptabelt eftersom specificiteten är nästan 100 % (99,9 %). En studie med ett större antal negativa prover från ett stort antal olika individer kommer att krävas för att fastställa den verkliga specificiteten hos denna analys.
Även om korrelationen mellan testning av enskilda och poolade prover är god, skär regressionslinjen X-axeln vid ett S/N-förhållande på 3 (motsvarande Y-värde är 1). Detta kan betyda att varje prov med ett S/N-förhållande mellan 2 och 3 i testet med ett enskilt prov skulle ha ett värde under 1 och därför inte upptäckas i det sammanslagna testet.
För en prevalens på 1 % HBsAg-positiva sera uppnådde en matematisk modell som beskrivs av Liu et al. (19) den maximala minskningen (80,5 %) av antalet tester för en poolstorlek på 11 sera. Vi anser dock att det kan uppstå ett problem med specificiteten på grund av effekten av poolning på andelen falskt positiva resultat. En ökning av icke-specifika proteiner, till följd av blandningen av sera, kan ge upphov till en ökning av bakgrundsfärgen. Med den poolstorlek på 5 som valdes för vår studie och ändringen av gränsvärdet från 2 till 1 observerades inga förluster i sensitivitet (falskt negativa) eller specificitet (falskt positiva).
Resultaten av den aktuella studien visar att tekniken med poolning av serum för påvisande av HBsAg är mycket känslig och specifik, och möjliggör också betydande ekonomiska besparingar. Dessa resultat liknar dem som erhållits av andra forskare som tillämpat metoden med pooling vid undersökning av HCV- och hiv-infektion (5-19). Hittills har endast två studier (20,21) rapporterats om tillämpningen av poolingmetoden vid undersökning av HBV-infektion. I en av dessa (20), som utfördes i samband med rutinmässig prenatal screening för hepatit B genom att testa 10 provpooler, fann författarna en låg prevalens av kroniska bärare (0,43 %) och drar slutsatsen att detta är en kostnadseffektiv metod och en giltig strategi i områden med låg seroprevalens, med en minskad sensitivitet som uppskattas till 4,2 %. I vår studie tillämpades poolingmetoden på gravida kvinnor, bland vilka prevalensen av kroniska HBsAg-bärare är 0,93 %, vilket gav en sensitivitet och specificitet på 100 %.
Fördelningen av de två viktigaste subtyperna av HBsAg (ad och ay) i vår miljö är ungefär 50 % för vardera, medan ay är vanligare hos narkotikamissbrukare som använder sig av parenteral behandling (22). Vi har visat att poolingmetoden förbättrar känsligheten, dvs. sänker detektionsgränsen för ett immunoassay som används för bestämning av de två viktigaste HBsAg-subtyperna. Vår poolingteknik gör det möjligt att detektera så små mängder som 0,20 ng/mL HBsAg/ad och 0,12 ng/mL HBsAg/ay, vilket är ännu lägre än de mängder som erhålls med standardmetoden. Att man finner en ökad känslighet med poolningstestning är inte förvånande eftersom detta har rapporterats av andra författare (16). Det är viktigt att bedöma känsligheten hos det EIA-kit som används för pooltestet, eftersom alla kit kanske inte är lämpliga för screening av pooler, vilket har visats när det gäller antikroppar mot hepatit C-virus (23,24).
Närvaron av anti-HBs i poolsera skulle kunna modifiera teknikens känslighet, men endast på ett signifikant sätt i titrar som är högre än 10 000 IE/mL, vilket endast har setts i prover från kontrollstudier efter vaccinering; i den här situationen är det inte indicerat att bestämma HBsAg. Faktum är att Cunninghan et al. (20) fann att endast 4,5 % av pooler bestående av serum från gravida kvinnor hade en anti-HBs titer som var högre än 7 500 IU/L. Med tanke på denna begränsning av känsligheten hos poolningsmetoden fann de att denna också låg runt 100 % i känslighet och specificitet. Våra resultat skulle kunna vara reproducerbara i andra områden med låg prevalens, men de bör tidigare demonstreras i områden med hög endemicitet för HBV. I dessa områden är majoriteten av befolkningen redan immuniserad mot detta virus, och det är möjligt att anti-HBs-titrar som hittas i serum är något förhöjda.
Rabenau et al. (21) undersökte säkerheten för serologiska tester i plasmapooler för HBsAg med hjälp av ett EIA-system som liknar vårt. I deras studie påverkades detektionen av HBsAg av förekomsten av låga anti-HBs-titrar efter 5 timmars inkubation. Efter dissociation av immunkomplexet kunde HBsAg dock fortfarande påvisas i poolen även i närvaro av hög anti-HBs-halt. I vår studie visar vi att endast en signifikant minskning av känsligheten resulterar för anti-HBs-titrar högre än 10 000 IU/L. Dessa skillnader kan bero på att proverna i vårt fall testades utan föregående inkubation. Detta skulle kunna förhindra antigenneutralisering genom immunokomplexbildning.
Vi anser därför att både titern av anti-HBs i serum och behandlingen av proverna med EIA före testet kan påverka poolningsmetodens känslighet. Varje laboratorium som önskar använda denna teknik bör ha dessa två faktorer i åtanke innan allmän användning införs.
WHO rekommenderar användning av serumpoolingmetoden vid hiv-infektion, när prevalensen av sjukdomen är mindre än 2 %, och med en maximal pooling av 5 serum (25). Enligt dessa indikationer tillämpar och rekommenderar de flesta studier användningen av poolingmetoder i områden med låg seroprevalens. I vår studie visar vi att pooling av serum också kan vara kostnadseffektivt i populationer med hög prevalens av HBsAg-bärare. Detta skulle kunna göra det möjligt att använda den i länder som tillhör områden med medelhög och hög endemicitet för HBV-infektion, vilket i allmänhet sammanfaller med underutvecklade länder eller utvecklingsländer, dvs. länder som har ett större behov av att minska de ekonomiska kostnaderna för laboratorietester. Det är dock nödvändigt att genomföra liknande studier i dessa områden för att bekräfta våra resultat. Det har dock redan visats att i länder som Kenya, som har en hög frekvens av hiv-infektion (7,3 %), skulle tillämpningen av pooling för upptäckt av hiv möjliggöra en ekonomisk besparing på 62 % utan någon betydande säkerhetsförlust (14). I Spanien, ett land som tillhör ett område med låg endemicitet för HBV-infektion och med en frekvens av HBsAg-bärare i den allmänna befolkningen på 1,2 % (4), kan det användas i alla de grupper där screening för HBsAg för närvarande är obligatorisk (t.ex. blodgivare, personer som genomgår autotransfusionsprogram, screening av gravida kvinnor).
Kostnads-nyttostudien av tillämpningen av tekniker för att upptäcka kroniska bärare av HBV gör det möjligt att visa att de ekonomiska besparingarna är större när de görs i ett stort antal bestämningar i grupper med låg seroprevalens, och användningen skulle också kunna vara kostnadseffektiv i områden med hög prevalens av infektion och även i laboratorier som utför ett litet antal bestämningar. Vi har visat ekonomiska kostnadsbesparingar beroende på både olika HBsAg-prevalens och antalet tester som ska utföras årligen. I vårt område skulle tillämpningen av poolingmetoden kunna spara cirka 74 % av de totala ekonomiska kostnaderna jämfört med den enskilda metoden.
Vissa utredare har nyligen börjat praktisera strategier för detektion av virala nukleinsyror hos blodgivare med hjälp av polymeraskedjereaktion (PCR) i syfte att öka den säkerhet som är förknippad med transfusion av blodderivat (26-29). På grund av att det inte är möjligt att genomföra individuella screeningar på grund av ekonomiska problem och den arbetsinsats som detta innebär, används nu metoden att sammanföra prover av serologiskt negativt blod. Detta förfarande kan öka blodsäkerheten genom en systematisk screening av blodgivningar till en relativt låg kostnad. Eftersom en av de största begränsningarna i tillämpningen av dessa metoder är av ekonomisk art, tror vi att det med vår studie skulle kunna finnas en teoretisk grund för användning av screening för HBV-, HCV- och hiv-infektioner i två steg till en relativt låg ekonomisk kostnad. I den första fasen skulle en kommersiell EIA kunna tillämpas på en pool av givarsera. I den andra fasen skulle tillämpningen av PCR-teknik på en pool av seronegativa prover kunna öka säkerheten i analysen. Tills framtida studier kan bevisa värdet av denna teknik med blodgivare anser vi att den endast skulle kunna tillämpas på diagnostisk och epidemiologisk testning.
Vi drar slutsatsen att tillämpningen av EIA på poolade serum är en känslig och specifik metod för att upptäcka de två viktigaste HBsAg-subtyperna i ett område med låg seroprevalens. Känsligheten minskar endast när mycket höga titrar av anti-HBs finns i de sammanslagna serumen. Poolingtekniken är en metod som också kan ge ekonomiska besparingar om den används vid studier av populationer med hög förekomst av HBsAg-bärare. Vi anser att ytterligare studier är nödvändiga för att bekräfta dessa resultat.
Acknowledgements
Vi vill tacka David H. Wallace (medlem av European Association of Science Editors och Council of Biological Editors) för den engelska översättningen av manuskriptet.
1. Maynard JE. Hepatit B: global betydelse och behov av kontroll. Vaccine 1990; 8 (Supl.): 18s-20s.
2. Margolis HS, Alter MJ, Hadler SC. Hepatit B: epidemiologi under utveckling och konsekvenser för kontroll. Sem Liver Dis 1991; 11: 84-92.
3. Alter MJ, Mast EE. Epidemiologin för viral hepatit i Förenta staterna. Gastroenterol Clin North Am 1994; 23: 437-55.
4. Suárez A, Riestra S, Navascués CA, et al. Positiva HBsAg-blodgivare i Asturien (Spanien): nuvarande prevalens och dess betydelse. (engelsk sammanfattning). Med Clin (Barcelona) 1994; 102: 329-32.
5. Emmanuel JC, Basset MT, Smith HJ, Jacobs JA. Pooling of sera for human immunodeficiency virus (HIV) testing: en ekonomisk metod för användning i utvecklingsländer. J Clin Pathol 1988; 41: 582-5.
6. Kline RL, Brothers TA, Brookmeyer R, et al. Utvärdering av seroprevalens av humant immunbristvirus i befolkningsundersökningar med hjälp av sammanslagna serum. J Clin Microbiol 1989; 27: 1449-52.
7. Cahoon-Young B, Chandler A, Livermore T, et al. Känslighet och specificitet hos sammanslagna serum jämfört med individuella serum i en undersökning av prevalensen av antikroppar mot humant immunbristvirus. J Clin Microbiol 1989; 27: 1893-5.
8. Frosner GG, Dobler G, von Sonnenburg FJ. Kostnadsminskning av obundet test för anti-HIV-testning genom undersökning av sammanslagna serum. AIDS 1990; 4: 73-5.
9. Behets F, Bertozzi S, Kasali M, et al. Framgångsrik användning av sammanslagna serum för att fastställa hiv-1-seroprevalens i Zaire med utveckling av kostnadseffektivitetsmodeller. AIDS 1990; 4: 737-41.
10. Monzon OT, Paladin FJ, Dimaandal E, et al. Relevans av antikroppsinnehåll och testformat vid hiv-testning av poolade serum. AIDS 1992; 6: 43-8.
11. Tamashiro H, Maskill W, Emmanuel J, et al. Reducing the cost of HIV antibody testing. Lancet 1993; 342: 87-90.
12. Perriens JH, Magazani K, Kapila N, et al. Användning av ett snabbtest och ett ELISA-test för hiv-antikroppsscreening av samlade serumprover i Lubumbashi, Zaire. J Virol Methods 1993; 41: 213-21.
13. McMahon EJ, Fang C, Layug L, Sandler SG. Pooling blood donor samples to reduce the cost of HIV-1 antibody testing. Vox Sang 1995; 68: 215-9.
14. Verstraeten T, Farah B, Duchateau L, Matu R. Pooling sera to reduce the cost of HIV surveillance: a feasibility study in a rural Kenyan district. Trop Med Int Health 1998; 3: 747-50.
15. Kamel MA, Ghaffar YA, Wasef MA, et al. Hög HCV-prevalens hos egyptiska blodgivare. Lancet 1992; 340: 427.
16. Neil AGS, Conradie JD. Låg kostnad för anti-HCV-screening av blodgivare. Lancet 1992; 340: 1096.
17. Fernández E, Riestra S, García S, Rodríguez S. Pooltester för upptäckt av hepatit C-virusinfektion. J Hepatol 1995; 23: 236.
18. García Z, Taylor L, Ruano A, et al. Utvärdering av en poolingmetod för rutinmässig anti-HCV-screening av blodgivare för att minska kostnadsbördan för blodbanker i utvecklingsländer. J Med Virol 1996; 49: 218-22.
19. Liu P, Shi ZX, Zhang YC, et al. En prospektiv studie av en serumpoolingstrategi vid screening av blodgivare för antikroppar mot hepatit C-virus. Transfusion 1997; 37: 732-6.
20. Cunningham R, Northwood JL, Kelly CD, et al. Rutinmässig prenatal screening för hepatit B med hjälp av poolade serum: validering och granskning av 10 års erfarenhet. J Clin Pathol 1998; 51: 392-5.
21. Rabenau H, Schutz R, Berger A, et al. Hur exakt är serologisk testning av plasmapooler för ytantigen av hepatit B-virus, anti-humant immunbristvirus 1 och 2 och antihepatit C-virus? (engelsk sammanfattning). Infus Transfus 1996; 23: 124-30.
22. Echevarría JE, León P, López JA, et al. HBsAg-subtypfördelning bland olika populationer av HBsAg-bärare i Spanien. Eur J Epidemiol 1995; 11: 39-45.
23. Neill AGS, Conradie JD. Pooltester för hepatit C-virus. Lancet 1994; 343: 738.
24. Liu P, Shi ZX, Zhang YC, Zhang XY. Jämförande studie av fyra EIA-kits för screening av antikroppar mot hepatit C-virus i poolade serum. Biomed Environ Sci 1998; 11: 75-80.
25. Rekommendationer för testning av hiv-antikroppar i serumpool. WHO Weekly Epidemiol Rec 1991; 44: 316-27.
26. Lefrere JJ, Coste J, Defer C, et al. Screening blood donations for viral genomes: multicenter study of real-time simulation using pooled samples on the model of hepatitis C virus RNA detection. Transfusion 1998; 38: 915-23.
27. Yerly S, Pedrocchi M, Perrin L. The use of polymerase chain reaction in plasma pools for the concomitant detection of hepatitis C virus and HIV type 1 RNA. Transfusion 1998; 38: 908-14.
28. Schottstedt V, Tuma W, Bunger G, Lefevre H. PCR for HBV, HCV and HIV-1 experiences and first results from a routine screening programme in a large blood transfusion service. Biologicals 1998; 26: 101-4.
29. Morandi PA, Schockmel GA, Yerly S, et al. Detektion av humant immunbristvirus typ 1 (HIV-1) RNA i pooler av serum som är negativa för antikroppar mot HIV-1 och HIV-2. J Clin Microbiol 1998; 36: 1534-8.
Lämna ett svar