BUCKALREGIONEN – EN FÖRDELANDE VÄG FÖR LÄKEMEDELSFÖRDELNING
Innovationer inom läkemedelsförmedling ger löfte om att minimera dosberoende bieffekter och maximera den biologiska aktiviteten samtidigt som man förbättrar patientens följsamhet.
Peroral administrering av läkemedel, den föredragna vägen för läkemedelsadministrering när det gäller patientens erfarenhet, har flera nackdelar, t.ex. hepatisk förstapassmetabolism, längre verkningstid och enzymatisk nedbrytning av läkemedel i mag-tarmkanalen (GI-kanalen). När GI- och hepatisk nedbrytning begränsar ett läkemedels säkerhet eller effekt är invasiva injektioner ofta det enda gångbara leveranssättet – med den potentiella konsekvensen av lägre patientföljsamhet.

Buccal administrering kan uppnå lokala och systemiska effekter och är attraktivt i och med att det övervinner bristerna med peroral administrering. Ämnen som absorberas genom buccalslemhinnan kringgår nämligen gastrointestinal enzymatisk nedbrytning och den hepatiska first-pass-effekten. Buccal administrering utgör dessutom ett bättre alternativ till injektioner eller tabletter för de patienter som har svårt att svälja.
Vad är buccalplatsen?
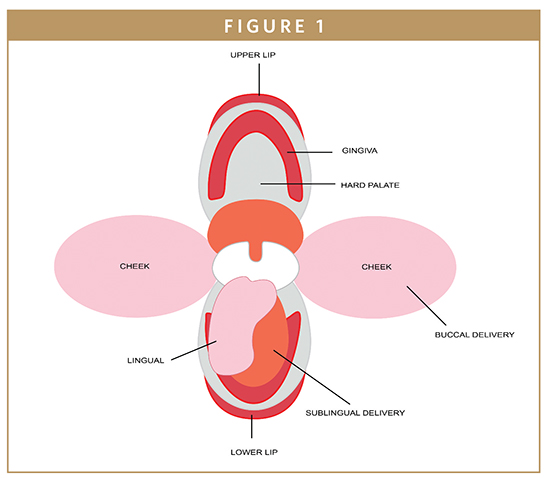
Buccalområdet är den inre beklädnaden av kinden och läppen och utgör ungefär en tredjedel av munhålans yta (figur 1).1 Buccalslemhinnan består av ett ytskikt av stratifierat skivepitel som är kopplat till den underliggande bindväven genom en basal lamina. Ett nätverk av blodkapillärer finns i bindväven där läkemedel som har trängt igenom epitelet kan komma in i den systemiska cirkulationen via den inre halsvenen.2
Buccalepitelet fungerar som en barriär för hydrofil läkemedelsgenomträngning, medan bindväven, som är mer hydrofil till sin natur, tycks påverka diffusionsfördröjningstiden för lipofila föreningar3 . Läkemedelstransporten genom slemhinnan kan vara trans- eller paracellulär (figur 2), där de flesta hydrofila läkemedel och makromolekyler permeerar genom passiv paracellulär diffusion och lipofila föreningar och små hydrofoba molekyler övervägande passerar genom paracellulär transport.4 Cellmembranet fungerar således som den viktigaste transportbarriären för hydrofila föreningar, och de intercellulära utrymmena utgör den viktigaste barriären för permeation av lipofila föreningar.

Vikten av mucoadhesion
Mucoadhesion är när två ytor, varav den ena är ett slemhinnemembran, fäster vid varandra. Det är en kritisk parameter för buccal administrering och formuleringsmaterial med optimala adhesiva egenskaper som ska väljas. Mucoadhesion sker i två steg – kontaktsteget följt av konsolideringssteget när adhesiva interaktioner etableras. Det finns sannolikt flera olika mekanismer som orsakar vidhäftning. Det är viktigt att adhesiva ledbrott inträffar som ett resultat av överhydrering av en doseringsform, eller som ett resultat av epitel- eller slemhinneomsättning. Omsättningstiden för det buccala epitelet har uppskattats till 3-8 dagar jämfört med cirka 30 dagar för huden.4

Ställets fördelar
Förutom den stora fördelen med systemisk tillförsel som kringgår lever- och tarmnedbrytning för större biotillgänglighet och mindre biverkningar har munnen en relativt stor yta för läkemedelstillförsel och god tillgänglighet jämfört med näsan, ändtarmen och slidan.5 Dessutom minskar den snabba cellomsättningen i munslemhinnan risken för vävnadsskador eller irritation.6 Även om den sublinguala slemhinnan är mer genomsläpplig, vaskulariserad och tunnare än den buckala slemhinnan är ytan på denna slemhinna mindre, den tvättas ständigt av saliven och den skjuvning som tungan utövar gör det svårt att hålla doseringsformen i kontakt med den sublinguala slemhinnan.7 Av alla dessa skäl är kindmucosan en föredragen plats i munhålan för administrering av system med kontrollerad frisättning som måste hålla sig kvar under en längre tidsperiod.8
Sitebegränsningar
Förbättring av absorptionshastigheten (μg/mm2/s) eller permeabiliteten hos den buckala vävnaden är ofta nödvändig för att kompensera för den begränsade yta som finns tillgänglig. Användningen av permeationsförstärkare (dvs. ämnen som omorganiserar epidermis- eller epitelstrukturen eller öppnar de intercellulära täta junkterna) är mycket viktig på detta område. Makromolekyler är mer komplicerade att leverera genom slemhinnan på grund av enzymatisk nedbrytning i saliven och dålig permeation genom buccalepitelet utan kemiskt och elektriskt baserad permeationsförbättring.9 Felaktig användning av permeationsförstärkare kan ge upphov till säkerhetsproblem när det gäller lokal vävnadsirritation men också som ett resultat av en oönskad bolus-effekt som driver upp koncentrationen av läkemedel i blodet till nivåer som inte är säkra.
En alternativ strategi för att säkerställa högre absorption av svårlösliga eller permeabla läkemedel i vävnaden är att öka uppehållstiden i munnen. Liksom med permeationsförstärkare kan en ökad uppehållstid orsaka irritation i vävnaden samt obehag för patienten och kräver en noggrann utvärdering av både omedelbara och långsiktiga effekter på vävnadsintegritet och funktionalitet. Att öka uppehållstiden i munhålan kan dessutom vara en utmaning eftersom läkemedlet snabbt kan elimineras på grund av salivens spolande verkan. Därför kan upprepade och frekventa doser behövas, om inte doseringsformen skapar ett starkt band med den absorberande slemhinnan. Det behövs forskning för att kvantifiera hur mycket spottspolning påverkar effektiviteten av oral transmucosal leverans från olika läkemedelsleveranssystem.
Mänskliga faktorer är viktiga att ta hänsyn till när man utvecklar en buccal produkt. Med tanke på att den buckala slemhinnan sträcker sig från de övre och nedre utrymmena mellan kinderna, läpparna och tandköttet, kan den exakta platsen där patienten placerar doseringsformen påverka vidhäftningen och absorptionen av läkemedlet, och dessa mänskliga faktorers implikationer kan påverka variabiliteten mellan patienterna. Hur doseringsformen placeras kan orsaka ytterligare komplikationer när doseringsformen är utformad för enkelriktad frisättning och har en specifik vidhäftande sida som ska placeras mot den inre kinden. Slutligen kan när och vad patienten äter, dricker eller röker ytterligare påverka absorptionen av läkemedlet genom slemhinnan.
Risken för dislokation och patientvariabilitet på grund av salivstimulering kan minimeras om läkemedlet administreras över natten till exempel när patienten inte äter eller talar.
Buccala doseringsformer
Och även om buccalslemhinnan först nu studeras ingående som en ny väg för läkemedelstillförsel, har dess potential för läkemedelstillförsel varit känd för mänskligheten i århundraden. Amerikanska urinvånare introducerade tuggtobak till europeiska bosättare på 1500-talet, och kokablad tuggades för 8 000 år sedan av peruanska skogsarbetare. Bukalslemhinnan har varit föremål för konventionella doseringsformer, t.ex. tabletter, trokéer och sugtabletter samt munsköljning och sprayer, och flera sådana produkter finns för närvarande på marknaden. Utmaningen ligger i att hålla dessa doseringsformer på platsen för absorption, doseringsnoggrannhet (vätskor) och obehag (tabletter). Tabletter har potential att lossna från slemhinnan, sväljas och sedan fästa vid matstrupens vägg och orsaka kvävningsrisk, särskilt för barn och äldre.
Mer avancerade system för läkemedelstillförsel, som filmer, plåster, tvåskiktstabletter, hydrogeler och tejper, tillsammans med användning av mikro- och nanopartiklar, håller på att utvecklas för att övervinna begränsningarna hos konventionella doseringsformer.
FILMER FÖR BUCKAL AVLÄGGNING – CUREFILM
Mukoadhesiva filmer är en föredragen doseringsform för administrering via buccalslemhinnan med tanke på deras flexibilitet, komfort, smaklighet och justerbara storlek. De har visat sig ha förbättrad följsamhet hos patienterna jämfört med vidhäftande tabletter.10,11 I motsats till flytande, gel- och salvaformuleringar förblir mucoadhesiva filmer i kontakt med slemhinnan längre, täcker en större yta och ger därför en mer exakt läkemedelsdosering.12 Mucoadhesiva filmer kan faktiskt utformas genom ett noggrant materialval så att de upprätthåller en omfattande vidhäftande kontakt med slemhinnan, vilket förlänger kvarhållstiden för leveranssystemet för ökad total läkemedelsabsorption. Dessutom är mucoadhesiva filmer väl lämpade för lokal terapi och skyddar till exempel sårytor i munnen från infektion.13
Filmsammansättningar utformas för att uppnå följande fysiska egenskaper: bioadhesiv styrka, draghållfasthet, smidighet, flexibilitet och förlängd sönderdelning. Dessa egenskaper är avgörande för att uppnå målprofilen för läkemedelsfrisättning, patientens acceptans och kompatibilitet med kommersiella tillverkningsprocesser. Att uppnå målspecifikationerna för buccala polymerfilmer är i hög grad beroende av typen och koncentrationen av de valda polymererna och den dos av aktiva beståndsdelar som levereras.
Som diskuterats här, även med en starkt vidhäftande film, kommer salivspolningen att leda till att en del av filmen löses upp i munhålan och sväljs. Dubbelskiktsfilmer med ett ocklusivt stödskikt har utformats för att driva enkelriktad läkemedelsfrisättning och absorption i munslemhinnan och kan leverera höga doser av aktiv substans. Även om sådana konstruktioner kan förbättra absorptionen i munnen har de flera nackdelar. De kan leda till användarfel vid tillämpningen, det ocklusiva lagret kan lossna och bli en kvävningsrisk, och slutligen driver komplexiteten i att skala upp en film med två lager upp tillverkningskostnaderna.
Med hänsyn till dessa begränsningar utnyttjar CURE Pharmaceuticals tillvägagångssätt för utveckling av buccalfilmer med CUREfilm den oundvikliga salivspolningen av en film med ett enda lager för att skapa bättre profiler för läkemedelsfrigörande. Vi utformar våra produkter för att kombinera den snabba bolus-effekten från buccal administrering med den förlängda frisättningen från GI-administrering för att uppnå en övergripande pulsatil eller långvarig frisättningsprofil. Med buccal administrering kan blodnivåerna nå en snabb topp och en kortare halveringstid kan innebära att effekten avtar snabbt. Om höga doser av ett läkemedel enbart ges via munnen (t.ex. över 100 mg) kan den lokala vävnadskoncentrationen bli för hög och skada vävnaden. Ett tillvägagångssätt med ett enda lager är att föredra eftersom det minimerar kostnader och användarfel.
För att skapa en buccal CUREfilm kombineras en noggrant utvald blandning av polymerer, permeationsförstärkare och lipider för att optimera vidhäftning, läkemedelsdiffusion och permeation genom slemhinnan. Lipider spelar en avgörande roll för lösliggörandet och stabiliteten hos aktiva ingredienser. De hjälper till att driva hydrofila föreningar genom slemhinneepitelet och främjar transcellulär transport av lipofila föreningar genom epitelet för att nå blodkärlen. Nanopartikulering av den aktiva beståndsdelen kan ge ytterligare en pil i formulatörens koger för att öka absorptionshastigheten.
För att uppnå ett tillräckligt magsäcksskydd och en effektiv intestinal frisättning av den del av läkemedlet som sväljs kan läkemedelspartiklar vara helt eller delvis inkapslade, enteriskt belagda eller tvärbundna till polymerer, som t.ex. kitosan, innan de införlivas i filmmatrisen. Andra strategier inkluderar liposomal eller micellär bildning, samkristallisering och användning av gelande eller svällbara polymerer.
Denna dubbla strategi kan vara mycket användbar för kombinationsläkemedel med olika metaboliska profiler där det ena läkemedlet förbereds för buccal absorption (dvs. om det har en hög förstapassagerande effekt), och det andra förbereds för frisättning i GI.
SAMMANFATTNING
Den faktiska utformningen och konstruktionen av en oral film som kan ge effektiv terapeutisk tillförsel kan vara en utmaning och kräver skapandet av ny teknik. Som ett resultat av dessa innovationer är buckala filmer nu en kommersiellt gångbar doseringsform som kan lösa många problem som läkemedelsindustrin, patienter och deras vårdgivare står inför. De kommer att kunna ersätta dagliga injektioner, t.ex. apomorfinininjektioner som tas av patienter som lider av Parkinsons sjukdom. De kan förbättra biotillgängligheten hos läkemedel, t.ex. cannabinoider, och på så sätt potentiellt sänka deras doser och psykoaktiva biverkningar. När snabb symtomlindring behövs kan de ge en bolus-effekt. De är ett bekvämt alternativ till osmakliga vätskor för barn och piller som är svåra att svälja för äldre.
Med tanke på de viktiga behov som de tillgodoser på marknaden har oral film blivit mycket populär. Faktum är att den globala marknaden värderades till 2,1 miljarder dollar 2017 och förväntas expandera med en CAGR på 13 % under prognosperioden från 2018 till 2026.14 Denna kommersiella tillväxt av orala filmer, inklusive buccalfilmer, återspeglar läkemedelsindustrins ökade fokus på patientcentrerad innovation vid utveckling av nya läkemedel och förbättring av gamla läkemedel – där patientens erfarenhet styr utformningen av läkemedelsleveranserna, vilket i sin tur förbättrar patientens resultat.
- Curatolo W. The lipoidal permeabilitetsbarriärer i huden och matsmältningskanalen. Pharm Res. 1987;4(4):271-277.
- Colombo P, Cagnani S, Buttini F, Santi P, et al. Biological In Vitro Models for Absorption by Non-Oral Routes, Reference Module in Chemistry, Molecular Sciences and Chemical Engineering, Elsevier. 2013.
- Kulkarni U, Mahalingam R, Pather SI, Li X, Jasti B. Porcine buccal mucosa as an in vitro model: relative contribution of epithelium and connective tissue as permeability barriers. J Pharm Sci. 2009;98(2):471-483. doi: 10.1002/jps.21436.
- Gandhi RB, Robinson JR. Oral cavity as a site for bioadhesive drug delivery Adv Drug Deliv Rev. 1994;13:43-74.
- Rathbone MJ, Drummond BK, Tucker IG. Munhålan som plats för systemisk läkemedelstillförsel Adv Drug Deliv Rev. 1994;13:1-22.
- Squier CA, Wertz PW. Structure and Function of the Oral Mucosa and Implications for Drug Delivery M.J. Rathbone (Ed.), Oral Mucosal Drug Delivery, Marcel Dekker, New York. 1996:1-26.
- Madhav NVS, Shakya AK, Shakya P, Singh K. Orotransmucosal drug delivery systems: a review. J Control Release. 2009;140:2-11.
- Madhav NVS, Shakya AK, Shakya P, Singh K. Orotransmucosal drug delivery systems: a review J Control Release. 2009;140:2-11.
- Morales JO, Brayden DJ. Buccal delivery of small molecules and biologics: of mucoadhesive polymers, films, and nanoparticles. Current Opinion Pharmacol. 2017;36:22-28.
- Kraisit P, Limmatvapirat S, Nunthanid J, et al. Framställning och karakterisering av hydroxipropylmetylcellulosa/polykarbofil mucoadhesiva blandfilmer med hjälp av en blandningsdesign Chem Pharm Bull. 2017;65(3):284-294.
- Giovino C, Ayensu I, Tetteh J, et al. Utveckling och karakterisering av kitosanfilmer impregnerade med insulinladdade PEGb-PLA-nanopartiklar (NP): ett potentiellt tillvägagångssätt för buccal leverans av makromolekyler. Int J Pharm. 2012;428(1-2):143-151.
- Abruzzo A, Bigucci F, Cerchiara T, et al. Mucoadhesive chitosan/gelatinfilmer för buccal leverans av propranololhydroklorid. Carbohydr Polym. 2012;87(1):581-588.
- Tejada G, Lamas MC, Svetaz L, Salomón CJ, Alvarez VA, et al. Effekten av tekniken för inkorporering av läkemedel och polymerkombination på prestandan hos biopolymeriska svampdödande buccalfilmer. Int J Pharmaceut. 2018;548(1):431-442.
- Transparency Market Research (TMR) report. Oral Thin Films Market – Global Industry Analysis, Size, Share, Growth, Trends, and Forecast, 2018-2026.

Robert Davidson är CURE:s vd och Chariman of the Board of Directors. Före sin roll på CURE Pharmaceutical har han varit ordförande och verkställande direktör för InnoZen Inc., verkställande direktör för Gel Tech LLC, verkställande direktör för Bio Delivery Technologies Inc. och har suttit i flera bolagsstyrelser. Davidson var ansvarig för utvecklingen av flera tekniker för läkemedelsleveranser och kommersiella varumärkesutvidgningar. Han har en magisterexamen i tillämpad projektledning från Villanova University, en magisterexamen i folkhälsa från American Military University, Virginia och en magisterexamen i hälsa och välbefinnande från Liberty University, Virginia. Davidson avslutade också sina forskarstudier vid University of Cambridge med en berömlig utmärkelse.

Jessica Rousset är CURE:s operativa chef. Rousset övervakar verksamheten och driver företagets strategi och tillväxt. Rousset har tidigare varit chef för innovation vid Children’s Hospital Los Angeles, där hon under en tioårsperiod hjälpte till att starta både terapeutiska och medicintekniska företag samt grundade och drev en nationell accelerator för pediatrisk teknik. Dessförinnan hade Rousset arbetat på The Scripps Research Institute och GlaxoSmithkline Biologicals i roller inom laboratorier, klinisk forskning och affärsutveckling. Hon utbildade sig till biokemisk ingenjör vid Institut National des Sciences Appliquées i Lyon, Frankrike.
Lämna ett svar