Palavras-chave
CADASIL – AVC – IRM
Introdução
Arteriopatia dominante autossômica cerebral com infartos subcorticais e Leucoencefalopatia (CADASIL) é uma doença hereditária de pequenas artérias causada por diferentes mutações patogênicas do gene NOTCH-3. Caracteriza-se pela associação da enxaqueca com a aura, sintomas psiquiátricos, eventos isquémicos recorrentes em idades precoces e comprometimento cognitivo. Este e seus típicos achados radiológicos é o que normalmente nos ajuda a suspeitar da doença. Geralmente é considerada uma doença de adultos jovens e de meia-idade, mas os casos em idosos podem ser subdiagnosticados. Relatamos o caso de um homem que foi diagnosticado com CADASIL no final dos anos setenta graças ao diagnóstico anterior da sua filha.
Casos
Caso 1
A filha da nossa paciente tinha 50 anos de idade quando foi enviada ao nosso hospital do ambulatório de neurologia para estudo posterior, devido aos achados radiológicos em sua ressonância magnética do cérebro, que consistiu em alterações da matéria branca em ambas as cápsulas externas, áreas periventriculares bilaterais e lobo temporal esquerdo.
A paciente freqüentava o referido consultório por ter sofrido enxaqueca com aura visual por 30 anos, com alguns episódios sugerindo aura visual sem dor de cabeça. Ela não apresentava outros sintomas. Ela era alérgica à fosfomicina e tinha sido submetida a amigdalectomia quando era criança. Ela não tinha nenhum outro histórico médico passado. Sua história familiar era notável: sua mãe tinha enxaqueca e demência leve e seu pai teve um derrame aos 75 anos de idade; seu avô paterno, tio e tia tinham tido derrames, e o tio tinha sido diagnosticado com doença de Alzheimer, um primo paterno tinha recebido em outro lugar o diagnóstico de “vasculite ANA+” e outro primo paterno tinha sido diagnosticado com esclerose múltipla. Ela tinha dois filhos saudáveis. O exame físico, incluindo uma meticulosa exploração neurológica, era completamente normal. A RM repetida do cérebro mostrou múltiplas lesões hiperintensas na matéria branca das áreas de protuberância posterior, periventricular e subcortical, incluindo os lobos temporais anteriores, especialmente o esquerdo, ambos semovalentes centrais, cápsulas internas e externas, sem sinais de microblemas recentes ou passados (figura 1). Todos os outros exames, incluindo hemograma, glucemia, função hepática e renal, taxa de sedimentação eritrocitária, hormônios séricos da tireóide, triagem de hipercoagulabilidade, triagem de vasculite, eletrocardiograma, radiografia de tórax, sífilis e sorologias de HIV, e ultra-sonografia de troncos supraaórticos com Doppler, estavam normais, exceto para uma colesterolemia de 220 mg/dl com colesterol LDL de 152 mg/dl. A biópsia da pele também foi normal. Foi encontrada uma mutação Arg169Cys (substituição da citosina pela timina no códon 505) no quarto exon do gene NOTCH 3, que é conhecido por ser patogênico, então ela foi diagnosticada com CADASIL. Com este diagnóstico, ambos os pais foram avaliados em nossa clínica.
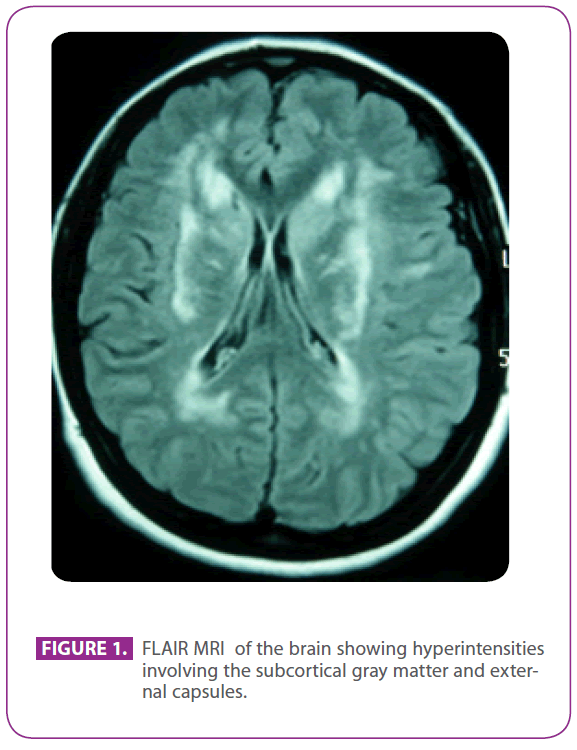
Figura 1: RM do cérebro com hiperintensidades envolvendo a matéria cinzenta subcortical e cápsulas externas.
Caso 2
Sua mãe tinha 78 anos de idade. Ela tinha uma longa história de enxaqueca sem aura e, nos últimos dois anos, desenvolveu uma demência leve com parkinson simétrico, flutuações e distúrbio do comportamento do sono REM, sugestivo de demência com corpos Lewy. A RM do cérebro descartou doença relevante da matéria branca.
O seu pai era um homem de 79 anos com vários fatores de risco vascular: diabetes mellitus tipo 2, dislipidemia e tabagismo há 50 anos, com um índice acumulado de 15 maços de anos, embora ele tivesse parado há 3 anos. Ele tinha doença cardíaca isquêmica com um infarto póstero-inferior do miocárdio em 1991. Nos últimos 8 anos teve três acidentes isquêmicos transitórios e um acidente vascular cerebral lacunar correspondente a diferentes territórios arteriais, com dificuldade de marcha progressiva, e nos últimos 6 meses havia se tornado um pouco retraído e apático. Ele não tinha histórico de enxaqueca. Estava a tomar metformina, clopidogrel, atenolol e atorvastatina. Ao exame físico estava consciente e orientado, mas um pouco desatento, a linguagem e a memória remota e recente eram normais, mostrava apraxia ideomotora, alteração da semelhança e interpretação dos ditos, sem reflexos de libertação frontal. Também mostrou hiperreflexia global com reflexos plantares flexores bilaterais, e marcha com passos curtos e movimentos reduzidos dos braços. A tomografia computadorizada realizada dois anos antes, após um de seus ataques isquêmicos transitórios, mostrou extensa doença de matéria branca, especialmente proeminente na cápsula externa e lobos temporais (figura 2).
Summing up, o paciente apresentava derrames isquêmicos recorrentes, leve comprometimento cognitivo subcortical e leucoencefalopatia, altamente desconfiado do CADASIL considerando o diagnóstico de sua filha. Foi realizado um teste genético, que mostrou a mesma mutação NOTCH 3 que a filha e confirmou o diagnóstico.
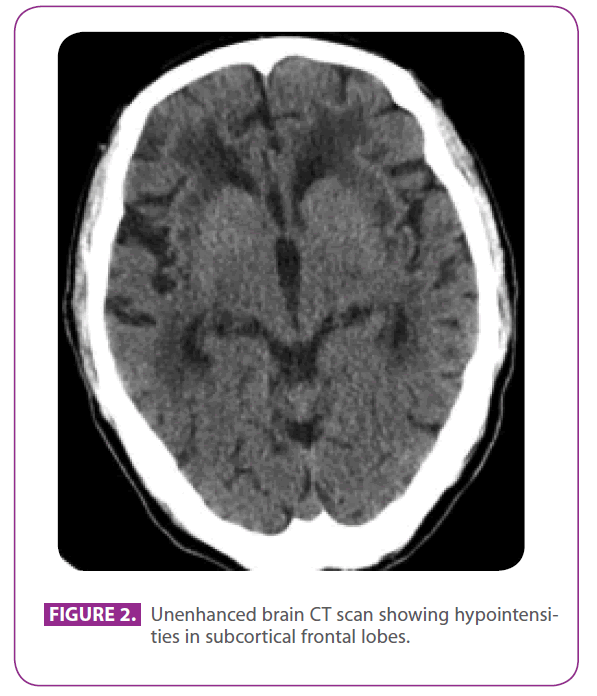
Figure 2: TC cerebral não melhorado mostrando hipointensidades nos lobos frontais subcorticais.
Discussão
CADASIL é a doença hereditária mais comum em pequenos vasos. No entanto, também pode ser esporádica, como já foram descritas as mutações de novo. Ela é causada por diferentes mutações patogênicas no gene NOTCH-3, que está situado no cromossomo 19, locus 19p13.2-p13.1, e consiste em 33 exons que codificam uma proteína de 2321 aminoácidos (1). Esta proteína é um receptor de superfície celular transmembrana de passo único expresso em células musculares lisas sistêmicas, com um domínio regulador extracelular e um domínio transdutor intracelular. Há mais de 190 mutações relatadas até o momento que podem levar ao CADASIL, e todas elas ocorrem nos exons 2 a 24 do gene NOTCH 3, que codificam as 34 repetições de fator de crescimento epidérmico da porção extracelular do NOTCH 3. Portanto, o rastreamento desses 23 exons tem 100% de sensibilidade e quase a mesma especificidade (2). Destas mutações, mais de 180 são mutações de falta de sentido, pelo menos 6 deleções, uma inserção, uma mudança de imagem e 2 duplicações. A maioria das mutações patogênicas NOTCH3 ocorre nos exons 3 e 4 (3).
Todas as mutações resultam na adição ou perda de um resíduo de cisteína em uma repetição semelhante ao EGF, e portanto um número ímpar de resíduos de cisteína que produz a formação de pontes de dissulfeto anormais. A NOTCH3 mutante causa degeneração das células lisas vasculares em pequenas artérias e arteríolas e acúmulo da proteína anormal na parede desses vasos, levando à estenose luminosa (1). No cérebro afeta a penetração das artérias cerebrais e leptomeníngeas, provocando a incapacidade destes vasos em auto-regular e hipoperfusão dos territórios irrigados por eles, e portanto infartos na matéria branca.
O primeiro sintoma do CADASIL, ao se apresentar, é geralmente enxaqueca com aura, com um início médio de idade de 30 anos. Aparece em 20 a 40% dos pacientes (4). A maioria dos ataques é típica com aura visual ou sensorial, mas metade dos pacientes também tem ataques atípicos com aura basilar, hemiplégica ou prolongada.
Agastos isquêmicos subcorticais, ataques transitórios ou AVC, aparecem em 60 a 85% dos pacientes, o primeiro com idade média de 50 anos, embora possa ocorrer logo na segunda década. Na maioria das vezes não há fatores de risco vascular convencional ou estes não são muito importantes. Em dois terços dos pacientes, os eventos isquêmicos apresentam-se clínica e radiologicamente como síndromes lacunares. A maioria das pacientes tem vários AVC, geralmente 2 a 5, levando em vários anos a dificuldades de marcha, incontinência urinária e fecal, demência e paralisia pseudobulbar (1). O comprometimento cognitivo é a segunda manifestação clínica mais freqüente. O sinal mais precoce é geralmente o comprometimento das capacidades executivas e da velocidade de processamento, que está presente na maioria dos pacientes com mais de 35 anos, mas pode aparecer logo na primeira década de vida (5). Esse comprometimento cognitivo é progressivo e normalmente piora com os acidentes vasculares cerebrais recorrentes, com a adição de comprometimento nas atividades instrumentais, memória, linguagem, raciocínio e habilidades visuoespaciais. Mais de 70% dos pacientes são dementes até a sexta década de vida. Afasias graves, apraxia ou agnosia são raras no CADASIL.
Psiquiátricos, principalmente distúrbios de humor, aparecem em 20% dos pacientes, em geral como episódios depressivos graves. A apatia está presente em 40% dos pacientes e não se relaciona com a depressão Outras manifestações clínicas menos comuns são a encefalopatia reversível aguda (6) (em 10% dos pacientes), a maioria delas ocorrendo após uma enxaqueca com aura, convulsões (em 5 a 10% dos pacientes), surdez, parkinson, hemorragias cerebrais (principalmente em pacientes com pressão alta), e infarto do miocárdio.
Embora penetre completamente, o CADASIL tem uma importante variabilidade de expressão clínica inter e intrafamiliar. A mesma mutação NOTCH-3 tem um amplo espectro clínico, sem diferenças claras entre pacientes homozigotos e heterozigotos. Na verdade, não há correlação entre genótipo e fenótipo clínico (4). A razão dessas diferenças não é conhecida, mas alguns possíveis modificadores fenotípicos do CADASIL têm sido descritos, como tabagismo atual por risco de AVC e idade do primeiro AVC, pressão arterial alta por risco de AVC, ou níveis de homocisteína por idade de início de enxaqueca (3,4). Esses e outros fatores podem influenciar a expressão clínica da doença modificando a expressão gênica ou afetando outras vias fisiopatológicas que podem levar às mesmas manifestações clínicas.
As alterações radiológicas aparecem em todos os indivíduos com mutação CADASIL antes dos 35 anos de idade e aumentam com o tempo. As características mais precoces e freqüentes são as áreas não-puntiformes hiperintensas em matéria branca cerebral e estruturas subcorticais em T2 e as imagens de recuperação de inversão de RM com atenuação de fluidos. O envolvimento de cápsulas externas e da parte anterior dos lobos temporais é típico desta doença e uma pista para o diagnóstico, pois ajudam no diagnóstico diferencial com outras condições como a doença de pequenos vasos (1).
CADASIL é comumente considerada uma doença de adultos jovens e de meia idade, mas o número de pacientes idosos pode ser subdiagnosticado (7,8). Nosso segundo caso pode servir de exemplo: um paciente de 79 anos com fatores de risco vascular e acidente vascular cerebral recorrente, com doença da matéria branca que foi considerada secundária à doença de pequenos vasos por vários neurologistas. O diagnóstico só foi feito após o conhecimento da mutação de sua filha. Em casos sem história familiar clara, uma mente aberta e atenção cuidadosa aos achados radiológicos sugestivos, como o envolvimento da cápsula externa ou lobos temporais anteriores, pode ser a única pista para um diagnóstico correto.
- Chabriat H, Joutel A, Dichgans M, Tournier-Lasserve E, Bousser MG. Cadasil. Lancet Neurol 2009; 8:643-53.
- Vazquez do Campo R, Morales-Vidal S, Randolph C, Chadwick L, Biller J. CADASIL: uma série de casos de 11 pacientes. Rev Neurol. 2011; 52:202-10.
- Adib-Samii P, Brice G, Martin RJ, Markus HS. Espectro clínico do CADASIL e o efeito dos fatores de risco cardiovascular no fenótipo: estudo em 200 indivíduos recrutados consecutivamente. Stroke 2010; 4:630-4.
- Singhal S, Bevan S, Barrick T, Rich P, Markus HS. A influência dos fatores de risco genéticos e cardiovasculares no fenótipo CADASIL. Cérebro. 2004; 127:2031-8.
- Dichgans M, Markus HS, Salloway S, Verkkoniemi A, Moline M, Wang Q, Posner H, Chabriat HS. Donepezil em pacientes com comprometimento cognitivo vascular subcortical: um ensaio aleatório duplo-cego em CADASIL. Lancet Neurol. 2008;7:310-8.
- Schon F, Martin RJ, Prevett M, Clough C, Enevoldson TP, Markus HS. “CADASIL coma”: uma encefalopatia aguda subdiagnosticada. J Neurol Neurocirurgia Psiquiatria. 2003;74:249-52.
- Liem MK, Lesnik Oberstein SA, Vollebregt MJ, Middelkoop HA, van der Grond J, Helderman-van den Enden AT. Homozigosidade para uma mutação NOTCH3 num paciente CADASIL de 65 anos com sintomas ligeiros: um relatório familiar. J Neurol. 2008 ;255:1978-80.
- Lee YC, Yang AH, Soong BW. A expressividade notavelmente variável do CADASIL: relato de um homem minimamente sintomático em uma idade avançada. J Neurol. 2009;256:1026-7
Deixe uma resposta