- O que são os corticoides?
- Corticoides e cortisol
- Tipos
- Doenças que podem ser tratadas com corticoides
- Absorção sistêmica
- Efeitos colaterais
- Efeitos colaterais na pele
- Efeitos colaterais nos olhos
- Efeitos metabólicos
- Efeitos cardiovasculares
- Efeitos musculoesqueléticos
- Efeitos colaterais no sistema nervoso central
- Efeitos imunológicos
- Outros efeitos
- Cuidados e perigos do uso de corticoides
- Referências
O que são os corticoides?
Os glicocorticoides, também chamados de corticoides ou corticosteroides, são fármacos poderosos, derivados do hormônio cortisol, que é produzido pela glândula suprarrenal.
Os corticoides são frequentemente usados como parte do tratamento de doenças de origem inflamatória, alérgica, imunológica e até contra alguns tipos de câncer.
Apesar de ser um medicamento muito eficaz contra várias doenças graves, os corticoides apresentam um grande defeito: um perfil muito extenso de efeitos colaterais, alguns deles graves, outros esteticamente indesejáveis.
Quando usados de forma prolongada, os corticoides levam ao ganho de peso, podem causar estrias, provocam acne, enfraquecem os ossos, aumentam o risco de infecções, etc.
Neste artigo iremos tratar das indicações e dos efeitos colaterais dos corticoides, com especial ênfase na prednisona e prednisolona, as drogas mais usadas desta classe.
Se você procura por uma bula simplificada da prednisona, acesse o seguinte artigo: PREDNISONA – Para Que Serve, Doses e Cuidados
Para informações sobre o uso de corticoides na COVID-19, acesse os seguintes artigos:
- DEXAMETASONA – BULA PARA PACIENTES.
- INFORMAÇÕES SOBRE A COVID-19.
Corticoides e cortisol
Os glicocorticoides são hormônios esteroides, não-anabolizantes e não-sexuais, produzidos pelo córtex da glândula supra-renal. O hormônio produzido naturalmente pelo nosso organismo é o cortisol.
Níveis normais de cortisol são essenciais para a nossa saúde, pois este hormônio tem ação no metabolismo da glicose, nas funções metabólicas do organismo, na cicatrização, no sistema imune, na função cardíaca, no controle do crescimento e em muitas outras ações básicas do nosso corpo.
O cortisol é um hormônio de estresse, pois sua produção eleva-se toda vez que o nosso organismo encontra-se sob estresse físico, como nos casos de traumatismos, infecções ou cirurgias. O cortisol aumenta a disponibilidade de glicose e energia, eleva a pressão arterial, aumenta o tônus cardíaco e prepara o organismo para sofrer e combater insultos.
Tipos
Os glicocorticoides usados na prática médica são versões sintéticas, produzidas laboratorialmente, do hormônio natural cortisol.
Existem várias formulações sintéticas de corticoides, as mais usadas são a prednisona, prednisolona, hidrocortisona, dexametasona, metilprednisolona e beclometasona (via inalatória).
Todo os corticoide sintético é mais potente que o cortisol natural, exceto pela hidrocortisona, que apresenta uma potência semelhante.
Potência de cada tipo de corticoide em relação ao cortisol:
- Hidrocortisona → potência semelhante ao cortisol.
- Deflazacorte → 3 vezes mais potente que o cortisol.
- Prednisolona → 4-5 vezes mais potente que o cortisol.
- Prednisona → 4-5 vezes mais potente que o cortisol.
- Triancinolona → 5 vezes mais potente que o cortisol.
- Metilprednisolona → 5-7.5 vezes mais potente que o cortisol.
- Betametasona → 25-30 vezes mais potente que o cortisol.
- Dexametasona → 25-30 vezes mais potente que o cortisol.
- Beclometasona (inalatória) → 8 pufs 4 vezes por dia equivale a 14 mg de prednisona oral diária.
60 mg de prednisona apresentam o mesmo efeito de 2 mg de dexametasona ou 300 mg do cortisol natural. Devido a essa potência maior dos corticoides sintéticos, conseguimos administrar nos pacientes doses muito acima dos níveis fisiológicos do cortisol, o que é essencial para o tratamento de algumas doenças.
Doenças que podem ser tratadas com corticoides
A prednisona e os corticoides em geral são drogas que conseguem modular processos inflamatórios e imunológicos do nosso organismo, tornando-se extremamente úteis em uma infinidade de doenças. Qualquer doença de origem alérgica, inflamatória ou autoimune pode ser tratada com algum desses corticoides (leia também: O QUE É UMA DOENÇA AUTOIMUNE?).
Só para se ter uma ideia da importância dos corticoides na prática médica, podemos citar como indicação para a sua administração as seguintes doenças:
- Asma.
- Esclerose múltipla.
- DPOC.
- Alergias, principalmente anafilaxias.
- Hepatite autoimune.
- Herpes Zoster.
- Lúpus.
- Artrite reumatoide.
- Leucemia.
- Linfoma.
- Púrpura trombocitopênica idiopática (PTI).
- Mieloma múltiplo.
- Edema cerebral.
- Paralisia facial de Bell.
- Gota.
- Sarcoidose.
- Rinite alérgica.
- Vitiligo.
- Psoríase.
- Granulomatose de Wegener.
- Doença inflamatória intestinal.
- Miastenia Gravis.
- Vasculites.
- Doença de Addison (insuficiência adrenal).
- Glomerulonefrites.
- Doenças de pele de origem inflamatória ou autoimune.
- Síndrome de Sjögren.
- Transplante de órgãos.
- Urticária.
As doses diárias equivalentes a 5-10 mg de prednisona são chamadas de doses fisiológicas por serem compatíveis com a produção diária natural de cortisol. Nestas doses, os corticoides sintéticos apresentam apenas efeito anti-inflamatório.
Em situações normais, a secreção de cortisol pela suprarrenal apresenta um ciclo circadiano, ou seja, sofre alterações de acordo com o período do dia. Durante as primeiras horas da manhã, a sua secreção está muito elevada, reduzindo-se ao máximo por volta das 23 horas. Por isso, optamos por administrar os corticoides durante a parte da manhã para tentar simular a secreção fisiológica que o organismo está habituado, diminuindo, assim, a incidência de efeitos colaterais.
Conforme a dose vai sendo elevada, a prednisona, ou qualquer outro glicocorticoide, começa a apresentar efeitos imunossupressores, o que justifica os seu uso nas doenças autoimunes e no transplante de órgãos.
Nas doenças autoimunes e glomerulonefrites podemos usar até 80 mg de prednisona por dia. Em casos graves, lançamos mão de um procedimento chamado pulsoterapia, que consiste na administração venosa de até 1000 mg de metilprednisolona por 3 dias seguidos. Essa pulsoterapia pode ser usada em vasculites severas, em casos de rejeição de órgãos transplantados e no tratamento de doenças autoimunes graves e descompensadas, como ocorre em alguns casos de Lúpus, por exemplo.
Os corticoides podem ser administrados por várias vias. Por exemplo, corticoides sistêmicos são aqueles tomados por via oral ou via intravenosa. Na asma é muito comum a administração do corticoide inalatório. Na rinite e sinusite a via preferencial é a intranasal. Nas doenças de pele, o corticoide é tópico, ou seja, em cremes ou pomadas. Pode haver corticoides em colírios e em soluções para administração nos ouvidos. Nas artrites, a via pode ser intra-articular (infiltração).
Absorção sistêmica
A imensa maioria dos efeitos colaterais ocorre nos pacientes que fazem uso prolongado e com doses elevadas de corticoides por via oral ou intravenosa. Isso não significa, porém, que as outras formas de administração de corticoides seja isenta de efeitos adversos.
Corticoides por via inalatória, muito usados no tratamento da asma, podem ter relevante absorção sistêmica, apesar desta ser bem menor do que a que ocorre com corticoides administrados por via oral. A fluticasona por via inalatória, por exemplo, reconhecidamente inibe a produção de cortisol pela suprarrenal e pode causar efeitos colaterais sistêmicos, quando usada seguidamente por vários meses, principalmente em crianças. Outras formas de corticoide inalatório parecem ter absorção sistêmica menor.
Injeções de dexametasona intra-articulares podem causar síndrome Cushing (explico o que é esta alteração mais à frente).
Mesmo os corticoides em pomada ou creme podem ser absorvidos pelo organismo de forma suficiente para provocar efeitos colaterais, caso o seu uso seja por tempo prolongado. A absorção do corticoide pela pele varia de acordo com alguns fatores. Por exemplo, áreas como as dobras cutâneas, couro cabeludo e a testa apresentam maior absorção. Nas crianças e em áreas com inflamação ou descamação da pele a absorção sistêmica dos corticoides também é maior.
Em geral, não existe forma de corticoide isenta de efeitos colaterais. Não importa a via, quanto maior for o tempo de tratamento e a dose utilizada, maior são os riscos de efeitos adversos.
Efeitos colaterais
Ao mesmo tempo que são drogas extremamente úteis em uma variedade de doenças graves, os corticoides apresentam, principalmente se usados a longo prazo, uma lista imensa de efeitos colaterais indesejáveis, que variam desde problemas estéticos até infecções graves por inibição do sistema imunológico.
Os efeitos colaterais estão intimamente relacionados à dose e ao tempo de uso. O uso esporádico e por pouco tempo não é capaz de levar aos efeitos adversos que serão descritos a seguir. Não é preciso se preocupar com a prescrição de corticoides por apenas uma semana, mesmo que este esteja em doses altas.
Toda vez que o uso de corticoides em doses elevadas ou por tempo prolongado for cogitado, é importante colocar na balança os possíveis benefícios e os prováveis efeitos. O uso estará indicado sempre que o médico julgar que a doença a ser tratada é mais grave que os potenciais efeitos adversos.
Após a leitura deste artigo você pode ficar com a impressão de que a prednisona e similares são drogas terríveis. É importante salientar que o uso prolongado e em doses elevadas só costuma ser indicado em doenças graves, que podem levar à morte ou a graves limitações.
Efeitos colaterais na pele
Os efeitos estéticos dos corticoides são os que mais incomodam os pacientes, principalmente as mulheres. Cerca de metade dos indivíduos que usam, pelo menos, 20 mg diários de prednisona, ou dose equivalente de qualquer outro corticoide por três ou mais meses irão apresentar efeitos colaterais estéticos.
Entre os mais comuns podemos citar a equimose e a púrpura associadas ao corticoide. Estas alterações são pequenas hemorragias que ocorrem em baixo da pele, normalmente em áreas expostas ao sol, como mãos e antebraços. Outro efeito adverso comum é uma pele mais fina e frágil.
Estrias de cor arroxeada localizadas na região abdominal, calvície, crescimento de pelos em mulheres e acne também ocorrem com frequências em usuários crônicos de corticoides por via oral.
O risco de cânceres de pele do tipo não-melanoma parece ser maior em pessoas que tomam corticoides por tempo prolongado.
Pacientes que fazem uso de corticoides em cremes e pomadas por longo tempo também podem apresentar efeitos indesejados na pele, como atrofia, estrias, teleangiectasias e manchas roxas. Um maior risco de infeções fúngicas na pele também ocorre com o tratamento prolongado.
Um sinal típico da toxicidade pelos corticoide é o desenvolvimento da aparência “cushingoide”, que se caracteriza por um face arredondada (chamada de fácies em lua), pelo acúmulo de gordura na região posterior do pescoço e das costas (chamado de corcova ou giba de búfalo) e pela distribuição irregular da gordura corporal, com predomínio na região abdominal e tronco.
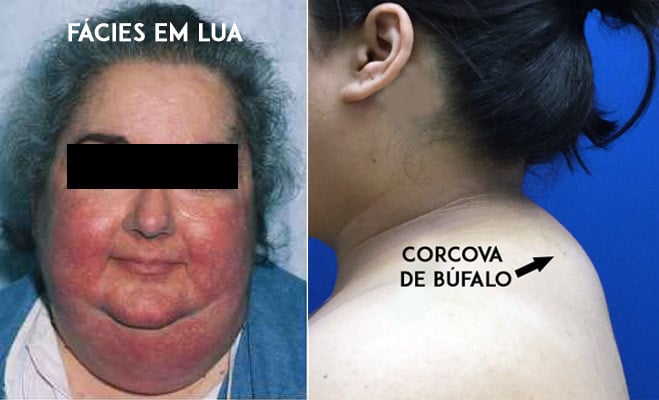
Esse conjunto de efeitos colaterais, chamado de síndrome de Cushing, é um dos mais incômodos, pois muda muito a aparência do paciente, principalmente nas pessoas que eram previamente magras.
A síndrome de Cushing surge, habitualmente, dentro dos dois primeiros meses de tratamento com corticoides em doses acima de 20 mg por dia. Em alguns pacientes, porém, doses acima de 10 mg por dia já são suficientes para provocar esta alteração.
Efeitos colaterais nos olhos
O uso contínuo de corticoides sistêmicos, normalmente por mais de 1 ano com doses maiores que o equivalente a 10 mg de prednisona por dia, pode levar a alterações oftalmológicas, como a catarata e glaucoma. Tanto os corticoides usados por via oral, por via nasal (spray nasal para asma ou bronquite) ou sob a forma de colírios podem causar ambas doenças.
Pacientes que fazem uso crônico de corticoides devem ser avaliados periodicamente por um oftalmologista, com o intuito de detectar sinais precoces de catarata ou glaucoma.
Efeitos metabólicos
A partir da dose de 5 mg por dia há uma clara tendência ao ganho de peso e acúmulo de gordura na região do tronco e abdômen. Quanto maior for a dose do corticoide, maior é o ganho de peso.
Além do acúmulo de gordura, a corticoterapia crônica também leva a alterações do metabolismo da glicose, podendo, inclusive, provocar diabetes mellitus. O risco é maior nos indivíduos que já apresentam valores de glicose ligeiramente alterados antes do início da corticoterapia. Apesar do diabetes ser reversível na maioria dos casos após a suspensão da droga, alguns pacientes permanecem diabéticos para o resto da vida.
Doses diárias de prednisona acima de 10 mg por mais de 3 meses também podem provocar alterações nos níveis de colesterol, nomeadamente elevações no colesterol LDL (colesterol ruim) e triglicerídeos, e redução dos níveis de colesterol HDL (colesterol bom).
Efeitos cardiovasculares
A incidência de várias doenças cardiovasculares costuma aumentar com o uso prolongado de corticoides. Podemos citar o aumento da ocorrência de hipertensão, infarto do miocárdio, insuficiência cardíaca e AVC.
O risco de doença cardiovascular depende da dose e do tempo de tratamento. Pacientes que desenvolvem síndrome de Cushing costumam ser os que apresentam a maior taxa de aterosclerose e maior risco de problemas cardíacos.
Doses pequenas de corticoides por pouco tempo não parecem aumentar o risco cardiovascular de forma relevante.
Efeitos musculoesqueléticos
O uso crônico de glicocorticoide está associado a diversas alterações músculo-esqueléticas. A mais comum é a osteoporose. Neste caso, mesmo doses baixas, como 2,5 mg ou 5 mg por dia, se usadas de forma crônica, podem acelerar a perda de massa óssea.
A corticoterapia prolongada também é responsável por aumento da incidência de necrose óssea, lesões musculares (miopatia), fraturas ósseas e distúrbios do crescimento, quando usado em crianças.
Efeitos colaterais no sistema nervoso central
O uso de corticoides, em um primeiro momento, pode causar uma sensação de bem-estar e euforia. Porém, a longo prazo ele está associado a uma maior incidência de quadros psiquiátricos, tais como psicose e depressão, além de insônia e alterações da memória.
Efeitos imunológicos
A imunossupressão causada pela corticoterapia é um efeito desejável nos casos das doenças autoimunes, mas pode também ser um grande problema, já que facilita a ocorrência de infecções. É preciso saber balancear bem os riscos com os benefícios.
O risco de infecção surge naqueles que tomam o equivalente a 10 mg por dia ou mais de prednisona por vários dias. Este risco torna-se muito elevado com doses acima de 40 mg por dia ou quando obtém-se uma dose acumulada de 700 mg de prednisona ao longo de todo o tratamento.
Além de facilitar infecções, os corticoides também inibem o surgimento da febre, dificultando o reconhecimento de um processo infeccioso em curso.
Doentes submetidos a altas doses de corticoides devem evitar vacinas compostas por vírus vivos, sob o risco de desenvolver infecções vacinais. Vacinas com vírus mortos podem ser administradas, porém, a corticoterapia também pode impedir a formação de anticorpos, fazendo com que a imunização apresente pouca eficácia. Muitas vezes são necessárias doses maiores para uma eficaz imunização.
A candidíase oral e a candidíase vaginal são infecções muito comuns nos pacientes que fazem uso crônico de glicocorticoides.
Outros efeitos
A lista de possíveis efeitos colaterais dos corticoides é muito extensa. Além dos que já foram citados, outros efeitos adversos relativamente comuns são: retenção de líquidos, alterações menstruais, gastrite, úlcera péptica, esteatose hepática, pancreatite e infertilidade.
Cuidados e perigos do uso de corticoides
A corticoterapia prolongada requer alguns cuidados, principalmente na hora de se suspender a droga.
O uso de prednisona ou similares por muito tempo, inibe a produção natural de cortisol pela glândula suprarrenal. Como os corticoides sintéticos têm uma meia-vida de algumas horas apenas, a suspensão abrupta faz com que após 2 ou 3 dias os níveis de cortisol fiquem próximo de zero. Quando a suprarrenal fica muito tempo inibida pela administração de corticoides exógenos, ela demora até voltar a produzir o cortisol naturalmente.
Em geral, tratamentos que duram menos de 3 semanas não costumam causar grandes efeitos colaterais nem causam inibição prolongada das supra renais.
Como o cortisol é um hormônio essencial para a vida, o paciente que suspende o corticoide sintético abruptamente entra em um estado chamado de insuficiência suprarrenal, podendo evoluir para choque circulatório, coma e óbito, se não for rapidamente atendido.
Por isso, a retirada dos corticoides após uso prolongado deve ser sempre feita de modo lento e gradual. Nunca se deve suspender o tratamento sem conhecimento médico.
Referências
- Systemic corticosteroid therapy – side effects and their management –
British Journal of Ophthalmology. - Review: Long-term side effects of glucocorticoids – Journal Expert Opinion on Drug Safety.
- Glucocorticoids – Huntington’s Outreach Project for Education, at Stanford.
- Prevention and treatment of systemic glucocorticoid side effects – International journal of dermatology.
- Pharmacologic use of glucocorticoids – UpToDate.
- Principais efeitos colaterais dos glicocorticóides sistêmicos – UpToDate.
- Efeitos adversos dos corticosteróides – StatPearls.
Deixe uma resposta