Combustão de hidrocarbonetos refere-se à reação química na qual um hidrocarboneto reage com oxigênio para criar dióxido de carbono, água e calor. Hidrocarbonetos são moléculas que consistem tanto de hidrogênio quanto de carbono. Eles são mais famosos por serem o constituinte primário dos combustíveis fósseis, nomeadamente gás natural, petróleo e carvão. Por esta razão, os recursos de combustíveis fósseis são frequentemente referidos como recursos de hidrocarbonetos. A energia é obtida dos combustíveis fósseis através da combustão (queima) do combustível. Embora existam impurezas nos combustíveis fósseis, a queima de hidrocarbonetos é o processo primário na queima do combustível fóssil. Um exemplo de combustão de hidrocarbonetos é ilustrado na Figura 1. Veja simulação no final da página para mais exemplos.
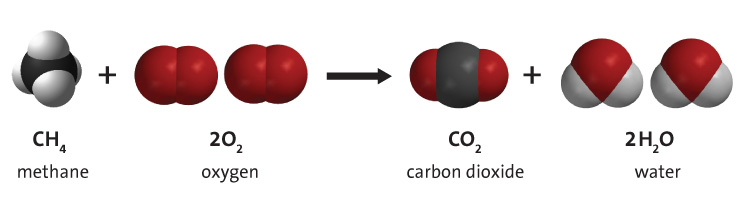
Descrição
Independentemente do tipo de hidrocarboneto, a combustão com oxigênio produz 3 produtos: dióxido de carbono, água e calor, como mostrado na reação geral abaixo. A energia necessária para quebrar as ligações nas moléculas de hidrocarbonetos é substancialmente menor que a energia liberada na formação das ligações nas moléculas de CO2 e H2O. Por esta razão, o processo libera quantidades significativas de energia térmica (calor). Esta energia térmica pode ser usada diretamente (talvez para aquecer uma casa) ou então pode ser convertida em energia mecânica, usando um motor térmico. No entanto, isto está sujeito a perdas de eficiência, resultando em perdas significativas de energia necessárias (como calor residual) regidas pela segunda lei da termodinâmica. A energia mecânica útil resultante será muito menor que a energia térmica inicial fornecida pela combustão de hidrocarbonetos.
Equação Geral de Reacção:
- refere-se ao número de átomos de carbono no hidrocarboneto
- refere-se ao número de átomos de hidrogênio no hidrocarboneto
- refere-se ao número de átomos de oxigênio necessários na reação de combustão do hidrocarboneto
Combustão de hidrocarbonetos e combustíveis fósseis
Nota que o CO2 é sempre produzido na combustão do hidrocarboneto; não importa que tipo de molécula de hidrocarboneto. A produção de CO2 e H2O é na verdade a forma como a energia útil é obtida dos combustíveis fósseis. Por esta razão, é importante distinguir entre o dióxido de carbono e outros produtos “residuais” que surgem de impurezas no combustível, como o enxofre e os compostos de nitrogênio. Os resíduos provenientes de impurezas podem ser eliminados com a tecnologia correta; o CO2 não pode ser eliminado a menos que os combustíveis fósseis não sejam queimados (usados) em primeiro lugar.
Não todos os combustíveis fósseis têm a mesma composição. O gás natural é composto por mais de 90% de metano (CH4), que é a menor molécula de hidrocarboneto. O petróleo tende a ser composto de moléculas de tamanho médio, embora a composição varie muito de um grau de petróleo bruto para o próximo. Em geral, quanto mais denso é o petróleo, mais longas são as cadeias de carbono nas moléculas. Finalmente, o carvão contém as maiores e mais complexas moléculas de hidrocarbonetos.
Os diferentes hidrocarbonetos têm diferentes proporções de hidrogênio para o carbono, eles produzem diferentes proporções de água para o dióxido de carbono. Em geral, quanto maior e mais complexa for a molécula, maior será a relação entre o carbono e o hidrogénio. Por este motivo, a combustão de quantidades iguais de diferentes hidrocarbonetos produzirá quantidades diferentes de dióxido de carbono, dependendo da razão entre o carbono e o hidrogénio nas moléculas de cada um. Como o carvão contém as moléculas de hidrocarbonetos mais longas e complexas, a queima do carvão liberta mais CO2 do que a queima da mesma massa de petróleo ou gás natural. Isto também altera a densidade energética de cada um destes combustíveis.
Emissão de dióxido de carbono
Below é um gráfico do CO2 emitido a partir da produção de 293,1 kWh (1.000.000 BTUs) de energia a partir de vários combustíveis hidrocarbonados.
| Combustível | kg de emissões de CO2 |
|---|---|
| Carvão antracite | 104 |
| Carvão betuminoso | 93.5 |
| Carvão Ligeiro | 97,9 |
| Carvão Subbituminoso | 97,4 |
| Diesel | 73.2 |
| Gasolina | 71,5 |
| Propano | 63,2 |
| Gás natural | 53.2 |
Animação de combustão
Selecione um combustível do menu suspenso para ver a reação líquida que ocorre durante a combustão.
Para Leitura Adicional
Para mais informações por favor veja as páginas relacionadas abaixo:
- Combustível fóssil
- Energia primária
- Recursos de hidrocarbonetos
- Carvão
- Óleo
- Gás natural
- Uma página aleatória
Deixe uma resposta