A REGIÃO BUCCAL – UMA VANTAGEM ADVANTE DE ENTREGA DE DROGAS
Inovações na administração de medicamentos contêm a promessa de minimizar os efeitos colaterais dose-dependentes e maximizar a atividade biológica enquanto melhora a aderência do paciente.
A administração peroral de fármacos, a via preferencial de administração de fármacos em termos de experiência do paciente, tem várias desvantagens, tais como metabolismo hepático de primeira passagem, maior início de ação e degradação enzimática de fármacos no trato gastrointestinal (GI). Quando o IG e a degradação hepática limitam a segurança ou eficácia de um fármaco, as injeções invasivas são freqüentemente o único modo viável de administração – com a conseqüência potencial de menor aderência do paciente.

A administração bucal pode alcançar efeitos locais e sistêmicos e é atrativa na medida em que supera as deficiências da administração peroral. Com efeito, as substâncias absorvidas através do bypass gastrointestinal da mucosa bucal degradam-se enzimática e o efeito hepático de primeira passagem. A administração bucal representa ainda uma melhor alternativa às injeções ou comprimidos para aqueles pacientes que têm dificuldade de deglutição.
Qual é o sítio bucal?
A área bucal é o revestimento interno da bochecha e do lábio, representando cerca de um terço da superfície da cavidade bucal (Figura 1).1 A mucosa bucal consiste de uma camada superficial de epitélio escamoso estratificado ligado ao tecido conjuntivo subjacente por uma lâmina basal. Uma rede de capilares sanguíneos está presente no tecido conjuntivo onde drogas que penetraram através do epitélio podem entrar na circulação sistêmica através da veia jugular interna.2
>9925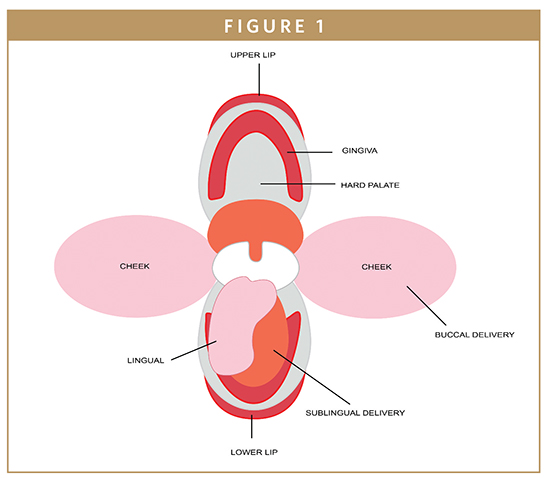
O epitélio vestibular atua como uma barreira à permeação de drogas hidrofílicas, enquanto o tecido conjuntivo, que é de natureza mais hidrofílica, parece afetar o tempo de defasagem difusa dos compostos lipofílicos.3 O transporte de drogas através da mucosa pode ser trans- ou paracelular (Figura 2), com a maioria das drogas hidrofílicas e macromoléculas permeando através da difusão paracelular passiva e compostos lipofílicos e pequenas moléculas hidrofóbicas predominantemente passando através do transporte paracelular.4 Como tal, a membrana celular atua como a maior barreira de transporte dos compostos hidrofílicos, e os espaços intercelulares se colocam como a maior barreira à permeação dos compostos lipofílicos.

A Importância da Mucoadhesion
Mucoadhesion é quando duas superfícies, uma das quais é uma membrana mucosa, aderem uma à outra. É um parâmetro crítico para a administração bucal e materiais de formulação com propriedades adesivas ideais a serem selecionados. A mucoadhesion acontece em dois estágios – o estágio de contato seguido pelo estágio de consolidação, quando as interações adesivas são estabelecidas. Provavelmente há múltiplos mecanismos em jogo que causam a aderência. É importante salientar que a falha do adesivo nas articulações ocorre como resultado da sobre-hidratação de uma forma de dosagem, ou como resultado de epitélio ou rotação de muco. O tempo de renovação do epitélio bucal foi estimado em 3 a 8 dias em comparação com cerca de 30 dias para a pele.4

Vantagens do local
Além do grande benefício do parto sistêmico que evita a degradação do fígado e intestino para maior biodisponibilidade e menores efeitos colaterais, a boca tem uma área relativamente grande para aplicação de drogas e boa acessibilidade em comparação ao nariz, reto e vagina.5 Além disso, a rápida rotatividade celular na mucosa bucal reduz o risco de danos ou irritação dos tecidos.6 Enquanto a mucosa sublingual é mais permeável, vascularizada e mais fina que a mucosa vestibular, a superfície desta mucosa é menor, constantemente lavada pela saliva, e o cisalhamento exercido pela língua dificulta a manutenção da forma de dosagem em contato com a mucosa sublingual.7 Por todas essas razões, a mucosa da bochecha é um local preferido dentro da cavidade bucal para a administração de sistemas de liberação controlada que precisam aderir por um longo período de tempo.8
Limitações do local
Aumentar a taxa de absorção (μg/mm2/s) ou permeabilidade do tecido vestibular é freqüentemente necessário para compensar a limitada área de superfície disponível. O uso de intensificadores de permeação (ou seja, substâncias que reorganizam a epiderme ou as estruturas epiteliais ou abrem as junções estreitas intercelulares) é muito importante nesta área. As macromoléculas são mais complexas de se administrar através da mucosa devido à degradação enzimática da saliva e à fraca permeação através do epitélio vestibular sem o aumento da permeação de base química e elétrica.9 O uso impróprio de intensificadores de permeação pode causar preocupações de segurança em relação à irritação local dos tecidos, mas também como resultado de um efeito indesejável do bolo que empurra a concentração da droga no sangue para níveis que não são seguros.
Uma estratégia alternativa para garantir uma maior absorção de drogas pouco solúveis ou permeáveis no tecido é aumentar o tempo de permanência na boca. Tal como acontece com os intensificadores de permeação, o aumento do tempo de permanência pode causar irritação nos tecidos, bem como desconforto ao paciente, e requer uma avaliação cuidadosa dos efeitos imediatos e a longo prazo na integridade e funcionalidade dos tecidos. Aumentar o tempo de permanência na cavidade oral pode ser ainda mais desafiador, uma vez que a droga pode ser rapidamente eliminada devido à acção de lavagem da saliva. Como resultado, doses repetidas e frequentes podem ser necessárias, a menos que a forma de dosagem crie uma forte ligação com a mucosa absorvente. Pesquisas são necessárias para quantificar a quantidade de rubor salivar que afeta a eficiência do parto transmucoso oral a partir de diferentes sistemas de administração de drogas.
Fatores humanos são importantes a serem levados em consideração ao desenvolver um produto bucal. Dado que a mucosa bucal se estende dos espaços superior e inferior entre as bochechas, lábios e gengivas, o local exato onde o paciente coloca a forma de dosagem pode afetar a aderência e absorção do medicamento, e essas implicações de fatores humanos podem afetar a variabilidade interpaciente. Como a forma de dosagem é colocada pode causar complicações adicionais quando a forma de dosagem é projetada para liberação unidirecional e tem um lado adesivo específico para ser colocado contra a bochecha interna. Finalmente, quando e o que o paciente come, bebe ou fuma pode afectar ainda mais a absorção do medicamento através da mucosa.
O risco de desalojamento e variabilidade do paciente devido à estimulação da saliva pode ser minimizado se o medicamento for administrado durante a noite, por exemplo, quando o paciente não está a comer ou a falar.
Formulários de dosagem búcica
Embora a mucosa bucal só agora esteja a ser amplamente estudada como uma nova via de administração de medicamentos, o seu potencial para a administração de medicamentos é conhecido pela humanidade há séculos. Os nativos americanos introduziram o tabaco de mascar aos colonos europeus nos anos 1500, e as folhas de coca foram mastigadas há 8.000 anos por forrageiros peruanos. A mucosa bucal tem sido alvo de atenção usando formas convencionais de dosagem, como comprimidos, troches e pastilhas, e lavagens e sprays bucais, com vários desses produtos atualmente no mercado. O desafio está em manter estas formas de dosagem no local de absorção, dosagem precisa (líquidos) e desconforto (comprimidos). Os comprimidos têm o potencial de se separarem da mucosa, serem engolidos e depois aderir à parede do esófago causando um risco de asfixia, especialmente para crianças e idosos.
Sistemas mais avançados de administração de medicamentos incluem filmes, adesivos, comprimidos de bilayer, hidrogel e fitas adesivas juntamente com o uso de micro e nanopartículas estão sendo desenvolvidos para superar as limitações das formas de dosagem convencionais.
FILMES PARA ENTREGA BUCCAL – CUREFILM
Mucoadhesivos são uma forma de dosagem preferida para administração de mucosa bucal, dada a sua flexibilidade, conforto, palatabilidade e tamanho ajustável. Eles demonstraram melhor adesão do paciente em comparação aos comprimidos adesivos.10,11 Em contraste com as formulações líquidas, gel e pomada, os filmes mucoadesivos permanecem em contato com a mucosa por mais tempo, cobrem uma maior área de superfície e, portanto, proporcionam uma dosagem mais precisa do medicamento.12 De fato, os filmes mucoadesivos podem ser projetados através de uma cuidadosa seleção de material para manter um amplo contato adesivo com a membrana da mucosa, prolongando o tempo de retenção do sistema de administração para aumentar a absorção total do medicamento. Além disso, os filmes mucoadesivos são bem adequados para terapia local, protegendo a superfície da ferida oral contra infecções, por exemplo.13
As composições do filme são projetadas para alcançar as seguintes propriedades físicas: resistência bioadhesiva, resistência à tração, maleabilidade, flexibilidade e desintegração prolongada. Estas propriedades são críticas para alcançar o perfil de liberação de drogas alvo, aceitação do paciente e compatibilidade com os processos de fabricação comercial. Atingir as especificações alvo dos filmes poliméricos bucais é altamente dependente do tipo e concentração dos polímeros selecionados e da dose de ingredientes ativos a serem entregues.
Como discutido aqui, mesmo com uma película fortemente adesiva, a descarga salivar fará com que parte da película se dissolva na cavidade oral e seja engolida. Filmes de dupla camada com uma camada de suporte oclusiva foram projetados para impulsionar a liberação e absorção unidirecional de drogas na mucosa bucal e podem fornecer altas doses de ingrediente ativo. Embora tais desenhos possam melhorar a absorção bucal, eles apresentam vários inconvenientes. Eles podem levar a erros do usuário em sua aplicação, a camada oclusiva pode se desalojar e se tornar um risco de asfixia e, por último, a complexidade da expansão de uma película de camada dupla aumenta os custos de fabricação.
Levando em consideração essas restrições, a abordagem da CURE Pharmaceutical ao desenvolvimento de película bucal com CUREfilm aproveita a inevitável descarga salivar de uma película de camada única para criar melhores perfis de liberação de fármacos. Nós projetamos nossos produtos para combinar o efeito bolus de início rápido do parto bucal com a liberação prolongada do parto GI para alcançar um perfil pulsátil geral ou de liberação sustentada. Na verdade, com o parto bucal, os níveis de sangue podem atingir o pico rapidamente, e uma meia-vida mais curta pode significar que o efeito se desgasta rapidamente. Além disso, se a administração de altas doses de um fármaco apenas por via bucal (por exemplo, mais de 100 mg), a concentração local do tecido pode ser demasiado elevada e danificar o tecido. Uma abordagem em uma única camada é preferível, pois minimiza os custos e erros do usuário.
Para criar um filme CURE bucal, uma mistura cuidadosamente selecionada de polímeros, intensificadores de permeação e lipídios são combinados para otimizar a aderência, difusão de drogas, e permeação através da mucosa. Os lipídios têm um papel crucial na solubilização e estabilidade dos ingredientes ativos. Eles ajudam a conduzir compostos hidrofílicos através do epitélio da mucosa e promovem o transporte trans-celular de compostos lipofílicos através do epitélio para alcançar os vasos sanguíneos. A nano-particulação do princípio ativo pode fornecer uma seta adicional na aljava do formulador para aumentar a taxa de absorção.
Para alcançar proteção gástrica suficiente e liberação intestinal eficiente da porção da droga que é ingerida, as partículas da droga podem ser total ou parcialmente encapsuladas, revestidas entéricas ou reticuladas a polímeros, como o quitosano, antes da sua incorporação na matriz do filme. Outras estratégias incluem a formação de lipossomal ou micelar, co-cristalização e o uso de polímeros gelificantes ou incháveis.
Esta estratégia dupla pode ser muito útil para drogas combinadas com diferentes perfis metabólicos em que uma droga é preparada para absorção bucal (ou seja, se tiver um alto efeito de primeira passagem), e a outra é preparada para liberação no GI.
SUMÁRIO
O desenho e a construção de um filme oral capaz de uma aplicação terapêutica eficaz pode ser um desafio e requer a criação de novas tecnologias. Como resultado dessas inovações, os filmes bucais são agora uma forma de dosagem comercialmente viável que pode resolver muitos problemas enfrentados pela indústria farmacêutica, pacientes e seus cuidadores. Eles serão capazes de substituir as injeções diárias, tais como as doses de apomorfina tomadas por pacientes que sofrem da doença de Parkinson. Eles podem melhorar a biodisponibilidade de medicamentos, tais como canabinóides, diminuindo potencialmente a sua dose e os efeitos secundários psicoactivos. Quando o alívio rápido dos sintomas é necessário, eles podem produzir um efeito bolus. Eles são uma alternativa conveniente aos líquidos intragáveis para crianças e pílulas difíceis de ingerir para idosos.
Dadas as importantes necessidades não atendidas pelo mercado, a taxa de adoção de filmes orais tem sido alta. De fato, o mercado global foi avaliado em 2,1 bilhões de dólares em 2017 e prevê-se que se expandirá a uma CAGR de 13% durante o período previsto de 2018 a 2026.14 Este crescimento comercial dos filmes orais, incluindo os filmes bucais, reflete o maior foco da indústria farmacêutica na inovação centrada no paciente no desenvolvimento de novos medicamentos e na melhoria de medicamentos antigos – onde a experiência do paciente impulsiona o design do fornecimento de medicamentos, o que, por sua vez, melhora os resultados do paciente.
- Curatolo W. As barreiras de permeabilidade lipoidal da pele e do trato alimentar. Pharm Res. 1987;4(4):271-277.
- Colombo P, Cagnani S, Buttini F, Santi P, et al. Biological In Vitro Models for Absorption by Non-Oral Routes, Reference Module in Chemistry, Molecular Sciences and Chemical Engineering, Elsevier. 2013.
- Kulkarni U, Mahalingam R, Pather SI, Li X, Jasti B. Mucosa bucal suína como modelo in vitro: contribuição relativa do epitélio e tecido conjuntivo como barreiras de permeabilidade. J Pharm Sci. 2009;98(2):471-483. doi: 10.1002/jps.21436.
- Gandhi RB, Robinson JR. Oral cavity as a site for bioadhesive drug delivery Adv. Drug Deliv Rev. 1994;13:43-74.
- Rathbone MJ, Drummond BK, Tucker IG. The oral cavity as a site for systemic drug delivery Adv Drug Deliv Rev. 1994;13:1-22.
- Squier CA, Wertz PW. Structure and Function of the Oral Mucosa and Implications for Drug Delivery M.J. Rathbone (Ed.), Oral Mucosal Drug Delivery, Marcel Dekker, New York. 1996:1-26.
- Madhav NVS, Shakya AK, Shakya P, Singh K. Orotransmucosal drug delivery systems: a review. J Control Release. 2009;140:2-11.
- Madhav NVS, Shakya AK, Shakya P, Singh K. Orotransmucosal drug delivery systems: a review J Control Release. 2009;140:2-11.
- Morales JO, Brayden DJ. Entrega bucal de pequenas moléculas e biologia: de polímeros mucoadhesivos, filmes e nanopartículas. Farmacologia de opinião atual. 2017;36:22-28.
- Kraisit P, Limmatvapirat S, Nunthanid J, et al. Preparação e caracterização de filmes de mistura hidroxipropilmetilcelulose/policarbofil mucoadhesivos usando uma abordagem de desenho de mistura Chem Pharm Bull. 2017;65(3):284-294.
- Giovino C, Ayensu I, Tetteh J, et al. Desenvolvimento e caracterização de filmes de quitosana impregnados com nanopartículas de PEGb-PLA carregadas com insulina (NPs): uma abordagem potencial para a administração bucal de macromoléculas. Int J Pharm. 2012;428(1-2):143-151.
- Abruzzo A, Bigucci F, Cerchiara T, et al. Mucoadhesive chitosan/gelatin films for buccal delivery of propranolol hydrochloride. Polímero de Carbohidrato. 2012;87(1):581-588.
- Tejada G, Lamas MC, Svetaz L, Salomón CJ, Alvarez VA, et al. Efeito da técnica de incorporação de drogas e combinação de polímeros no desempenho de filmes biopoliméricos antifúngicos bucais. Int J Pharmaceut. 2018;548(1):431-442.
- Transparency Market Research (TMR) report. Oral Thin Films Market – Global Industry Analysis, Size, Share, Growth, Trends, and Forecast, 2018-2026.

Robert Davidson é o CEO da CURE e Chariman do Conselho de Administração. Antes de sua função na CURE Pharmaceutical, ele atuou como Presidente e Diretor Executivo da InnoZen Inc., Diretor Executivo da Gel Tech LLC, Diretor Executivo da Bio Delivery Technologies Inc., e atuou em vários conselhos corporativos. O Sr. Davidson foi responsável pelo desenvolvimento de várias tecnologias de distribuição de medicamentos e extensões de marcas comerciais. Ele tem um Mestrado em Gestão Aplicada de Projetos pela Universidade Villanova, Mestrado em Saúde Pública pela Universidade Militar Americana, Virginia e um Mestrado em Saúde e Bem-estar pela Universidade Liberty, Virginia. Davidson também completou sua Pós-Graduação na Universidade de Cambridge com carta de recomendação.

Jessica Rousset é a Diretora Operacional da CURE. A Sra. Rousset supervisiona as operações e conduz a estratégia corporativa e o crescimento. A Sra. Rousset trabalhou anteriormente como Chefe de Inovação no Children’s Hospital Los Angeles, onde durante um período de dez anos, ela ajudou a lançar empresas de dispositivos médicos e terapêuticos e fundou e operou um acelerador de tecnologia pediátrica nacional. Antes disso, a Sra. Rousset ocupou cargos no The Scripps Research Institute e na GlaxoSmithkline Biologicals em funções de laboratório, pesquisa clínica e desenvolvimento de negócios. Ela formou-se como engenheira bioquímica no Institut National des Sciences Appliquées em Lyon, França.
Deixe uma resposta