Introduction
Les néoplasmes de la paroi thoracique sont soit primaires, soit métastatiques avec un taux de malignité d’environ 50% pour cent (1). Les atteintes de la paroi thoracique dues à des néoplasmes pulmonaires primaires sont rares, se produisant dans environ 5 % de toutes les tumeurs pulmonaires primaires (2). Les tumeurs primaires de la paroi thoracique proviennent des tissus mous, des os et des cartilages ; leur incidence est de 2 à 5 % dans la population générale (3). La survie globale à cinq ans après résection des néoplasmes primaires de la paroi thoracique est d’environ soixante pour cent ; une rechute survient chez jusqu’à 50 % des patients, avec une survie à cinq ans de 17 % (4).
Le diagnostic d’une tumeur de la paroi thoracique doit comporter une anamnèse et un examen attentifs du patient, une tomodensitométrie (TDM), une résonance magnétique nucléaire (RMN) et une tomographie par émission de positons (TEP). Un diagnostic histologique préopératoire doit être obtenu au moyen d’une aspiration à l’aiguille fine (FNAB) ou d’une biopsie excisionnelle.
Les complications péri- et postopératoires (principalement pulmonaires et infectieuses) après une résection de la paroi thoracique surviennent chez près de 25% des patients, raison pour laquelle une évaluation préopératoire approfondie du patient, comprenant des tests de fonction pulmonaire avec DLCo et une évaluation cardiaque, est fortement recommandée (5).
Dans ce contexte, nous rapportons par la présente notre technique de reconstruction chirurgicale après une résection de la paroi thoracique antérieure et un calage du corps sternal pour une tumeur primaire de la paroi thoracique (chondrosarcome).
Technique chirurgicale
Les reconstructions de la paroi thoracique peuvent être particulièrement difficiles en fonction de la taille de la résection, du site et de l’habitus du patient.
La stratégie chirurgicale doit être soigneusement analysée en préopératoire en gardant à l’esprit :
- La nécessité d’obtenir une résection radicale oncologique (R0);
- Une identification correcte de la ou des côtes et de l’implication sternale par la tumeur au moyen d’un scanner est la première étape (parfois la tumeur n’est pas palpable/visible) ;
- Une reconstruction adéquate avec des matériaux prothétiques adéquats, visant à éviter les hernies pulmonaires, à restaurer la stabilité physiologique, la rigidité et la synchronisation des mouvements de la paroi thoracique liés à la respiration et à protéger les organes internes.
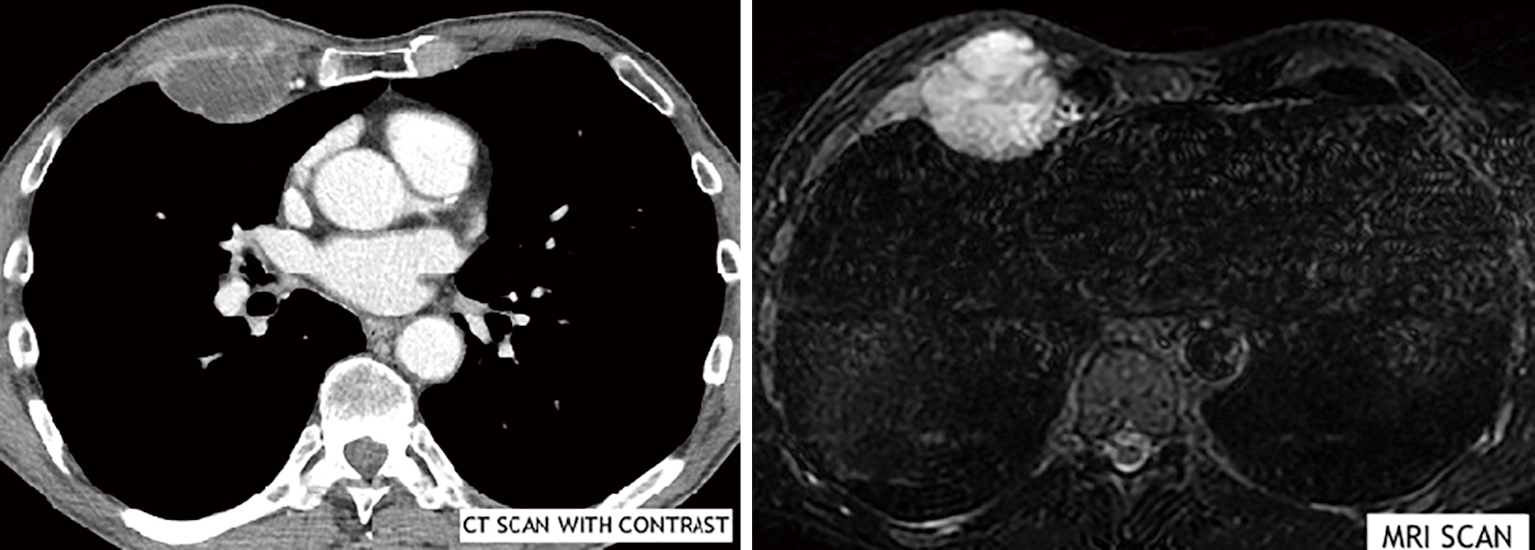
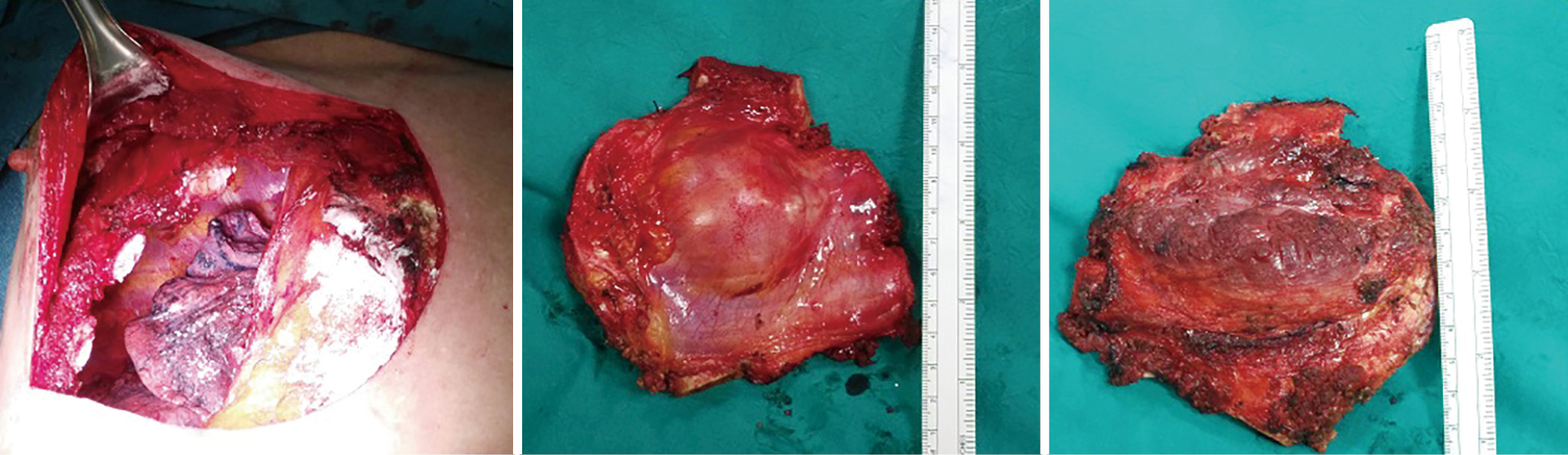
A titre d’exemple de cette technique chirurgicale, nous présentons le cas d’un monsieur de 74 ans qui s’est présenté à notre unité pour des douleurs thoraciques. A l’examen, une lésion saillante de la paroi thoracique antérieure droite a été vue et palpée. Le patient a décrit une augmentation de la douleur et de la taille de la lésion en quelques semaines. Le scanner a confirmé la présence d’une masse hétéroplastique (46×42×43 mm3) impliquant les 4ème et 5ème côtes de manière antérieure (Figure 1). Un FNAB échoguidé a été réalisé et un diagnostic final de chondrosarcome mixte a été obtenu. La masse était positive à la TEP avec un SUV max de 7. Le RMN a montré une augmentation dimensionnelle (54×51×53 mm3) de la tumeur, la masse étant très proche du corps sternal (Figure 1). Une indication chirurgicale a été posée. Habituellement, l’accès chirurgical privilégié pour ces lésions est une thoracotomie antérieure, l’incision cutanée se prolongeant cutanément sur la ligne midsternale (Figure 2). Une résection de la paroi thoracique (côtes III, IV et V) a été réalisée en bloc avec un coin de corps sternal, afin de garder des marges sûres par rapport à la lésion (Figure 3). La reconstruction a été réalisée avec une « technique en sandwich », en ancrant trois plaques de titane aux côtes réséquées et au corps sternal, entre deux couches de mailles biologiques, une en dessous des plaques – pour reconstruire la cavité endothoracique et empêcher la hernie du poumon et protéger les organes internes – et une au-dessus, pour reconstruire le plan musculaire (Figure 4). Une exérèse en forme de losange de la peau et des tissus sous-cutanés dans le site de la biopsie (FNAB) a été réalisée (positif pour une infiltration tumorale) (Figure 4). Le drain thoracique a été retiré au jour 2 postopératoire (Figure 5).



Discussion
Les caractéristiques d’une reconstruction réussie de la paroi thoracique doivent viser à restaurer la rigidité de la paroi thoracique, à préserver la mécanique pulmonaire et à protéger les organes intrathoraciques, à éviter les mouvements paradoxaux de la cavité thoracique et, éventuellement, à réduire la déformation thoracique (6).
Plusieurs techniques et matériaux de reconstruction ont été décrits dans la littérature au fil des années. Cependant, les lecteurs conviendront qu’il n’y a pas un seul matériau ou une seule technique qui fonctionne le mieux pour toutes les reconstructions, mais chaque reconstruction doit être abordée avec le matériau et la technique appropriés en fonction du besoin, en gardant à l’esprit les exigences suscitées par le Roux et Sherma depuis 1983 (6). Le choix des matériaux disponibles est copieux et comprend des mailles synthétiques et biologiques, du méthacrylate de méthyle, du PTFE (GORE-TEX), des plaques de titane, des allogreffes et des homogreffes (matériaux bioprothétiques humains et porcins), des lambeaux de muscle ou d’omentum et dernièrement des prothèses personnalisées imprimées en 3D (7,8).
Notre préférence pour la reconstruction des résections de la paroi thoracique antérieure avec atteinte sternale est basée sur l’utilisation de deux matériaux prothétiques différents, une maille biologique (XCM Biologic Tissue Matrix™) et des plaques de titane (MatrixRIB™). L’approche de la reconstruction avec deux matériaux prothétiques différents doit être bien réfléchie car, en cas d’infection, la nécessité de retirer les deux matériaux prothétiques est très élevée. En fait, certains auteurs rapportent un taux d’infection des mailles synthétiques compris entre 10% et 25% avec la nécessité de les retirer pour résoudre l’infection (9). Le XCM Biologic Tissue Matrix™ est une matrice tridimensionnelle biologique stérile non réticulée, dérivée du derme porcin. Cette maille est traitée par un processus qui désinfecte le tissu, inactive les virus tout en garantissant une réépithélialisation cellulaire, en maintenant l’essentiel des composants de la matrice extracellulaire naturelle et en minimisant les dommages à l’architecture tissulaire. Les caractéristiques de ce filet permettent une utilisation sûre avec un second matériau prothétique (plaques de titane), il peut être facilement façonné avec précision et garantit un bon renforcement sur le défaut grâce à sa résistance à la tension uniforme ; il crée également un substrat idéal qui évite l’hernie pulmonaire et les dommages, et protège les autres organes internes.
La mécanique respiratoire physiologique qui est établie par le système poumon-poitrine (compliance/élastance), est garantie si le poumon et la paroi thoracique sont intacts. La cage thoracique, constituée par les côtes qui sont ancrées antérieurement par leurs cartilages costaux au sternum et postérieurement aux vertèbres thoraciques, est un système rigide mais plastique, fondamental pour contribuer à la stabilité et au synchronisme respiratoire.
Les grands défauts altérant l’intégrité de la cage thoracique, modifient gravement la mécanique respiratoire (respiration paradoxale), provoquant une détresse respiratoire et une instabilité du patient.
Pour cette raison, il est important de restaurer son intégrité, en recréant la rigidité et la stabilité originelles au moyen de plaques fixées sur les marges des côtes réséquées et du corps sternal lui-même.
Nous privilégions le système de fixation MatrixRIB™ pour nos reconstructions ; il s’agit de plaques en titane précontraintes qui, après un remodelage minimal suivant le profil des côtes, sont fixées sur les marges des côtes réséquées à l’aide de vis, recréant ainsi l’aspect anatomique et physiologique de la cage thoracique.
Les vis de verrouillage au lieu de la barre de fixation des clips de côtes sont, à notre avis, plus recommandables, car : (I) sont susceptibles d’être mieux tolérées en postopératoire en raison d’une moindre douleur due à une contrainte mineure du faisceau costal et (II) sont plus sujettes à un moindre taux de dislocation/rupture postopératoire (7,10).
Comme on peut le voir dans les vidéos de notre cas (figures 6,7), en raison du mauvais habitus tissulaire du patient, nous avons implanté et fixé aux tissus mous extrathoraciques et au muscle grand pectoral (précédemment déconnecté de la cage thoracique), par-dessus les barres de titane, une seconde maille XCM Biologic Tissue Matrix™ façonnée ( » technique du sandwich « ).


Quelle que soit la technique utilisée pour établir la stabilité du squelette, une couverture tissulaire complète de la prothèse est obligatoire, en utilisant une suture directe, des greffes de peau, des lambeaux d’avancement locaux, des lambeaux myocutanés pédiculés ou des lambeaux libres (13).
Remerciements
Aucun.
Note de bas de page
Conflits d’intérêts : Les auteurs n’ont aucun conflit d’intérêt à déclarer.
Déclaration éthique : Les auteurs sont responsables de tous les aspects du travail en veillant à ce que les questions liées à l’exactitude ou à l’intégrité de toute partie du travail soient examinées et résolues de manière appropriée. Un consentement éclairé écrit a été obtenu du patient pour la publication de ce manuscrit et de toute image qui l’accompagne.
- D’Addario G, Früh M, Reck M, et al. Cancer du poumon non à petites cellules métastatique : Lignes directrices de pratique clinique de l’ESMO pour le diagnostic, le traitement et le suivi. Ann Oncol 2010;21 Suppl 5:v116-9.
- Filosso PL, Sandri A, Guerrera F, et al. Tumeurs pulmonaires primaires envahissant la paroi thoracique. J Thorac Dis 2016;8:S855-62.
- Shah AA, D’Amico TA. Tumeurs primaires de la paroi thoracique. J Am Coll Surg 2010;210:360-6.
- King RM, Pairolero PC, Trastek VF, et al. Tumeurs primaires de la paroi thoracique : facteurs affectant la survie. Ann Thorac Surg 1986;41:597-601.
- Spicer JD, Shewale JB, Antonoff MB, et al. L’influence de la technique de reconstruction sur les résultats pulmonaires et infectieux périopératoires après résection de la paroi thoracique. Ann Thorac Surg 2016;102:1653-9.
- le Roux BT, Shama DM. La résection des tumeurs de la paroi thoracique. Curr Probl Surg 1983;20:345-86.
- Sanna S, Brandolini J, Pardolesi A, et al. Matériaux et techniques dans la reconstruction de la paroi thoracique : une revue. J Vis Surg 2017;3:95.
- Wu Y, Chen N, Xu Z, et al. Application de la technologie d’impression 3D à la résection des tumeurs de la paroi thoracique et à la reconstruction de la paroi thoracique. J Thorac Dis 2018;10:6880-90.
- Daigeler A, Druecke D, Hakimi M, et al. Reconstruction de la paroi thoracique- suivi à long terme incluant des tests de fonction pulmonaire. Langenbecks Arch Surg 2009;394:705-15.
- Muthialu N, McIntyre D, McIntosh N, et al. Taux de fracture inquiétant des barres STRATOS dans les corrections de pectus. Eur J Cardiothorac Surg 2019;55:300-3.
- Sandri A, Donati G, Blanc CD, et al. Résection et coin sternal – partie I de la résection. Asvide 2020;7:003. Disponible en ligne : http://www.asvide.com/watch/33047
- Sandri A, Donati G, Blanc CD, et al. Résection et cale sternale – partie II. Asvide 2020;7:004. Disponible en ligne : http://www.asvide.com/watch/33048
- Seder CW, Rocco G. Reconstruction de la paroi thoracique après résection étendue. J Thorac Dis 2016;8:S863-71.
Laisser un commentaire