La région buccale – UNE VOIE AVANTAGEUSE POUR L’ADMINISTRATION DES MÉDICAMENTS
Les innovations en matière d’administration des médicaments sont prometteuses pour minimiser les effets secondaires dépendants de la dose et maximiser l’activité biologique tout en améliorant l’adhésion des patients.
L’administration perorale des médicaments, la voie d’administration privilégiée en termes d’expérience des patients, présente plusieurs inconvénients, tels que le métabolisme de premier passage hépatique, un délai d’action plus long et la dégradation enzymatique des médicaments dans le tractus gastro-intestinal (GI). Lorsque la dégradation GI et hépatique limite la sécurité ou l’efficacité d’un médicament, les injections invasives sont souvent le seul mode d’administration viable – avec pour conséquence potentielle une moindre adhésion du patient.

L’administration buccale permet d’obtenir des effets locaux et systémiques et présente l’intérêt de pallier les déficiences de l’administration perorale. En effet, les substances absorbées par la muqueuse buccale contournent la dégradation enzymatique gastro-intestinale et l’effet de premier passage hépatique. L’administration buccale représente en outre une meilleure alternative aux injections ou aux comprimés pour les patients qui ont des difficultés à avaler.
Qu’est-ce que le site buccal ?
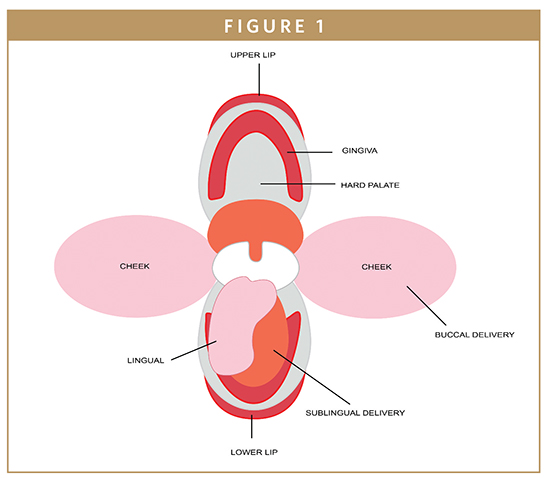
La zone buccale est le revêtement interne de la joue et de la lèvre, représentant environ un tiers de la surface de la cavité buccale (figure 1).1 La muqueuse buccale est constituée d’une couche superficielle d’épithélium pavimenteux stratifié liée au tissu conjonctif sous-jacent par une lame basale. Un réseau de capillaires sanguins est présent dans le tissu conjonctif où les médicaments qui ont traversé l’épithélium peuvent entrer dans la circulation systémique via la veine jugulaire interne.2
L’épithélium buccal agit comme une barrière à la perméation des médicaments hydrophiles, tandis que le tissu conjonctif, qui est de nature plus hydrophile, semble affecter le temps de retard de diffusion des composés lipophiles.3 Le transport des médicaments à travers la muqueuse peut être trans- ou paracellulaire (Figure 2), la plupart des médicaments hydrophiles et des macromolécules traversant par diffusion paracellulaire passive et les composés lipophiles et les petites molécules hydrophobes passant principalement par transport paracellulaire4. Ainsi, la membrane cellulaire agit comme la principale barrière de transport pour les composés hydrophiles, et les espaces intercellulaires se posent comme la principale barrière à la perméation des composés lipophiles.

L’importance de la mucoadhésion
On parle de mucoadhésion lorsque deux surfaces, dont l’une est une muqueuse, adhèrent l’une à l’autre. C’est un paramètre critique pour l’administration buccale et les matériaux de formulation ayant des propriétés adhésives optimales doivent être sélectionnés. La mucoadhésion se produit en deux étapes – l’étape de contact suivie de l’étape de consolidation lorsque les interactions adhésives sont établies. De multiples mécanismes sont probablement à l’origine de l’adhésion. Il est important de noter que l’échec de l’articulation adhésive se produira à la suite d’une surhydratation de la forme posologique ou à la suite du renouvellement de l’épithélium ou du mucus. Le temps de renouvellement de l’épithélium buccal a été estimé à 3 à 8 jours, contre environ 30 jours pour la peau4.

Avantages du site
En plus de l’avantage majeur de l’administration systémique qui contourne la dégradation hépatique et intestinale pour une plus grande biodisponibilité et des effets secondaires moindres, la bouche présente une surface relativement importante pour l’application du médicament et une bonne accessibilité par rapport au nez, au rectum et au vagin.5 De plus, le renouvellement rapide des cellules de la muqueuse buccale réduit le risque de dommages ou d’irritation des tissus.6 Bien que la muqueuse sublinguale soit plus perméable, plus vascularisée et plus mince que la muqueuse buccale, la surface de cette muqueuse est plus petite, constamment lavée par la salive, et le cisaillement exercé par la langue rend difficile le maintien de la forme posologique en contact avec la muqueuse sublinguale.7 Pour toutes ces raisons, la muqueuse de la joue est un site privilégié dans la cavité buccale pour l’administration de systèmes à libération contrôlée qui doivent adhérer pendant une période prolongée.8
Limitations du site
L’amélioration du taux d’absorption (μg/mm2/s) ou de la perméabilité du tissu buccal est souvent nécessaire pour compenser la surface limitée disponible. L’utilisation d’amplificateurs de perméation (c’est-à-dire des substances qui réorganisent l’épiderme ou les structures épithéliales ou ouvrent les jonctions serrées intercellulaires) est très importante dans ce domaine. Les macromolécules sont plus difficiles à administrer à travers la muqueuse en raison de leur dégradation enzymatique dans la salive et de leur faible perméabilité à travers l’épithélium buccal sans amélioration de la perméation par voie chimique ou électrique9. L’utilisation inappropriée d’amplificateurs de perméation peut poser des problèmes de sécurité en ce qui concerne l’irritation locale des tissus, mais aussi en raison d’un effet bolus indésirable qui augmente la concentration de médicament dans le sang à des niveaux qui ne sont pas sûrs.
Une stratégie alternative pour assurer une absorption plus élevée des médicaments peu solubles ou perméables dans les tissus est d’augmenter le temps de séjour dans la bouche. Comme pour les amplificateurs de perméation, l’augmentation du temps de séjour peut provoquer une irritation des tissus ainsi qu’un inconfort pour le patient et nécessite une évaluation minutieuse des effets immédiats et à long terme sur l’intégrité et la fonctionnalité des tissus. Augmenter le temps de séjour dans la cavité buccale peut être un défi supplémentaire car le médicament peut être rapidement éliminé en raison de l’action de rinçage de la salive. Par conséquent, des doses répétées et fréquentes peuvent être nécessaires, à moins que la forme galénique ne crée une liaison forte avec la muqueuse absorbante. Des recherches sont nécessaires pour quantifier dans quelle mesure le rinçage salivaire affecte l’efficacité de l’administration transmuqueuse orale de différents systèmes d’administration de médicaments.
Les facteurs humains sont importants à prendre en compte lors du développement d’un produit buccal. Étant donné que la muqueuse buccale s’étend des espaces supérieurs et inférieurs entre les joues, les lèvres et les gencives, l’endroit précis où le patient place la forme posologique peut affecter l’adhérence et l’absorption du médicament, et ces implications des facteurs humains peuvent affecter la variabilité interpatient. La façon dont la forme posologique est placée peut entraîner des complications supplémentaires lorsque la forme posologique est conçue pour une libération unidirectionnelle et possède une face adhésive spécifique à placer contre la face interne de la joue. Enfin, quand et ce que le patient mange, boit ou fume peut encore affecter l’absorption du médicament à travers la muqueuse.
Le risque de délogement et la variabilité du patient due à la stimulation salivaire peuvent être minimisés si le médicament est administré la nuit par exemple, lorsque le patient ne mange pas ou ne parle pas.
Formes posologiques buccales
Bien que la muqueuse buccale ne fasse l’objet que maintenant d’études approfondies en tant que nouvelle voie d’administration de médicaments, son potentiel pour l’administration de médicaments est connu de l’humanité depuis des siècles. Les Amérindiens ont introduit le tabac à mâcher auprès des colons européens dans les années 1500, et les feuilles de coca ont été mâchées il y a 8 000 ans par les bergers péruviens. La muqueuse buccale a été ciblée par des formes de dosage conventionnelles, telles que des comprimés, des troches et des pastilles, ainsi que des bains de bouche et des sprays, plusieurs produits de ce type étant actuellement sur le marché. Le défi réside dans la tenue de ces formes posologiques au site d’absorption, la précision du dosage (liquides) et l’inconfort (comprimés). Les comprimés ont le potentiel de se séparer de la muqueuse, d’être avalés, puis d’adhérer à la paroi de l’œsophage causant un risque d’étouffement, en particulier pour les enfants et les personnes âgées.
Des systèmes plus avancés d’administration de médicaments comprennent des films, des patchs, des comprimés bicouches, des hydrogels et des bandes ainsi que l’utilisation de micro- et nanoparticules sont en cours de développement pour surmonter les limites des formes de dosage conventionnelles.
FILMS POUR L’ADMINISTRATION BUCCALE – CUREFILM
Les films mucoadhésifs sont une forme posologique privilégiée pour l’administration par la muqueuse buccale compte tenu de leur flexibilité, de leur confort, de leur palatabilité et de leur taille ajustable. Ils ont démontré une meilleure observance des patients par rapport aux comprimés adhésifs.10,11 Contrairement aux formulations liquides, gels et pommades, les films mucoadhésifs restent en contact avec la muqueuse plus longtemps, couvrent une plus grande surface et permettent donc un dosage plus précis du médicament.12 En effet, les films mucoadhésifs peuvent être conçus grâce à une sélection minutieuse des matériaux pour maintenir un contact adhésif étendu avec la membrane muqueuse, prolongeant le temps de rétention du système d’administration pour une absorption totale accrue du médicament. En outre, les films mucoadhésifs sont bien adaptés à la thérapie locale, protégeant les surfaces des plaies orales contre l’infection par exemple.13
Les compositions des films sont conçues pour obtenir les propriétés physiques suivantes : force bioadhésive, résistance à la traction, pliabilité, flexibilité et désintégration prolongée. Ces propriétés sont essentielles pour obtenir le profil cible de libération du médicament, l’acceptabilité par le patient et la compatibilité avec les procédés de fabrication commerciaux. L’obtention des spécifications cibles des films polymères buccaux dépend fortement du type et de la concentration des polymères sélectionnés et de la dose de principes actifs délivrés.
Comme discuté ici, même avec un film fortement adhésif, la chasse salivaire fera qu’une partie du film se dissoudra dans la cavité buccale et sera avalée. Les films à double couche avec une couche dorsale occlusive ont été conçus pour entraîner une libération et une absorption unidirectionnelles du médicament dans la muqueuse buccale et peuvent délivrer des doses élevées de principe actif. Si ces conceptions peuvent améliorer l’absorption buccale, elles présentent plusieurs inconvénients. Ils peuvent entraîner une erreur de l’utilisateur dans leur application, la couche occlusive peut se déloger et devenir un risque d’étouffement, et enfin, la complexité de la mise à l’échelle d’un film à double couche fait augmenter les coûts de fabrication.
Tenant compte de ces contraintes, l’approche de CURE Pharmaceutical pour le développement de films buccaux avec CUREfilm tire parti de l’inévitable chasse salivaire d’un film à couche unique pour créer de meilleurs profils de libération de médicaments. Nous concevons nos produits de manière à combiner l’effet bolus à action rapide de l’administration buccale avec la libération prolongée de l’administration gastro-intestinale pour obtenir un profil global de libération pulsatile ou prolongée. En effet, avec l’administration buccale, les taux sanguins peuvent atteindre un pic rapidement, et une demi-vie plus courte peut signifier que l’effet s’estompe rapidement. De plus, si l’on administre de fortes doses d’un médicament uniquement par voie buccale (par exemple, plus de 100 mg), la concentration locale dans les tissus pourrait être trop élevée et endommager les tissus. Une approche à couche unique est préférable car elle minimise les coûts et les erreurs d’utilisation.
Pour créer un CUREfilm buccal, un mélange soigneusement sélectionné de polymères, d’amplificateurs de perméation et de lipides est combiné pour optimiser l’adhérence, la diffusion du médicament et la perméation à travers la muqueuse. Les lipides jouent un rôle crucial dans la solubilisation et la stabilité des ingrédients actifs. Ils aident à faire passer les composés hydrophiles à travers l’épithélium de la muqueuse et favorisent le transport transcellulaire des composés lipophiles à travers l’épithélium pour atteindre les vaisseaux sanguins. La nano-particulation de l’ingrédient actif peut fournir une flèche supplémentaire dans le carquois du formulateur pour augmenter le taux d’absorption.
Pour obtenir une protection gastrique suffisante et une libération intestinale efficace de la partie du médicament qui est avalée, les particules de médicament peuvent être entièrement ou partiellement encapsulées, enrobées par voie entérique ou réticulées à des polymères, tels que le chitosan, avant leur incorporation dans la matrice du film. D’autres stratégies comprennent la formation de liposomes ou de micelles, la cocristallisation, et l’utilisation de polymères gélifiants ou gonflables.
Cette double stratégie peut être très utile pour les médicaments combinés avec différents profils métaboliques dans lesquels un médicament est préparé pour l’absorption buccale (c’est-à-dire, s’il a un effet de premier passage élevé), et l’autre est préparé pour la libération dans le GI.
SUMMAIRE
La conception et la construction proprement dites d’un film oral capable d’assurer une délivrance thérapeutique efficace peuvent être difficiles et nécessitent la création de nouvelles technologies. Grâce à ces innovations, les films buccaux sont désormais une forme galénique commercialement viable qui peut résoudre de nombreux problèmes auxquels sont confrontés l’industrie pharmaceutique, les patients et leurs soignants. Ils pourront remplacer les injections quotidiennes, comme les piqûres d’apomorphine prises par les patients souffrant de la maladie de Parkinson. Ils peuvent améliorer la biodisponibilité des médicaments, tels que les cannabinoïdes, ce qui pourrait réduire leur dose et leurs effets secondaires psychoactifs. Lorsqu’un soulagement rapide des symptômes est nécessaire, ils peuvent produire un effet de bolus. Ils constituent une alternative pratique aux liquides peu appétissants pour les enfants et aux pilules difficiles à avaler pour les personnes âgées.
Compte tenu des importants besoins non satisfaits du marché auxquels ils répondent, le taux d’adoption des films oraux a été élevé. En effet, le marché mondial était évalué à 2,1 milliards de dollars en 2017 et devrait se développer à un TCAC de 13% au cours de la période de prévision de 2018 à 2026.14 Cette croissance commerciale des films oraux, y compris les films buccaux, reflète l’intérêt accru de l’industrie pharmaceutique pour l’innovation centrée sur le patient dans le développement de nouveaux médicaments et l’amélioration des anciens médicaments – où l’expérience du patient oriente la conception de l’administration des médicaments, ce qui améliore les résultats pour le patient.
- Curatolo W. Les barrières de perméabilité lipoïdales de la peau et du tube alimentaire. Pharm Res. 1987;4(4):271-277.
- Colombo P, Cagnani S, Buttini F, Santi P, et al. Biological In Vitro Models for Absorption by Non-Oral Routes, Reference Module in Chemistry, Molecular Sciences and Chemical Engineering, Elsevier. 2013.
- Kulkarni U, Mahalingam R, Pather SI, Li X, Jasti B. La muqueuse buccale porcine comme modèle in vitro : contribution relative de l’épithélium et du tissu conjonctif comme barrières de perméabilité. J Pharm Sci. 2009;98(2):471-483. doi : 10.1002/jps.21436.
- Gandhi RB, Robinson JR. La cavité buccale comme site d’administration de médicaments bioadhésifs Adv Drug Deliv Rev. 1994;13:43-74.
- Rathbone MJ, Drummond BK, Tucker IG. The oral cavity as a site for systemic drug delivery Adv Drug Deliv Rev. 1994;13:1-22.
- Squier CA, Wertz PW. Structure et fonction de la muqueuse orale et implications pour l’administration de médicaments M.J. Rathbone (Ed.), Oral Mucosal Drug Delivery, Marcel Dekker, New York. 1996:1-26.
- Madhav NVS, Shakya AK, Shakya P, Singh K. Orotransmucosal drug delivery systems : a review. J Control Release. 2009;140:2-11.
- Madhav NVS, Shakya AK, Shakya P, Singh K. Orotransmucosal drug delivery systems : a review J Control Release. 2009;140:2-11.
- Morales JO, Brayden DJ. Administration buccale de petites molécules et de produits biologiques : de polymères mucoadhésifs, de films et de nanoparticules. Current Opinion Pharmacol. 2017;36:22-28.
- Kraisit P, Limmatvapirat S, Nunthanid J, et al. Préparation et caractérisation de films de mélange mucoadhésif hydroxypropyl méthylcellulose/polycarbophile en utilisant une approche de conception de mélange Chem Pharm Bull. 2017;65(3):284-294.
- Giovino C, Ayensu I, Tetteh J, et al. Développement et caractérisation de films de chitosan imprégnés de nanoparticules (NPs) PEGb-PLA chargées en insuline : une approche potentielle pour la délivrance buccale de macromolécules. Int J Pharm. 2012;428(1-2):143-151.
- Abruzzo A, Bigucci F, Cerchiara T, et al. Films mucoadhésifs de chitosan/gélatine pour la délivrance buccale de chlorhydrate de propranolol. Carbohydr Polym. 2012;87(1):581-588.
- Tejada G, Lamas MC, Svetaz L, Salomón CJ, Alvarez VA, et al. Effet de la technique d’incorporation du médicament et de la combinaison de polymères sur la performance des films buccaux antifongiques biopolymériques. Int J Pharmaceut. 2018;548(1):431-442.
- Rapport de Transparency Market Research (TMR). Oral Thin Films Market – Global Industry Analysis, Size, Share, Growth, Trends, and Forecast, 2018-2026.

Robert Davidson est le PDG et le chariman du conseil d’administration de CURE. Avant son rôle chez CURE Pharmaceutical, il a été président et chef de la direction d’InnoZen Inc, chef de la direction de Gel Tech LLC, chef de la direction de Bio Delivery Technologies Inc, et a siégé à plusieurs conseils d’administration d’entreprises. M. Davidson a été responsable du développement de plusieurs technologies d’administration de médicaments et d’extensions de marques commerciales. Il est titulaire d’un certificat de maîtrise en gestion de projet appliquée de l’université Villanova, d’une maîtrise en santé publique de l’université militaire américaine, en Virginie, et d’une maîtrise en santé et bien-être de l’université Liberty, en Virginie. Davidson a également terminé ses études supérieures à l’Université de Cambridge avec une lettre de recommandation.

Jessica Rousset est la directrice de l’exploitation de CURE. Mme Rousset supervise les opérations et dirige la stratégie et la croissance de l’entreprise. Mme Rousset a précédemment occupé le poste de responsable de l’innovation à l’hôpital pour enfants de Los Angeles, où, sur une période de dix ans, elle a contribué au lancement d’entreprises de produits thérapeutiques et de dispositifs médicaux et a fondé et géré un accélérateur national de technologie pédiatrique. Avant cela, Mme Rousset a occupé des postes au Scripps Research Institute et chez GlaxoSmithkline Biologicals dans des fonctions de laboratoire, de recherche clinique et de développement commercial. Elle a suivi une formation d’ingénieur en biochimie à l’Institut national des sciences appliquées de Lyon, en France.
.
Laisser un commentaire