- Qu’est-ce qu’un corticoïde ?
- Corticoïdes et cortisol
- Types
- Maladies pouvant être traitées par les corticostéroïdes
- Absorption systémique
- Effets secondaires
- Effets secondaires cutanés
- Effets secondaires oculaires
- Effets métaboliques
- Effets cardiovasculaires
- Effets musculo-squelettiques
- Effets secondaires sur le système nerveux central
- Effets immunologiques
- Autres effets
- Soins et dangers de l’utilisation des corticostéroïdes
- Références
Qu’est-ce qu’un corticoïde ?
Les glucocorticoïdes, également appelés corticoïdes ou corticostéroïdes, sont des médicaments puissants dérivés de l’hormone cortisol, produite par la glande surrénale.
Les corticoïdes sont souvent utilisés dans le cadre du traitement des maladies d’origine inflammatoire, allergique, immunitaire et même contre certains types de cancer.
Bien qu’étant un médicament très efficace contre plusieurs maladies graves, les corticoïdes ont un défaut majeur : un profil très étendu d’effets secondaires, certains graves, d’autres esthétiquement indésirables.
Lorsqu’ils sont utilisés de manière prolongée, les corticoïdes entraînent une prise de poids, peuvent provoquer des vergetures, provoquer de l’acné, fragiliser les os, augmenter le risque d’infections, etc.
Dans cet article, nous traiterons des indications et des effets secondaires des corticoïdes, en mettant l’accent sur la prednisone et la prednisolone, les médicaments les plus utilisés de cette classe.
Si vous recherchez une notice simplifiée pour la prednisone, accédez à l’article suivant : PREDNISONE – A quoi ça sert, doses et soins
Pour des informations sur l’utilisation des corticostéroïdes dans le COVID-19, accédez aux articles suivants :
- DEXAMETHASONE – BULA POUR LES PATIENTS.
- INFORMATIONS SUR LE COVID-19.
Corticoïdes et cortisol
Les glucocorticoïdes sont des hormones stéroïdes, non anabolisantes et non sexuelles, produites par le cortex de la glande surrénale. L’hormone produite naturellement par notre corps est le cortisol.
Un taux normal de cortisol est essentiel pour notre santé, car cette hormone a une action sur le métabolisme du glucose, les fonctions métaboliques de l’organisme, la cicatrisation, le système immunitaire, la fonction cardiaque, le contrôle de la croissance et bien d’autres actions fondamentales de notre corps.
Le cortisol est une hormone du stress, car sa production augmente chaque fois que notre corps est soumis à un stress physique, comme en cas de traumatisme, d’infection ou de chirurgie. Le cortisol augmente la disponibilité du glucose et de l’énergie, élève la pression artérielle, augmente le tonus cardiaque et prépare le corps à subir et à combattre les insultes.
Types
Les glucocorticoïdes utilisés dans la pratique médicale sont des versions synthétiques, produites en laboratoire, de l’hormone naturelle cortisol.
Il existe plusieurs formulations synthétiques de corticoïdes, les plus utilisées sont la prednisone, la prednisolone, l’hydrocortisone, la dexaméthasone, la méthylprednisolone et la béclométhasone (voie inhalée).
Tous les corticoïdes synthétiques sont plus puissants que le cortisol naturel, à l’exception de l’hydrocortisone qui a une puissance similaire.
Puissance de chaque type de corticoïde par rapport au cortisol :
- Hydrocortisone → puissance similaire au cortisol.
- Déflazacort → 3 fois plus puissant que le cortisol.
- Prédnisolone → 4 à 5 fois plus puissant que le cortisol.
- Prednisone → 4-5 fois plus puissant que le cortisol.
- Triamcinolone → 5 fois plus puissant que le cortisol.
- Méthylprednisolone → 5-7,5 fois plus puissant que le cortisol.
- Bétaméthasone → 25-30 fois plus puissant que le cortisol.
- La dexaméthasone est → 25 à 30 fois plus puissante que le cortisol.
- La béclométhasone (inhalée) → 8 pufs 4 fois par jour est équivalente à 14 mg de prednisone orale quotidienne.
60 mg de prednisone ont le même effet que 2 mg de dexaméthasone ou 300 mg de cortisol naturel. En raison de cette plus grande puissance des corticostéroïdes synthétiques, nous sommes en mesure d’administrer aux patients des doses bien supérieures aux niveaux physiologiques de cortisol, ce qui est essentiel pour le traitement de certaines maladies.
Maladies pouvant être traitées par les corticostéroïdes
La prednisone et les corticostéroïdes en général sont des médicaments capables de moduler les processus inflammatoires et immunologiques de notre organisme, ce qui les rend extrêmement utiles dans une multitude de maladies. Toute maladie d’origine allergique, inflammatoire ou auto-immune peut être traitée par l’un de ces corticoïdes (lire aussi : QU’EST-CE QU’UNE MALADIE AUTOIMUNE ?).
Pour avoir une idée de l’importance des corticoïdes dans la pratique médicale, on peut citer les maladies suivantes comme indications de leur administration :
- Asthme.
- Sclérose en plaques.
- BPCO.
- Allergies, notamment anaphylaxie.
- Hépatite auto-immune.
- Herpès Zoster.
- Lupus.
- Polyarthrite rhumatoïde.
- Leucémie.
- Lymphome.
- Purpura thrombocytopénique idiopathique (PTI).
- Myélome multiple.
- Oedème cérébral.
- Paralysie faciale de Bell.
- Goutte.
- Sarcoïdose.
- Rhinite allergique.
- Vitiligo.
- Psoriasis.
- Granulomatose de Wegener.
- Maladie inflammatoire de l’intestin.
- Myasthénie grave.
- Vascularites.
- Maladie d’Addison (insuffisance surrénale).
- Glomérulonéphrite.
- Maladies cutanées d’origine inflammatoire ou auto-immune.
- Syndrome de Sjögren.
- Greffe d’organe.
- Urticaire.
Les doses quotidiennes équivalentes à 5-10 mg de prednisone sont appelées doses physiologiques car elles sont compatibles avec la production quotidienne naturelle de cortisol. A ces doses, les corticoïdes de synthèse ne présentent qu’un effet anti-inflammatoire.
En situation normale, la sécrétion de cortisol par la surrénale présente un cycle circadien, c’est-à-dire qu’elle subit des modifications en fonction de la période de la journée. Pendant les premières heures de la matinée, sa sécrétion est très élevée, pour se réduire à un maximum vers 23 heures. C’est pourquoi nous choisissons d’administrer les corticoïdes le matin pour essayer de simuler la sécrétion physiologique à laquelle l’organisme est habitué, ce qui réduit l’incidence des effets secondaires.
A mesure que la dose est augmentée, la prednisone, ou tout autre glucocorticoïde, commence à présenter des effets immunosuppresseurs, ce qui justifie son utilisation dans les maladies auto-immunes et les transplantations d’organes.
Dans les maladies auto-immunes et les glomérulonéphrites, nous pouvons utiliser jusqu’à 80 mg de prednisone par jour. Dans les cas graves, nous utilisons une procédure appelée thérapie pulsée, qui consiste à administrer par voie intraveineuse jusqu’à 1000 mg de méthylprednisolone pendant 3 jours consécutifs. Cette thérapie pulsée peut être utilisée dans les vascularites sévères, dans les cas de rejet d’organes transplantés et dans le traitement des maladies auto-immunes sévères et décompensées, comme cela se produit dans certains cas de lupus, par exemple.
Les corticostéroïdes peuvent être administrés par différentes voies. Par exemple, les corticoïdes systémiques sont ceux pris par voie orale ou intraveineuse. Dans l’asthme, l’administration de corticostéroïdes inhalés est très fréquente. Dans la rhinite et la sinusite, la voie préférée est intranasale. Dans les maladies de la peau, les corticoïdes sont topiques, c’est-à-dire sous forme de crèmes ou de pommades. Les corticoïdes sont disponibles sous forme de gouttes pour les yeux et de solutions à administrer dans les oreilles. Dans l’arthrite, la voie peut être intra-articulaire (infiltration).
Absorption systémique
La grande majorité des effets secondaires surviennent chez les patients prenant des corticostéroïdes oraux ou intraveineux à dose élevée et prolongée. Cela ne signifie pas pour autant que les autres formes d’administration des corticostéroïdes sont exemptes d’effets indésirables.
Les corticostéroïdes inhalés, largement utilisés dans le traitement de l’asthme, peuvent avoir une absorption systémique pertinente, bien qu’elle soit bien moindre que celle qui se produit avec les corticostéroïdes administrés par voie orale. La fluticasone inhalée, par exemple, est connue pour inhiber la production de cortisol par la glande surrénale et peut provoquer des effets secondaires systémiques lorsqu’elle est utilisée en continu pendant plusieurs mois, en particulier chez les enfants. D’autres formes de corticostéroïdes inhalés semblent avoir une absorption systémique plus faible.
Les injections intra-articulaires de dexaméthasone peuvent provoquer un syndrome de Cushing (j’explique plus loin ce qu’est cette modification).
Même les corticostéroïdes en pommade ou en crème peuvent être absorbés dans l’organisme de manière suffisante pour provoquer des effets secondaires s’ils sont utilisés de manière prolongée. L’absorption des corticostéroïdes par la peau varie en fonction d’un certain nombre de facteurs. Par exemple, les zones telles que les plis de la peau, le cuir chevelu et le front sont plus susceptibles d’être absorbées. Chez les enfants et dans les zones présentant une inflammation de la peau ou une desquamation, l’absorption systémique des corticostéroïdes est également plus importante.
En général, aucune forme de corticostéroïde n’est exempte d’effets secondaires. Quelle que soit la voie d’administration, plus la durée du traitement et la dose utilisée sont longues, plus les risques d’effets indésirables sont élevés.
Effets secondaires
Bien qu’ils soient des médicaments extrêmement utiles dans une variété de maladies graves, les corticostéroïdes ont, surtout s’ils sont utilisés à long terme, une énorme liste d’effets secondaires indésirables, allant de problèmes cosmétiques à des infections graves dues à l’inhibition du système immunitaire.
Les effets secondaires sont étroitement liés à la dose et à la durée d’utilisation. Une utilisation sporadique et à court terme n’est pas susceptible d’entraîner les effets indésirables qui seront décrits ci-dessous. Il n’y a pas lieu de s’inquiéter de prescrire des corticoïdes pour une semaine seulement, même s’ils sont à fortes doses. L’utilisation sera indiquée chaque fois que le médecin juge que la maladie à traiter est plus grave que les effets indésirables potentiels.
Après avoir lu cet article, vous avez peut-être l’impression que la prednisone et les médicaments similaires sont des médicaments terribles. Il est important de noter que l’utilisation prolongée de fortes doses n’est généralement indiquée que dans les maladies graves, qui peuvent entraîner la mort ou des limitations sévères.
Effets secondaires cutanés
Les effets esthétiques des corticostéroïdes sont ceux qui gênent le plus les patients, en particulier les femmes. Environ la moitié des personnes utilisant au moins 20 mg par jour de prednisone, ou une dose équivalente de tout autre corticostéroïde pendant trois mois ou plus, présenteront des effets secondaires esthétiques.
Les plus fréquents d’entre eux sont les ecchymoses et le purpura associés aux corticostéroïdes. Ces modifications sont de petites hémorragies qui se produisent sous la peau, généralement dans les zones exposées au soleil comme les mains et les avant-bras. Un autre effet indésirable fréquent est une peau plus fine et plus fragile.
Des stries de couleur violette situées dans la région abdominale, la calvitie, la pousse des cheveux chez les femmes et l’acné sont également fréquentes chez les utilisateurs chroniques de corticostéroïdes oraux.
Le risque de cancers de la peau de type non mélanome semble être plus élevé chez les personnes prenant des corticostéroïdes pendant une période prolongée.
Les patients qui prennent des corticostéroïdes sous forme de crèmes et de pommades pendant une longue période peuvent également subir des effets indésirables sur la peau, tels que l’atrophie, les vergetures, la téléangiectasie et les taches violettes. Un risque accru d’infections fongiques de la peau survient également en cas de traitement prolongé.
Un signe typique de toxicité des corticostéroïdes est le développement de l’aspect « cushingoïde », qui se caractérise par un visage arrondi (appelé faciès lunaire), une accumulation de graisse dans la région postérieure du cou et du dos (appelée bosse ou giba de buffle), et une répartition inégale de la graisse corporelle, avec une prédominance dans la région abdominale et le tronc.
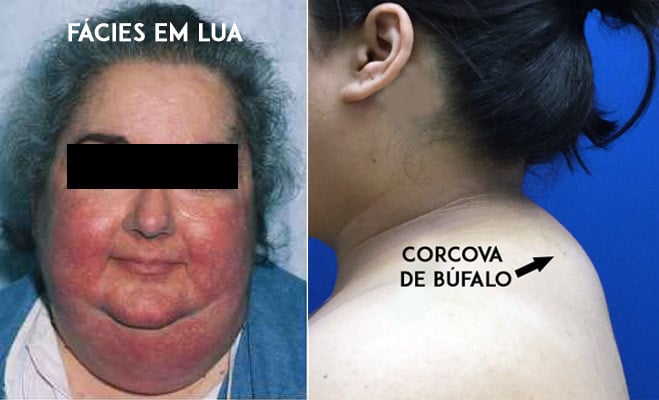
Cet ensemble d’effets secondaires, appelé syndrome de Cushing, est l’un des plus gênants, car il modifie considérablement l’apparence du patient, en particulier chez les personnes qui étaient auparavant minces.
Le syndrome de Cushing apparaît généralement dans les deux premiers mois de traitement par corticoïdes à des doses supérieures à 20 mg par jour. Chez certains patients, cependant, des doses supérieures à 10 mg par jour sont déjà suffisantes pour provoquer cette modification.
Effets secondaires oculaires
L’utilisation continue de corticostéroïdes systémiques, généralement pendant plus d’un an avec des doses supérieures à l’équivalent de 10 mg de prednisone par jour, peut entraîner des modifications ophtalmologiques, telles que la cataracte et le glaucome. Les corticostéroïdes utilisés par voie orale, nasale (spray nasal pour l’asthme ou la bronchite) ou sous forme de collyre peuvent provoquer ces deux maladies.
Les patients qui prennent des corticostéroïdes de façon chronique doivent être évalués périodiquement par un ophtalmologiste afin de détecter les signes précoces de cataracte ou de glaucome.
Effets métaboliques
Après une dose de 5 mg par jour, il existe une nette tendance à la prise de poids et à l’accumulation de graisse dans la région du tronc et de l’abdomen. Plus la dose de corticoïde est élevée, plus la prise de poids est importante.
En plus de l’accumulation de graisse, la corticothérapie chronique entraîne également des altérations du métabolisme du glucose, et peut même provoquer un diabète sucré. Le risque est plus élevé chez les personnes qui présentent déjà des valeurs de glucose légèrement altérées avant le début de la corticothérapie. Bien que le diabète soit réversible dans la plupart des cas après l’arrêt du médicament, certains patients restent diabétiques à vie.
Des doses quotidiennes de prednisone supérieures à 10 mg pendant plus de 3 mois peuvent également entraîner des modifications du taux de cholestérol, à savoir une élévation du LDL-cholestérol (mauvais cholestérol) et des triglycérides, et une diminution du HDL-cholestérol (bon cholestérol).
Effets cardiovasculaires
L’incidence de diverses maladies cardiovasculaires augmente généralement avec l’utilisation prolongée de corticostéroïdes. On peut citer la survenue accrue d’hypertension, d’infarctus du myocarde, d’insuffisance cardiaque et d’accident vasculaire cérébral.
Le risque de maladie cardiovasculaire dépend de la dose et de la durée du traitement. Les patients qui développent un syndrome de Cushing ont généralement le taux le plus élevé d’athérosclérose et le risque le plus élevé de problèmes cardiaques.
De petites doses de corticostéroïdes pendant une courte période ne semblent pas augmenter le risque cardiovasculaire de manière pertinente.
Effets musculo-squelettiques
L’utilisation chronique de glucocorticoïdes est associée à plusieurs changements musculo-squelettiques. La plus courante est l’ostéoporose. Dans ce cas, même de faibles doses comme 2,5 mg ou 5 mg par jour, si elles sont utilisées de façon chronique, peuvent accélérer la perte de masse osseuse.
La corticothérapie prolongée est également responsable d’une incidence accrue de nécrose osseuse, de lésions musculaires (myopathie), de fractures osseuses et de troubles de la croissance lorsqu’elle est utilisée chez les enfants.
Effets secondaires sur le système nerveux central
L’utilisation de corticostéroïdes, au début, peut provoquer une sensation de bien-être et d’euphorie. Cependant, à long terme, elle est associée à une incidence plus élevée de troubles psychiatriques, tels que la psychose et la dépression, ainsi que l’insomnie et les altérations de la mémoire.
Effets immunologiques
L’immunosuppression provoquée par la corticothérapie est un effet souhaitable en cas de maladies auto-immunes, mais elle peut aussi être un gros problème, car elle facilite la survenue d’infections. Il faut savoir bien équilibrer les risques et les bénéfices.
Le risque d’infection se pose chez ceux qui prennent l’équivalent de 10 mg par jour ou plus de prednisone pendant plusieurs jours. Ce risque devient très élevé avec des doses supérieures à 40 mg par jour ou lorsqu’une dose cumulée de 700 mg de prednisone est obtenue sur l’ensemble du traitement.
En plus de faciliter l’infection, les corticoïdes inhibent également l’apparition de la fièvre, rendant difficile la reconnaissance d’un processus infectieux en cours.
Les patients sous fortes doses de corticoïdes doivent éviter les vaccins composés de virus vivants, au risque de développer des infections vaccinales. Des vaccins contenant des virus tués peuvent être administrés, mais la corticothérapie peut également empêcher la formation d’anticorps, ce qui rend l’immunisation peu efficace. Des doses plus importantes sont souvent nécessaires pour une immunisation efficace.
La candidose orale et la candidose vaginale sont des infections très fréquentes chez les patients sous glucocorticoïdes chroniques.
Autres effets
La liste des effets secondaires possibles des corticoïdes est très étendue. Outre ceux déjà mentionnés, d’autres effets indésirables relativement fréquents sont la rétention d’eau, les modifications menstruelles, la gastrite, l’ulcère gastroduodénal, la stéatose hépatique, la pancréatite et l’infertilité.
Soins et dangers de l’utilisation des corticostéroïdes
La corticothérapie prolongée nécessite certaines précautions, notamment lors de l’arrêt du médicament.
L’utilisation à long terme de la prednisone ou de médicaments similaires inhibe la production naturelle de cortisol par la glande surrénale. Les corticostéroïdes synthétiques n’ayant une demi-vie que de quelques heures, un arrêt brutal fait que le taux de cortisol est proche de zéro après 2 ou 3 jours. Lorsque la surrénale est inhibée pendant une longue période par l’administration de corticostéroïdes exogènes, il faut du temps avant qu’elle ne se remette à produire naturellement du cortisol.
En général, les traitements qui durent moins de 3 semaines n’entraînent pas d’effets secondaires majeurs ni d’inhibition prolongée des surrénales.
Comme le cortisol est une hormone essentielle à la vie, le patient qui arrête brutalement les corticoïdes de synthèse entre dans un état appelé insuffisance surrénale, et peut évoluer vers un choc circulatoire, un coma et la mort s’il n’est pas pris en charge rapidement.
C’est pourquoi le retrait des corticoïdes après une utilisation prolongée doit toujours se faire lentement et progressivement. Le traitement ne doit jamais être interrompu sans connaissance médicale.
Références
- Corticothérapie systémique – effets secondaires et leur gestion –
British Journal of Ophthalmology. - Revue : Effets secondaires à long terme des glucocorticoïdes – Journal Expert Opinion on Drug Safety.
- Glucocorticoïdes – Projet de sensibilisation à la maladie de Huntington pour l’éducation, à Stanford.
- Prévention et traitement des effets secondaires des glucocorticoïdes systémiques – Journal international de dermatologie.
- Utilisation pharmacologique des glucocorticoïdes – UpToDate.
- Effets secondaires majeurs des glucocorticoïdes systémiques – UpToDate.
- Effets indésirables des corticostéroïdes – StatPearls.
Laisser un commentaire