|
|
Tässä artikkelissa on useita ongelmia. Auta parantamaan sitä tai keskustele näistä asioista keskustelusivulla. (Opi miten ja milloin voit poistaa nämä malliviestit)
(Opi, miten ja milloin voit poistaa tämän malliviestin) |
Monosakkaridit (kreikankielisestä sanasta monos: yksinäinen, sakkar: sokeri), joita kutsutaan myös nimellä yksinkertaiset sokerit (simple sugars), ovat sokereiden yksinkertaisimpia sokerilajikkeita ja perustavimpia yksiköitä (monomeerejä) hiilihydraatteja. Yleinen kaava on C
nH
2nO
n, joskaan kaikki tähän kaavaan sopivat molekyylit (esim. etikkahappo) eivät ole hiilihydraatteja. Ne ovat yleensä värittömiä, vesiliukoisia ja kiteisiä kiinteitä aineita. Nimestään (sokerit) poiketen vain joillakin monosakkarideilla on makea maku.
Monosakkarideja ovat esimerkiksi glukoosi (dekstroosi), fruktoosi (levuloosi) ja galaktoosi. Monosakkaridit ovat disakkaridien (kuten sakkaroosi ja laktoosi) ja polysakkaridien (kuten selluloosa ja tärkkelys) rakennusaineita. Jokainen hydroksyyliryhmää kannattava hiiliatomi on kiraalinen, lukuun ottamatta ketjun päässä olevia hiiliatomeja. Näin syntyy useita isomeerimuotoja, joilla kaikilla on sama kemiallinen kaava. Esimerkiksi galaktoosi ja glukoosi ovat molemmat aldoheksooseja, mutta niillä on erilainen fysikaalinen rakenne ja erilaiset kemialliset ominaisuudet.
Monosakkaridilla glukoosilla on keskeinen rooli aineenvaihdunnassa, jossa kemiallista energiaa uutetaan glykolyysin ja sitruunahappokierron avulla elävien organismien energian tuottamiseksi. Joitakin muita monosakkarideja voidaan muuttaa elävässä organismissa glukoosiksi.
Rakenne ja nimikkeistö
Monosakkarideilla on muutamaa poikkeusta (esim. deoksiriboosi) lukuun ottamatta tämä kemiallinen kaava: (CH2O)x, jossa tavallisesti x ≥ 3. Monosakkaridit voidaan luokitella niiden sisältämien hiiliatomien lukumäärän x mukaan: trioosi (3), tetroosi (4), pentoosi (5), heksoosi (6), heptoosi (7) ja niin edelleen.
Glukoosi, jota käytetään energianlähteenä ja tärkkelyksen, glykogeenin ja selluloosan synteesissä, on heksoosi. Riboosi ja deoksiriboosi (RNA:ssa ja DNA:ssa) ovat pentoosisokereita. Esimerkkejä heptooseista ovat ketoosit, mannoheptuloosi ja sedoheptuloosi. Monosakkarideja, joissa on kahdeksan tai enemmän hiiltä, havaitaan harvoin, koska ne ovat melko epävakaita. Vesiliuoksissa monosakkaridit esiintyvät renkaina, jos niissä on enemmän kuin neljä hiiltä.
Lineaariketjuiset monosakkaridit
Yksinkertaisilla monosakkarideilla on lineaarinen ja haarautumaton hiilirunko, jossa on yksi funktionaalinen karbonyyliryhmä (C=O) ja yksi hydroksyyliryhmä (OH) kussakin jäljelle jäävässä hiiliatomissa. Näin ollen yksinkertaisen monosakkaridin molekyylirakenne voidaan kirjoittaa muodossa H(CHOH)n(C=O)(CHOH)mH, jossa n + 1 + m = x; joten sen alkuainekaava on CxH2xOx.
Konventionaalisesti hiiliatomit numeroidaan 1:stä x:ään pitkin selkärankaa alkaen siitä päästä, joka on lähimpänä C=O-ryhmää. Monosakkaridit ovat hiilihydraattien yksinkertaisimmat yksiköt ja sokerin yksinkertaisin muoto.
Jos karbonyyli on asemassa 1 (eli n tai m on nolla), molekyyli alkaa formyyliryhmällä H(C=O)- ja on teknisesti aldehydi. Tällöin yhdisteestä käytetään nimitystä aldoosi. Muussa tapauksessa molekyylissä on ketoryhmä, karbonyyli -(C=O)- kahden hiilen välissä; tällöin se on muodollisesti ketoni, ja sitä kutsutaan ketoosiksi. Biologisesti kiinnostavien ketoosien karbonyyli on tavallisesti asemassa 2.
Yllä olevia eri luokitteluja voidaan yhdistää, jolloin saadaan esimerkiksi nimitykset ”aldoheksoosi” ja ”ketotrioosi”.
Avoketjuisten monosakkaridien yleisemmässä nimikkeistössä yhdistetään hiilarien lukumäärää osoittava kreikkalainen etuliite (tri-, tetr-, pent-, heks- jne.) ja aldoosien suffiksit ”-oosi” ja ketoosien ”-uloosi”. Jälkimmäisessä tapauksessa, jos karbonyyli ei ole asemassa 2, sen sijainti ilmoitetaan numeerisella infiksillä. Esimerkiksi H(C=O)(CHOH)4H on pentoosi, H(CHOH)(C=O)(CHOH)3H on pentuloosi ja H(CHOH)2(C=O)(CHOH)2H on pent-3-uloosi.
Avoketjuiset stereoisomeerit
Kaksi monosakkaridia, joilla on ekvivalentti molekyylikaavio (sama ketjun pituus ja sama karbonyyliasento), voivat silti olla erillisiä stereoisomeerejä, joiden molekyylit eroavat toisistaan avaruudellisen orientaation suhteen. Näin tapahtuu vain, jos molekyyli sisältää stereogeenisen keskuksen, tarkemmin sanottuna hiiliatomin, joka on kiraalinen (liittyy neljään eri molekyylin alarakenteeseen). Näillä neljällä sidoksella voi olla mikä tahansa kahdesta avaruuskonfiguraatiosta, jotka eroavat toisistaan kätisyyden perusteella. Yksinkertaisessa avoketjuisessa monosakkaridissa jokainen hiili on kiraalinen lukuun ottamatta ketjun ensimmäistä ja viimeistä atomia sekä (ketooseissa) hiiltä, jossa on ketoryhmä.
Esimerkiksi triketoosilla H(CHOH)(C=O)(CHOH)(CHOH)H (glyseroni, dihydroksiasetoni) ei ole stereogeenistä keskusta, ja siksi se on olemassa yhtenä stereoisomeerinä. Toisessa trioosissa, aldoosissa H(C=O)(CHOH)2H (glyseraldehydi), on yksi kiraalinen hiili – keskeinen hiili numero 2 – joka on sitoutunut ryhmiin -H, -OH, -C(OH)H2 ja -(C=O)H. Tämä hiili on kiraalinen. Siksi se on olemassa kahtena stereoisomeerinä, joiden molekyylit ovat toistensa peilikuvia (kuten vasen ja oikea hanska). Monosakkaridit, joissa on neljä tai useampia hiilareita, voivat sisältää useita kiraalisia hiilareita, joten niillä on tyypillisesti enemmän kuin kaksi stereoisomeeria. Saman kaavion omaavien erillisten stereoisomeerien lukumäärää rajoittaa 2c, jossa c on kiraalisten hiilien kokonaismäärä.
Fischerin projektio on systemaattinen tapa piirtää asyklisen monosakkaridin luurankokaava siten, että jokaisen kiraalisen hiilen kätisyys on hyvin määritelty. Yksinkertaisen avoketjuisen monosakkaridin jokainen stereoisomeeri voidaan tunnistaa kiraalisten hydroksyylien (kiraalisiin hiileihin kiinnittyneiden hydroksyylien) sijainnin (oikealle tai vasemmalle) perusteella Fischerin kaaviossa.
Useimmat stereoisomeerit ovat itsessään kiraalisia (eroavat peilikuvistaan). Fischerin projektiossa kaksi peilikuvallista isomeeria eroavat toisistaan siten, että kaikkien kiraalisten hydroksyylien sijainnit on käännetty oikealta vasemmalle. Peilikuvalliset isomeerit ovat kemiallisesti identtisiä ei-kiraalisissa ympäristöissä, mutta niillä on yleensä hyvin erilaiset biokemialliset ominaisuudet ja esiintymät luonnossa.
Vaikka useimmat stereoisomeerit voidaan järjestää pareittain peilikuvallisiksi muodoiksi, on olemassa joitakin ei-kiraalisia stereoisomeerejä, jotka ovat identtisiä peilikuvansa kanssa huolimatta siitä, että niillä on kiraaliset keskukset. Näin tapahtuu aina, kun molekyylin kuvaaja on symmetrinen, kuten 3-ketopentoosissa H(CHOH)2(CO)(CHOH)2H, ja molemmat puoliskot ovat toistensa peilikuvia. Tällöin peilaus vastaa puolen kierroksen kiertoa. Tästä syystä 3-ketopentoosin stereoisomeerejä on vain kolme erillistä, vaikka molekyylissä on kaksi kiraalista hiiltä.
Erillisillä stereoisomeereillä, jotka eivät ole toistensa peilikuvia, on yleensä erilaiset kemialliset ominaisuudet, myös ei-kirallisissa ympäristöissä. Siksi kullekin peiliparille ja kullekin ei-kiraaliselle stereoisomeerille voidaan antaa erityinen monosakkaridien nimi. Esimerkiksi aldoheksoosin stereoisomeerejä on 16 erilaista, mutta nimi ”glukoosi” tarkoittaa tiettyä peilikuvaparia aldoheksooseja. Fischer-projektiossa toisen glukoosin isomeerien hydroksyyli on vasemmalla puolella C3:ssa ja oikealla puolella C4:ssä ja C5:ssä, kun taas toisen isomeerin kuvio on päinvastainen. Näillä erityisillä monosakkaridien nimillä on tavanomaiset kolmikirjaimiset lyhenteet, kuten ”Glu” glukoosille ja ”Thr” treoosille.
Yleisesti monosakkaridilla, jossa on n epäsymmetristä hiiltä, on 2n stereoisomeeria. Aldoosimonosakkaridin avoimen ketjun stereoisomeerien lukumäärä on yhdellä suurempi kuin samanpituisen ketoosimonosakkaridin. Jokaisella ketoosilla on 2(n-3) stereoisomeeria, jossa n > 2 on hiilivetyjen lukumäärä. Jokaisella aldoosilla on 2(n-2) stereoisomeeria, joissa n > 2 on hiilivetyjen lukumäärä.Näitä kutsutaan myös epimeereiksi, joiden epäsymmetristen tai kiraalisten hiiliatomien -OH- ja -H-ryhmät ovat asettuneet eri tavalla (tämä ei koske niitä hiilivetyjä, joissa on karbonyylifunktionaalinen ryhmä).
Monosakkaridien konfiguraatio
Kuten monet kiraaliset molekyylit, glyseraldehydin kaksi stereoisomeeria kääntävät vähitellen lineaarisesti polarisoidun valon polarisaatiosuuntaa sen läpikulkiessa, jopa liuoksessa. Nämä kaksi stereoisomeeria merkitään etuliitteillä D- ja L- pyörimissuunnan mukaan: D-glyseraldehydi on dekstroottinen (kiertää polarisaatioakselia myötäpäivään), kun taas L-glyseraldehydi on levorottinen (kiertää sitä vastapäivään).

D- ja L- etuliitteitä käytetään myös muiden monosakkaridien yhteydessä erottamaan kaksi tiettyä stereoisomeeria, jotka ovat toistensa peilikuvia. Tätä tarkoitusta varten tarkastellaan sitä kiraalista hiiltä, joka on kauimpana C=O-ryhmästä. Sen neljän sidoksen on liityttävä -H:hon, -OH:hon, -C(OH)H:hon ja muuhun molekyyliin. Jos molekyyliä voidaan kiertää avaruudessa siten, että näiden neljän ryhmän suunnat vastaavat D-glyseraldehydin C2:n analogisten ryhmien suuntia, isomeeri saa etuliitteen D-. Muussa tapauksessa se saa L- etuliitteen.
Fischer-projektiossa D- ja L- etuliitteet määrittelevät sen hiiliatomin konfiguraation, joka on toiseksi alimpana: D-, jos hydroksyyli on oikealla puolella, ja L-, jos se on vasemmalla puolella.
Huomaa, että D- ja L- etuliitteet eivät ilmaise polarisoidun valon pyörimissuuntaa, joka on kaikkien kiraalisten keskusten järjestelyjen yhteisvaikutus. Molemmat enantiomeerit kuitenkin pyörittävät valoa aina vastakkaisiin suuntiin saman verran. Katso myös D/L-järjestelmä.
Monosakkaridien syklisoituminen
Monosakkaridi siirtyy usein asyklisestä (avoketjuisesta) muodosta sykliseen muotoon nukleofiilisen additioreaktion kautta karbonyyliryhmän ja jonkin saman molekyylin hydroksyylien välillä. Reaktiossa syntyy hiiliatomien rengas, jonka sulkee yksi silloittava happiatomi. Tuloksena syntyvässä molekyylissä on hemiasetaali- tai hemiketaliryhmä riippuen siitä, oliko lineaarinen muoto aldoosi vai ketoosi. Reaktio on helppo kääntää päinvastaiseksi, jolloin saadaan alkuperäinen avoketjuinen muoto.
Näissä syklisissä muodoissa rengas on yleensä viisi tai kuusi atomia. Näitä muotoja kutsutaan vastaavasti furanoseiksi ja pyranoseiksi – analogisesti furaanin ja pyranin kanssa, jotka ovat yksinkertaisimpia yhdisteitä, joilla on sama hiili-happirengas (vaikkakin niistä puuttuvat näiden kahden molekyylin kaksoissidokset). Esimerkiksi aldiheksoosi glukoosi voi muodostaa hiilen 1 hydroksyylin ja hiilen 4 hapen välille hemiasetaalisidoksen, jolloin syntyy molekyyli, jolla on 5-jäseninen rengas, jota kutsutaan glukofuranoosiksi. Sama reaktio voi tapahtua hiilien 1 ja 5 välillä muodostaen 6-jäsenisen renkaan molekyylin, jota kutsutaan glukopyranoosiksi. Syklisiä muotoja, joissa on seitsemänatominen rengas (sama kuin oksepaanissa), joita esiintyy harvoin, kutsutaan heptooseiksi.



Monien monosakkaridien (mukaan lukien glukoosi), sykliset muodot ovat vallitsevia sekä kiinteässä tilassa että liuoksissa, ja siksi samaa nimeä käytetään yleisesti avoimen ja suljetun ketjun isomeereistä. Siten esimerkiksi termi ”glukoosi” voi tarkoittaa glukofuranoosia, glukopyranoosia, avoketjuista muotoa tai näiden kolmen sekoitusta.
Syklisoituminen synnyttää uuden stereogeenisen keskuksen karbonyyliä kantavaan hiileen. Karbonyylin hapen korvaava -OH-ryhmä voi päätyä kahteen eri asentoon renkaan keskitasoon nähden. Näin jokaisesta avoketjuisesta monosakkaridista saadaan kaksi syklistä isomeeria (anomeeria), joita merkitään etuliitteillä α- ja β-. Molekyyli voi vaihtaa näiden kahden muodon välillä mutarotaatioksi kutsutulla prosessilla, joka koostuu renkaanmuodostusreaktion kääntämisestä ja sitä seuraavasta toisesta renkaanmuodostuksesta.
Haworthin projektio
Syklisen monosakkaridin stereokemiallinen rakenne voidaan esittää Haworthin projektiona. Tässä kuvassa D-aldo-heksoosin pyranoosimuodon α-isomeerin anomeerisen hiilen -OH on hiiliatomien tason alapuolella, kun taas β-isomeerin anomeerisen hiilen -OH on tason yläpuolella. Pyranoosit omaksuvat tyypillisesti tuolikonformaation, joka muistuttaa sykloheksaanin konformaatiota. Tässä konformaatiossa α-isomeerin anomeerisen hiilen -OH on aksiaalisessa asennossa, kun taas β-isomeerin anomeerisen hiilen -OH on ekvatoriaalisessa asennossa (tarkastellaan D-aldo-heksoosisokereita).
-
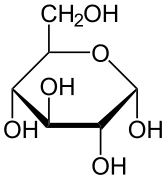
α-D-Glucopyranose
-

β-D-glukopyranoosi
Johdannaiset
On olemassa suuri määrä biologisesti tärkeitä muunnettuja monosakkarideja:
- Aminosokereita, kuten:
- galaktosamiini
- glukosamiini
- sialiinihappo
- N-asetyyliglukosamiini
- Sulfosokereita, kuten:
- sulfokinovoosi
- Muut, kuten:
- askorbiinihappo
- mannitoli
- glukuronihappo
Ks. myös
- Monosakkaridien nimikkeistö
- Vähennyssokeri
- Sokerihappo
- Sokerialkoholi
- Disakkaridi
.
Muistiinpanot
- ^ ”Hiilihydraatit”. Chemistry for Biologists. Royal Society of Chemistry. Haettu 10. maaliskuuta 2017.
- ^ NCERT TEXT BOOK CLaSS-12
- ^ ”Carbohydrates”. Chemistry for Biologists. Royal Society of Chemistry. Haettu 10. maaliskuuta 2017.
- ^ Pigman, William Ward; Anet, E. F. L. J. (1972). ”Chapter 4: Mutarotations and Actions of Acids and Bases”. Teoksessa Pigman ja Horton (toim.). The Carbohydrates: Chemistry and Biochemistry. 1A (2nd ed.). San Diego: Sivut 165-194.
- ^ IUPAC, Compendium of Chemical Terminology, 2nd ed. (”Kultainen kirja”) (1997). Korjattu verkkoversio: (2006-) ”Haworthin esitys”. doi:10.1351/goldbook.H02749
.


Vastaa