ORIGINAL PAPERS
Hepatiitti B:n pinta-antigeenin osoittaminen käyttäen yhdistettyjä seerumeita. A cost-benefit analysis
E. Fernández, L. Rodrigo1, S. García, S. Riestra1 ja C. Blanco
Biokemian yksikkö. Hospital de Cabueñes. Gijón. 1Gastroenterologian yksikkö. Hospital Central de Asturias. Oviedo. Espanja
Kirjeenvaihto
ABSTRACT
Tavoitteet: tutkia toteutettavuutta ja tehdä kustannus-hyötyanalyysi viiden näytteen yhdistämisstrategiasta, jossa käytetään entsyymi-immunomääritystä (EIA) hepatiitti B:n pinta-antigeenin (HBsAg) seulontaan.
Materiaali ja menetelmät: Poolausmenetelmän herkkyyden ja spesifisyyden arvioimiseksi kukin 40 positiivisesta seerumista (heikosti HBsAg-positiivisesta voimakkaasti HBsAg-positiiviseen) ja 250 negatiivisesta seerumista testattiin pooliin 4 HBsAg-negatiivisen seerumin kanssa. HBsAg/ad:n ja HBsAg/ay:n toteamisraja arvioitiin käyttäen puhdistettujen alatyyppien seerumeita. Tutkimus tehtiin todellisissa olosuhteissa 340 raskaana olevan naisen seerumipoolilla.
Tulokset: Tämän tekniikan herkkyys ja spesifisyys olivat 100 %. Yksittäisissä ja yhdistetyissä olosuhteissa tutkittujen 40 näytteen näyte/leikkaussuhteiden välinen korrelaatiokerroin oli 0,792 (p < 0,005). Yhdistelmämenetelmässä HBsAg/ad:n ja HBsAg/ay:n havaitsemisaste on alhaisempi, 0,20 ng/ml ja 0,12 ng/ml, ja yksittäisessä menetelmässä 0,34 ng/ml ja 0,29 ng/ml. Pooling-menetelmä ei menetä herkkyyttään enintään 100 IU/L anti-HB:n arvoille neljässä seerumissa, jotka on sekoitettu positiivisen seerumin kanssa. Kustannus-hyötyanalyysi osoitti, että pooling-menetelmällä voitaisiin säästää 30-75 prosenttia HBsAg-määrityksen kustannuksista sen mukaan, oliko seroprevalenssi 10 prosenttia vai 1 prosentti.
Johtopäätökset: Yhdistetty HBsAg EIA ei tuottanut huonompaa tulosta kuin yksittäinen EIA-testi, ja se oli kustannustehokas ja pätevä strategia alueilla, joilla esiintyvyys on korkea, keskisuuri tai matala.
Avainsanat: Hepatiitti B:n pinta-antigeeni. Seerumien yhdistäminen. Kustannus-hyötyanalyysi.
Rodrigo L, Fernández E, García S, Riestra S, Blanco C. Hepatiitti B:n pinta-antigeenin osoittaminen käyttäen yhdistettyjä seerumeita. Kustannus-hyötyanalyysi. Rev Esp Enferm Dig 2006; 98: 112-121.
Introduction
Hepatiitti B -virusinfektio (HBV) on sairaus, joka vaikuttaa miljooniin ihmisiin maailmanlaajuisesti. Sen pääasiallinen reservuaari on krooniset HBV:n kantajat. On arvioitu, että noin 300 miljoonaa ihmistä koko maailmassa on saanut tämän viruksen tartunnan (1). HBV-infektion lääketieteelliset seuraukset ovat sekä vaihtelevia että ennalta arvaamattomia ja riippuvat muun muassa potilaan iästä ja immuunipuolustuksesta. HBV on tunnetusti kroonisen hepatiitin, maksakirroosin ja hepatosellulaarisen karsinooman etiologinen aiheuttaja.
Infektion esiintyvyydessä on kuitenkin suuria eroja, ja tämä on johtanut siihen, että on muodostettu kolme suurta aluetta, joilla on korkea, keskisuuri ja matala endeemisyys (2). Useimmissa kehittyneissä maissa kroonisten HBV:n kantajien esiintyvyys on alle 2 %, ja tartunnan siirtyminen tapahtuu ennen kaikkea tiettyihin riskiryhmiin kuuluvilla aikuisilla (huumeiden käyttäjät, homoseksuaaliset miehet, promiskuusi heteroseksuaalit, terveydenhuollon työntekijät) (3). Espanjassa HBV:n kantajien esiintyvyyden on todettu olevan 1,2 prosenttia (4), ja HBsAg:n tunnistaminen verenluovuttajilta, raskaana olevilta naisilta ja henkilöiltä, jotka osallistuvat automaattisiin verensiirto-ohjelmiin, on pakollista.
Seerumin yhdistämistekniikalla pyritään alentamaan kustannuksia menettämättä tehoa, ja sitä on käytetty pääasiassa kehitysmaissa etsittäessä vasta-aineita inhimillistä immuunikatovirusta (HI-virusta) (5-14) ja hepatiitti C -virusta (HCV) (15-19) vastaan. Menetelmällä saadut tulokset ovat osoittautuneet erittäin lupaaviksi, sillä ne ovat vähentäneet merkittävästi laboratoriotestien kustannuksia ilman, että niiden herkkyys on merkittävästi heikentynyt.
Tässä tutkimuksessa pyritään arvioimaan, voidaanko seerumin yhdistämistekniikkaa soveltaa HBsAg:n osoittamiseen, selvittämään tekijöitä, jotka voivat muuttaa sen herkkyyttä, ja suorittamaan kustannus-hyötyanalyysi tälle diagnostiselle menetelmälle.
Materiaali ja menetelmät
HBsAg:n määritys
HBsAg:n arviointiin käytettiin Imx HBsAg -määritystä (Abbott Laboratories, Abbott Park, IL), joka on kvalitatiivinen kolmannen sukupolven mikropartikkelien entsyymi-immunomääritys (EIA). HBsAg:n esiintyminen tai puuttuminen määritetään vertaamalla fluoresoivan tuotteen muodostumisnopeutta raja-arvoon, joka lasketaan negatiivisen kalibraattorin (N) nopeudesta (ihmisplasma, joka ei reagoi HBsAg:n suhteen). Imx HBsAg -määritys laskee näytteen (S) nopeuden ja negatiivisen kalibraattorin nopeuden suhteen. Yhden seerumin EIA:n raja-arvoksi (S/N) vahvistettiin 2.
Pooling-tekniikka suoritetaan lisäämällä 200 mcL pooliin, eli saamalla seos, jossa on 40 mcL kutakin poolin muodostavaa viittä seerumia (laimennus 1/5). Raja-arvoksi vahvistettiin negatiivisten näytteiden keskiarvo lisättynä kolmella keskihajonnalla, jolloin arvoksi saatiin 1. Näin ollen katsotaan, että tässä viiden näytteen ryhmässä on ei-reaktiivinen näyte, kun S/N-kerroin on < raja-arvo, kun taas S/N-poolin raja-arvo > voi viitata vähintään yhden reaktiivisen näytteen olemassaoloon. Tällöin on tarpeen testata yksittäiset näytteet uudelleen reaktiivisen näytteen (reaktiivisten näytteiden) tunnistamiseksi. Kaikki testit tehdään kahtena kappaleena.
Edellä esitetyn mukaisesti spesifisyys arvioitiin arvioimalla HBsAg:n määrä 50:ssä 250:n negatiivisen seerumin poolissa. Herkkyyden laskemiseksi testattiin 40 seerumia, joiden pitoisuusjakauma oli sama kuin yleispopulaatiossa, josta ne otettiin näytteeksi, pooliin, jossa oli 4 negatiivista seerumia.
HBsAg-alatyypit (ad ja ay)
Imx HBsAg:n havaitsemisraja ad:n ja ay:n osalta arvioitiin käyttäen seerumeita, jotka olivat peräisin puhdistettujen HBsAg-alatyyppien paneelista (hepatiitti-HBsAg-herkkyyspaneeli, Abbott Laboratories). HBsAg/ad- ja HBsAg/ay-pitoisuudet vaihtelivat välillä 0,13-2,32 ng/ml ja välillä 0,21-2,24 ng/ml. Havaitsemisraja määritettiin yksittäisistä seerumeista ja 4 HBsAg-negatiivista seerumia sisältävästä poolista.
HBs-vasta-ainepitoisuuden vaikutus
Voidaksemme selvittää, voisiko HBs-vasta-aineiden esiintyminen yhdistelmätestillä tutkituissa seerumeissa neutralisoida HBsAg:n ja häiritä tekniikan herkkyyttä, sovelsimme menetelmää, jossa seerumi, jonka HBsAg/ad- ja HBsAg/ay-pitoisuudet olivat tunnettuja, yhdistettiin neljään seerumiin, joiden HBs-vasta-aineiden titterit olivat tunnettuja.
Anti-HBs:n kvantitatiivinen määritys tehtiin mikropartikkeli-entsyymi-immunomääritysmenetelmällä (mEIA) käyttäen AxSYm-autoanalysaattoria (AxSYmTM AUSAB, Abbott Laboratories, Abbott Park, IL). Korkean anti-HBs-titterin omaavat seerumit saatiin HBV-rokotuksen jälkeen rokotetuilta kontrolleilta ja hepatiitti B:stä toipuneilta potilailta.
Pool-testi HBsAg:n seulonnassa
Pool-testauksen validiteetin arvioimiseksi suoritettiin kenttätoiminnan simulaatio edellä esitetyllä menetelmällä 1525 seeruminäytteellä, jotka saatiin raskaana olevilta naisilta aiemmassa tutkimuksessamme HCV-infektion yleisyyden arvioimiseksi ja joiden näytteet säilytettiin keräilystä lähtien lämpötilassa, joka oli ollut -20 ºC. Näistä valittiin satunnaisesti 300 HBsAg-negatiivista ja 14 HBsAg-positiivista näytettä. Määritykset tehtiin ilman aiempaa tietoa poolin koostumuksesta.
Testien määrän vähentäminen
Kun poolin tulos on positiivinen, jokainen komponentti on testattava erikseen uudelleen HBsAg-positiivisen näytteen tai näytteiden tunnistamiseksi. Näin ollen mitä suurempi on positiivisten poolien määrä (eli HBsAg:n esiintyvyys), sitä pienempi on suoritettavien testien määrän väheneminen.
Tämän perusteella testien määrän prosentuaalinen väheneminen käytettäessä HBsAg:n seulontaan yhdistettyjä seerumeita laskettiin kaikkein epäsuotuisimmissa ja epätodennäköisimmissä olosuhteissa (alhainen esiintyvyys) eli silloin, kun missään poolista ei esiintynyt enempää kuin yksi positiivinen seerumi. Esimerkiksi jos HBsAg-seroprevalenssi on 2 %, jos 100 seerumia analysoidaan 20 poolista, näistä 2 on positiivisia. Näin ollen on tarpeen lisätä 10 määritystä (10 seerumia, jotka testataan uudelleen yksitellen) 20 alkuperäiseen määritykseen (20 poolia), jolloin saadaan yhteensä 30 määritystä. Tässä esimerkissä voidaan säästää 70 prosenttia kustannuksista. Kustannus-hyötyanalyysin tekemiseksi HBsAg-testauksen hinnaksi arvioitiin 3 Yhdysvaltain dollaria näytettä kohti. Tämä perustuu kaupallisen sarjan todelliseen keskihintaan sairaalassamme.
Tilastollinen analyysi
Tiedot kerättiin tietokantaan ja analysoitiin myöhemmin SPSS for Windows -tilastopaketin Release 10.0:n avulla. Käytettiin Spearmanin ei-parametrista lineaarista korrelaatiota. Tulokset ilmaistaan keskiarvona ± SD. Tasoa p < 0,05 pidettiin tilastollisesti merkitsevänä.
Tulokset
Yksikään 50:stä HBsAg-negatiivisen seerumin poolista ei osoittautunut positiiviseksi (S/N-pooli > 1), ja S/N-poolin arvot olivat seuraavat: 0,767 ± 0,076 (vaihteluväli 0,67-0,88). Tämän näytteen kohdalla poolitekniikan spesifisyys oli siis 100 %. Toisaalta kaikki 40 HBsAg-positiivista seerumia, kun ne määritettiin yhdistettynä, antoivat S/N-arvot, jotka olivat suuremmat kuin 1 (jolloin herkkyys oli myös 100 %). Näiden 40 näytteen S/N-suhteiden välinen korrelaatiokerroin oli 0,792 (p < 0,05).
Kahdellakymmenelläkuudellakymmenelläkymmenelläkuudelläkuudellakymmenellä prosentilla näytteistä, joiden näytteillä oli korkea HBsAg-tiitteri, S/N-suhde oli jopa suurempi kuin yksittäisellä näytteellä. Näytteiden, joilla oli matalat HBsAg-tiitterit (S/N single < 25, n = 12), korrelaatiokerroin oli kuitenkin erinomainen (R = 0,9739, p < 0,05), kuten voidaan nähdä (kuva 1).

Havaitsemisraja single-menetelmällä oli 0.34 ng/ml ad-alatyypin osalta ja 0,29 ng/ml ay-alatyypin osalta, kun taas pooling-menetelmällä havaittiin alhaisemmat antigeenipitoisuudet: 0,20 ng/ml ja 0,12 ng/ml. Tulokset, jotka saatiin sovellettaessa yksittäistä ja yhdistelmämenetelmää seerumiin, joiden HBsAg/ad- ja HBsAg/ay-pitoisuudet vaihtelivat (kuva 2).

Kun anti-HBs-titteri poolissa on alle 100 IU/L, tekniikka ei menetä herkkyyttään; jopa silloin, kun anti-HBs:n titterit nousevat 10 000 IU/L:iin, tekniikka kykenee yhä havaitsemaan HBsAg-pitoisuudet, jotka jäävät jopa alle 1,5 ng/ml:n. Eri anti-HBs-pitoisuuksien vaikutus HBsAg-alatyyppien havaitsemisrajaan pooling-menetelmää käytettäessä esitetään (kahden määrityksen keskiarvo) (kuva 3).
Todellisissa olosuhteissa raskaana olevien naisten seerumeilla tehdyssä tutkimuksessa pooling-menetelmä johti kaikkien analysoitujen näytteiden oikeaan luokitukseen. Näin ollen herkkyys ja spesifisyys olivat 100 %.
Pooling-menetelmällä saavutettu testien lukumäärän prosentuaalinen väheneminen vähenee HBsAg:n seroprevalenssin kasvaessa. On nähtävissä, että jopa 10 prosentin HBsAg-prevalenssilla tutkitussa näytteessä saavutetaan vähintään 30 prosentin säästö (kuva 4).

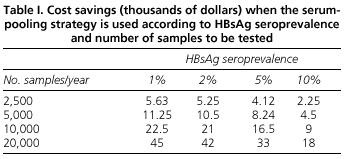
Serumipooling-strategian taloudellisten hyötyjen analyysi osoittaa, että saavutetut säästöt riippuvat sekä HBsAg:n prevalenssista että tehtävien määritysten määrästä. Näin ollen maissa, joissa esiintyvyys on alhainen, kuten meillä, pooling-menetelmä vähentää HBsAg:n testauskustannuksia. Arvioimme esimerkiksi, että jos laboratoriossa tehdään 2 500 määritystä yhden vuoden aikana pooling-menetelmää käyttäen, säästöt ovat 5 630 Yhdysvaltain dollaria, ja jos hyvin kiireisessä sairaalassa tehdään vuosittain 20 000 määritystä, säästöt ovat 45 000 Yhdysvaltain dollaria (taulukko I).
Keskustelu
Yhteenvetomenetelmän lähestymistapa on säilyttää reaktioseoksen laimennos ja lopullinen tilavuus jokaisessa yhdistetyssä testissä, jotta herkkyyttä ei menetettäisi, minkä vuoksi laimennosta vähennetään ja se korvataan osittain lisäseerumeilla. Tällä tavoin raja-arvoa ei tarvitse muuttaa standardimenetelmään nähden yksilöidyissä näytteissä. Tutkimuksessamme käytetty menetelmä oli kuitenkin automatisoitu ja näytteen laimennus suoritettiin autoanalysaattorilla. Tästä syystä kunkin näytteen laimennus oli 1:5, kun se sekoitettiin neljän muun seerumin kanssa. Tämän vuoksi tutkimuksessamme oli tarpeen muuttaa raja-arvoa ja rajoittaa seerumien lukumäärää pooliin, jotta herkkyyttä ei menetettäisi.
Spesifisyyden osalta on huomattava, että poolien keskiarvo oli vain hieman yli 3 keskihajontaa raja-arvosta. Näin ollen vääriä positiivisia tuloksia voidaan odottaa noin 1 prosentissa tapauksista. Mielestämme tämä on hyväksyttävää, koska spesifisyys on lähes 100 % (99,9 %). Tämän määrityksen todellisen spesifisyyden selvittämiseksi tarvitaan tutkimus, jossa otetaan suurempi määrä negatiivisia näytteitä useilta eri henkilöiltä.
Vaikka yksittäisten ja yhdistettyjen näytteiden testauksen välinen korrelaatio on hyvä, regressiosuora leikkaa X-akselin S/N-suhteen ollessa 3 (vastaava Y-arvo on 1). Tämä voi tarkoittaa sitä, että minkä tahansa näytteen, jonka S/N-suhde on yksittäisen näytteen testissä välillä 2 ja 3, arvo on alle 1 eikä sitä näin ollen havaita yhdistetyssä testissä.
Kun HBsAg-positiivisten seerumien esiintyvyys on 1 %, Liun ja muiden (19) kuvaamalla matemaattisella mallilla saavutettiin suurin mahdollinen testien lukumäärän vähennys (80,5 %) 11 seerumin poolikoolla. Mielestämme spesifisyyteen saattaa kuitenkin liittyä ongelmia, jotka johtuvat poolituksen vaikutuksesta väärien positiivisten tulosten määrään. Epäspesifisten proteiinien lisääntyminen seerumien sekoittumisen seurauksena voi lisätä taustaväriä. Kun tutkimukseemme valittu poolin koko oli 5 ja kun raja-arvo muutettiin 2:sta 1:een, herkkyydessä (väärät negatiiviset tulokset) tai spesifisyydessä (väärät positiiviset tulokset) ei havaittu menetyksiä.
Tämän tutkimuksen tulokset osoittavat, että seerumien yhdistämistekniikka HBsAg:n havaitsemiseksi on erittäin herkkä ja spesifinen, ja sen avulla voidaan myös saavuttaa huomattavia taloudellisia säästöjä. Nämä tulokset ovat samankaltaisia kuin muilla tutkijoilla, jotka ovat soveltaneet pooling-menetelmää HCV- ja HIV-infektion tutkimiseen (5-19). Tähän mennessä on raportoitu vain kahdesta tutkimuksesta (20,21), joissa pooling-menetelmää on sovellettu HBV-infektion tutkimiseen. Toisessa näistä tutkimuksista (20), joka suoritettiin rutiininomaisen synnytystä edeltävän hepatiitti B:n seulonnan yhteydessä testaamalla 10 näytepoolia, todettiin, että kroonisten kantajien esiintyvyys oli alhainen (0,43 %), ja kirjoittajat päättelivät, että tämä on kustannustehokas menetelmä ja käyttökelpoinen strategia alueilla, joilla seroprevalenssi on matala, mutta herkkyys vähenee arviolta 4,2 prosenttia. Tutkimuksessamme pooling-menetelmän soveltaminen raskaana oleviin naisiin, joiden keskuudessa HBsAg:n kroonisten kantajien esiintyvyys on 0,93 prosenttia, osoitti 100 prosentin herkkyyttä ja spesifisyyttä.
HBsAg:n kahden tärkeimmän alatyypin (ad ja ay) jakauma ympäristössämme on noin 50 % kummastakin, ja ay on yleisempi parenteraalista reittiä käyttävillä huumeriippuvaisilla (22). Olemme osoittaneet, että pooling-menetelmä parantaa herkkyyttä eli pienentää kahden tärkeimmän HBsAg-alatyypin määrittämiseen käytettävän immunomäärityksen toteamisrajaa. Pooling-tekniikkamme mahdollistaa HBsAg/ad:n havaitsemisen jopa 0,20 ng/ml ja HBsAg/ay:n havaitsemisen 0,12 ng/ml, mikä on jopa alhaisempi kuin standardimenetelmällä saadut määrät. Havainto lisääntyneestä herkkyydestä poolitestauksen yhteydessä ei ole yllättävä, koska muutkin kirjoittajat ovat raportoineet tästä (16). On tärkeää arvioida poolitesteissä käytettävän EIA-pakkauksen herkkyys, koska kaikki pakkaukset eivät välttämättä sovellu poolien seulontaan, kuten on osoitettu hepatiitti C -viruksen vasta-aineiden tapauksessa (23,24).
Anti-HB:n esiintyminen pooliseerumissa voi muuttaa tekniikan herkkyyttä, mutta vain merkittävällä tavalla, kun titterit ovat korkeammat kuin 10 000 IU/mL, mikä on havaittu vain rokotuksen jälkeisistä kontrollitutkimuksista otetuissa näytteissä; HBsAg:n määrittäminen ei ole tällaisessa tilanteessa aiheellista. Itse asiassa Cunninghan ja muut (20) havaitsivat, että vain 4,5 %:lla raskaana olevien naisten seerumeista tehdyistä poolista oli yli 7 500 IU/L:n anti-HBs-titteri. Kun otetaan huomioon tämä poolausmenetelmän herkkyyttä koskeva rajoitus, he havaitsivat, että myös herkkyys ja spesifisyys olivat noin 100 prosenttia. Tuloksemme voisivat olla toistettavissa muilla alueilla, joilla esiintyvyys on alhainen, mutta ne olisi osoitettava aiemmin alueilla, joilla HBV:n endeemisyys on korkea. Näillä alueilla suurin osa väestöstä on jo immunisoitu tätä virusta vastaan, ja on mahdollista, että seerumissa todetut anti-HBs-titterit ovat hieman koholla.
Rabenau ym. (21) tutkivat HBsAg:n serologisten testien turvallisuutta HBsAg:n varalta plasmapoolissa käyttämällä samankaltaista EIA-järjestelmää kuin meillä. Heidän tutkimuksessaan HBsAg:n havaitsemiseen vaikutti alhaiset anti-HBs-titterit 5 tunnin inkubaation jälkeen. Immuunikompleksin dissosioitumisen jälkeen HBsAg oli kuitenkin edelleen havaittavissa poolista, vaikka anti-HBs-pitoisuus olisi ollut korkea. Tutkimuksessamme osoitamme, että herkkyys heikkenee merkittävästi vain silloin, kun anti-HBs-titterit ovat yli 10 000 IU/L. Nämä erot voivat johtua siitä, että meidän tapauksessamme näytteet testattiin ilman edeltävää inkubointia. Tämä saattaa estää antigeenin neutraloitumisen immunokompleksin muodostumisen kautta.
Näin ollen uskomme, että sekä anti-HBs:n titteri seerumissa että näytteiden käsittely ennen testiä EIA:lla voivat vaikuttaa pooling-menetelmän herkkyyteen. Jokaisen laboratorion, joka haluaa käyttää tätä tekniikkaa, olisi pidettävä mielessä nämä kaksi tekijää ennen kuin se otetaan yleiseen käyttöön.
WHO suosittelee seerumin pooling-menetelmän käyttöä HIV-infektiossa, kun taudin esiintyvyys on alle 2 %, ja enintään viiden seerumin pooling-menetelmää (25). Näiden ohjeiden mukaisesti useimmat tutkimukset soveltavat ja suosittelevat pooling-menetelmien käyttöä alueilla, joilla seroprevalenssi on alhainen. Tutkimuksessamme osoitamme, että seerumien yhdistäminen voi olla kustannustehokasta myös väestöissä, joissa HBsAg-kantajien esiintyvyys on suuri. Tämä voisi mahdollistaa sen käytön maissa, jotka kuuluvat HBV-infektion keskisuuren ja suuren endeemisyyden alueisiin, mikä yleensä vastaa alikehittyneitä tai kehitysmaita eli maita, joissa on suurempi tarve vähentää laboratoriokokeiden taloudellisia kustannuksia. On kuitenkin tarpeen tehdä vastaavia tutkimuksia näillä alueilla, jotta tuloksemme voidaan vahvistaa. On kuitenkin jo osoitettu, että esimerkiksi Keniassa, jossa HIV-infektioiden esiintymistiheys on korkea (7,3 %), pooling-menetelmällä voitaisiin saavuttaa 62 prosentin taloudelliset säästöt ilman merkittävää turvallisuuden heikkenemistä (14). Espanjassa, joka kuuluu HBV-infektion vähäisen endeemisyyden alueeseen ja jossa HBsAg:n kantajien osuus väestöstä on 1,2 prosenttia (4), sitä voidaan käyttää kaikissa niissä ryhmissä, joissa HBsAg:n seulonta on nykyisin pakollista (kuten verenluovuttajilla, autotransfuusio-ohjelmiin osallistuvilla henkilöillä ja raskaana olevilla naisilla tehtävä seulonta).
HBV:n kroonisten kantajien havaitsemisessa käytettävien tekniikoiden kustannus-hyötyanalyysin avulla voidaan osoittaa, että taloudelliset säästöt ovat suuremmat, kun ne tehdään suuressa määrässä määrityksiä ryhmissä, joiden seroprevalenssi on alhainen, ja sen käyttö voisi olla kustannustehokasta myös alueilla, joilla infektioiden esiintyvyys on suuri, ja jopa laboratorioissa, jotka suorittavat pienen määrän määrityksiä. Olemme osoittaneet taloudelliset kustannussäästöt sekä HBsAg:n eri esiintyvyyden että vuosittain tehtävien testien määrän mukaan. Meidän alueellamme pooling-menetelmän soveltaminen voisi säästää noin 74 prosenttia taloudellisista kokonaiskustannuksista verrattuna yksittäiseen menetelmään.
Jotkut tutkijat ovat viime aikoina alkaneet harjoitella strategioita virusnukleiinihappojen osoittamiseksi verenluovuttajista polymeraasiketjureaktiota (PCR) käyttäen verensiirtoihin liittyvän turvallisuuden lisäämiseksi (26-29). Koska yksittäisiä seulontatutkimuksia ei ole mahdollista tehdä taloudellisten ongelmien ja työmäärän vuoksi, käytetään nykyään serologisesti negatiivisten verinäytteiden yhdistämismenetelmää. Tämä menettely saattaa lisätä veren turvallisuutta, kun verenluovutukset seulotaan järjestelmällisesti ja suhteellisen pienin kustannuksin. Koska yksi tärkeimmistä rajoituksista näiden menetelmien soveltamisessa on taloudelliset syyt, uskomme, että tutkimuksemme avulla voitaisiin luoda teoreettinen perusta HBV-, HCV- ja HIV-infektioiden seulonnan käytölle kahdessa vaiheessa suhteellisen alhaisin taloudellisin kustannuksin. Ensimmäisessä vaiheessa kaupallista EIA:ta voitaisiin soveltaa luovuttajien seerumiin; toisessa vaiheessa PCR-tekniikoiden soveltaminen seronegatiivisten näytteiden joukkoon voisi lisätä analyysin turvallisuutta. Ennen kuin tulevissa tutkimuksissa voidaan osoittaa tämän tekniikan arvo verenluovuttajilla, uskomme, että sitä voitaisiin soveltaa vain diagnostisiin ja epidemiologisiin testeihin.
Päätelmämme on, että EIA:n soveltaminen yhdistettyihin seerumeihin on herkkä ja spesifinen menetelmä kahden tärkeimmän HBsAg:n alatyypin havaitsemisessa alueella, jolla seroprevalenssi on alhainen. Herkkyys heikkenee vain silloin, kun yhdistetyissä seerumeissa on hyvin korkeita anti-HBs-tittereitä. Yhdistämistekniikka on menetelmä, joka voi mahdollistaa myös taloudellisia säästöjä, jos sitä käytetään tutkittaessa väestöjä, joissa HBsAg-kantajien esiintyvyys on suuri. Mielestämme lisätutkimukset ovat tarpeen näiden havaintojen vahvistamiseksi.
Kiitokset
Haluamme kiittää David H. Wallacea (European Association of Science Editorsin ja Council of Biological Editorsin jäsen) käsikirjoituksen englanninkielisestä käännöksestä.
1. Maynard JE. Hepatiitti B: maailmanlaajuinen merkitys ja valvonnan tarve. Vaccine 1990; 8 (Supl.): 18s-20s.
2. Margolis HS, Alter MJ, Hadler SC. Hepatiitti B: kehittyvä epidemiologia ja vaikutukset torjuntaan. Sem Liver Dis 1991; 11: 84-92.
3. Alter MJ, Mast EE. Virushepatiittien epidemiologia Yhdysvalloissa. Gastroenterol Clin North Am 1994; 23: 437-55.
4. Suárez A, Riestra S, Navascués CA, et al. Positiiviset HBsAg-positiiviset verenluovuttajat Asturiassa (Espanja): nykyinen esiintyvyys ja sen merkitys. (Englanninkielinen tiivistelmä). Med Clin (Barcelona) 1994; 102: 329-32.
5. Emmanuel JC, Basset MT, Smith HJ, Jacobs JA. Seerumien yhdistäminen ihmisen immuunikatoviruksen (HIV) testausta varten: taloudellinen menetelmä käytettäväksi kehitysmaissa. J Clin Pathol 1988; 41: 582-5.
6. Kline RL, Brothers TA, Brookmeyer R, et al. Evaluation of human immunodeficiency virus seroprevalence in population surveys using pooled sera. J Clin Microbiol 1989; 27: 1449-52.
7. Cahoon-Young B, Chandler A, Livermore T, et al. Sensitivity and specificity of pooled versus individual sera in a human immunodeficiency virus antibody prevalence study. J Clin Microbiol 1989; 27: 1893-5.
8. Frosner GG, Dobler G, von Sonnenburg FJ. HIV-vasta-aineiden linkittämättömän testauksen kustannusten vähentäminen tutkimalla yhdistettyjä seerumeita. AIDS 1990; 4: 73-5.
9. Behets F, Bertozzi S, Kasali M, et al. Sucessful use of pooled sera to determine HIV-1 seroprevalence in Zaire with development of cost-efficiency models. AIDS 1990; 4: 737-41.
10. Monzon OT, Paladin FJ, Dimaandal E, et al. Vasta-ainepitoisuuden ja testimuodon merkitys yhdistettyjen seerumien HIV-testauksessa. AIDS 1992; 6: 43-8.
11. Tamashiro H, Maskill W, Emmanuel J, et al. HIV-vasta-ainetestauksen kustannusten vähentäminen. Lancet 1993; 342: 87-90.
12. Perriens JH, Magazani K, Kapila N, et al. Pikatestin ja ELISA-testin käyttö HIV-vasta-aineiden seulontaan yhdistetyistä seeruminäytteistä Lubumbashissa, Zairessa. J Virol Methods 1993; 41: 213-21.
13. McMahon EJ, Fang C, Layug L, Sandler SG. Verenluovuttajanäytteiden yhdistäminen HIV-1-vasta-ainetestauksen kustannusten vähentämiseksi. Vox Sang 1995; 68: 215-9.
14. Verstraeten T, Farah B, Duchateau L, Matu R. Pooling sera to reduce the cost of HIV surveillance: a feasibility study in a rural Kenyan district. Trop Med Int Health 1998; 3: 747-50.
15. Kamel MA, Ghaffar YA, Wasef MA, et al. High HCV prevalence in Egyptian blood donors. Lancet 1992; 340: 427.
16. Neil AGS, Conradie JD. Verenluovuttajien edullinen HCV-vastainen seulonta. Lancet 1992; 340: 1096.
17. Fernández E, Riestra S, García S, Rodríguez S. Poolitestit hepatiitti C -virusinfektion toteamiseksi. J Hepatol 1995; 23: 236.
18. García Z, Taylor L, Ruano A, et al. Evaluation of a pooling method for routine anti-HCV screening of blood donors to lower the cost burden on blood banks in countries under development. J Med Virol 1996; 49: 218-22.
19. Liu P, Shi ZX, Zhang YC, et al. A prospective study of a serum-pooling strategy in screening blood donors for antibody to hepatitis C virus. Transfusion 1997; 37: 732-6.
20. Cunningham R, Northwood JL, Kelly CD, et al. Rutiininomainen synnytystä edeltävä seulonta hepatiitti B:n varalta käyttäen yhdistettyjä seerumeita: validointi ja katsaus 10 vuoden kokemukseen. J Clin Pathol 1998; 51: 392-5.
21. Rabenau H, Schutz R, Berger A, et al. How accurate is serologic testing of plasma pools for hepatitis B virus surface antigen, anti-human immunodeficiency virus 1 and 2, and anti-hepatitis C virus? (englanninkielinen tiivistelmä). Infus Transfus 1996; 23: 124-30.
22. Echevarría JE, León P, López JA, et al. HBsAg-alatyypin jakautuminen eri HBsAg-kantajapopulaatioissa Espanjassa. Eur J Epidemiol 1995; 11: 39-45.
23. Neill AGS, Conradie JD. Hepatiitti C -viruksen allastestit. Lancet 1994; 343: 738.
24. Liu P, Shi ZX, Zhang YC, Zhang XY. Vertaileva tutkimus neljästä EIA-pakkauksesta hepatiitti C -viruksen vasta-aineiden seulontaan yhdistetyissä seerumeissa. Biomed Environ Sci 1998; 11: 75-80.
25. Suositukset HIV-vasta-aineen testaamiseksi seerumipoolissa. WHO Weekly Epidemiol Rec 1991; 44: 316-27.
26. Lefrere JJ, Coste J, Defer C, et al. Screening blood donations for virus genomes: multicenter study of real-time simulation using pooled samples on the model of hepatitis C virus RNA detection. Transfusion 1998; 38: 915-23.
27. Yerly S, Pedrocchi M, Perrin L. Polymeraasiketjureaktion käyttö plasmapooleissa C-hepatiittiviruksen ja HIV-tyypin 1 RNA:n samanaikaiseen osoittamiseen. Transfusion 1998; 38: 908-14.
28. Schottstedt V, Tuma W, Bunger G, Lefevre H. PCR HBV:n, HCV:n ja HIV-1:n toteamiseksi kokemuksia ja ensimmäisiä tuloksia rutiiniseulontaohjelmasta suuressa verensiirtopalvelussa. Biologicals 1998; 26: 101-4.
29. Morandi PA, Schockmel GA, Yerly S, et al. Ihmisen immuunikatoviruksen tyypin 1 (HIV-1) RNA:n osoittaminen HIV-1- ja HIV-2-vasta-aineiden suhteen negatiivisten seerumien poolista. J Clin Microbiol 1998; 36: 1534-8.
Vastaa