Karbonaatti-ionin Lewis-rakenne piirretään tässä ohjeessa vaihe vaiheelta. CO32-:n Lewis-rakenteen piirtämisessä käytetään kokonaisvalenssielektronien käsitettä. Kun CO32-:n Lewis-rakenne on saatu valmiiksi, pitäisi olla -2-varaus ja stabiilisuus. Näistä asioista opit tässä opetusohjelmassa.
- Karbonaatti-ioni | CO32-
- CO32- Lewis-rakenne
- CO32- Lewis-rakenteen piirtämisen vaiheet
- CO32-:n valanssikuorien elektronien kokonaislukumäärä
- Valenssielektronipareja yhteensä
- CO32-ionin keskusatomi
- Yksittäiset atomiparit
- Atomien varaukset
- Tarkista stabiilisuus ja minimoi atomien varaukset muuttamalla yksinäiset ioniparit sidoksiksi
- CO32- (karbonaatti)ionin Lewis-rakenne
- karbonaatin Lewis-rakenne ja bikarbonaatin Lewis-rakenne
Karbonaatti-ioni | CO32-
Karbonaatti-ionilla on -2 varaus. Metallikarbonaattiyhdisteet ovat yleisiä maailmassa. Esimerkkinä voidaan antaa CaCO3.
CO32- Lewis-rakenne
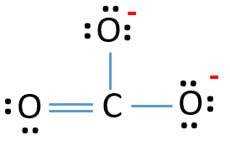
CO32-ionin Lewis-rakenteessa on kolme σ-sidosta ja π-sidos hiiliatomin ympärillä.
CO32- Lewis-rakenteen piirtämisen vaiheet
CO32- Lewis-rakenteen piirtämiseen tarvitaan seuraavat vaiheet, ja ne selitetään yksityiskohtaisesti tässä ohjeessa.
- Hiili- ja happiatomien valanssikuorien elektronien kokonaislukumäärän selvittäminen
- Elektroniparien kokonaismäärä
- Keskiatomin valinta
- Asetetaan yksinäiset parit atomeihin
- Tarkistetaan atomien stabiilisuus ja minimoidaan atomien varaukset muuttamalla yksinäiset parit sidoksiksi.
Oikean Lewis-rakenteen piirtäminen on tärkeää, jotta voit piirtää CO32-:n resonanssirakenteet oikein.
CO32-:n valanssikuorien elektronien kokonaislukumäärä
Hiili sijaitsee jaksollisen järjestelmän ryhmässä 4. Hiilellä on siis neljä elektronia valenssikuoressaan.Happi sijaitsee 6. ryhmässä. Sillä on kuusi elektronia valenssikuoressa.
- Hiiliatomin antamien valenssielektronien kokonaismäärä = 4
CO32- ionissa on kolme happiatomia, Näin ollen
- Happiatomien antamien valenssielektronien kokonaismäärä = 6 *3 = 18
CO32- ionissa on -2 varaus. Näin ollen valenssielektroneja on kaksi elektronia enemmän.
- Valenssielektronien kokonaismäärä = 4 + 18 + 2 = 24
Valenssielektronipareja yhteensä
Valenssielektronipareja yhteensä = σ-sidokset + π-sidokset + valenssikuorissa olevat yksinäiset parit
Valenssielektronipareja yhteensä määräytyy jakamalla valenssielektronien kokonaismäärä kahdella. CO32-ionin tapauksessa elektronipareja on yhteensä 12.
CO32-ionin keskusatomi
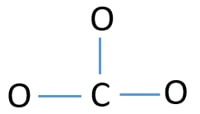
Keskusatomina toimimiseksi on tärkeää, että sillä on suurempi valanssi. Hiilellä on paremmat mahdollisuudet olla keskusatomi (Katso kuva), koska hiilen valenssi voi olla 4. Hapen korkein valenssi on 2. Nyt voimme siis rakentaa luonnoksen CO32- ionista.
Yksittäiset atomiparit
- Ylläolevassa luonnoksessa on valmiiksi jo kolme C-O sidosta. Näin ollen jäljellä on enää yhdeksän (12-3 = 9) valenssielektroniparia.
- Merkitään ensin nuo yhdeksän valenssielektroniparia yksinäisiksi pareiksi ulkopuolisten atomien (happiatomien) päälle. Yksi happiatomi ottaa kolme yksinäistä elektroniparia kahdeksikkosäännön mukaisesti (happiatomi ei voi pitää valenssikuoressaan enempää kuin kahdeksan elektronia).
- Kolmen happiatomin kohdalla käytetään yhdeksän elektroniparia. Nyt ei ole enää yksinäisiä pareja, joita merkitä hiiliatomeihin happiatomien merkitsemisen jälkeen (atomien ulkopuolella).
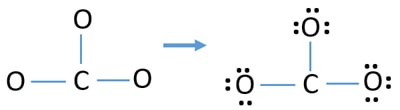
Atomien varaukset
Atomien elektroniparien merkitsemisen jälkeen, meidän pitäisi merkitä kunkin atomin varaukset. Varausten merkitseminen on merkittävää, koska sen avulla määritetään ionin paras Lewis-rakenne. Kun olet merkinnyt varaukset, huomaat, että jokainen happiatomi saa -1 varauksen ja hiiliatomi saa +1 varauksen.
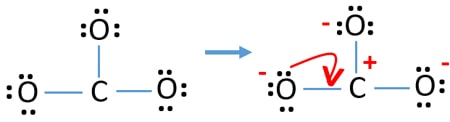
Tarkista stabiilisuus ja minimoi atomien varaukset muuttamalla yksinäiset ioniparit sidoksiksi
- Happea sisältävien atomien pitäisi pitää negatiivisia varauksia, koska hapen elektronegatiivisuus on korkeampi kuin hiiliatomin. Muuten voidaan sanoa, että happiatomien kyky pitää negatiivisia varauksia on suurempi kuin hiiliatomien.
- Piirretty rakenne ei ole stabiili, koska kaikilla atomeilla on varaus (Lewisin rakenteen pitäisi olla stabiili, jossa on vähemmän varauksia).
- Nyt meidän pitäisi yrittää minimoida varaukset muuntamalla yksinäinen pari tai parit sidoksiksi. Muunnetaan siis yhden happiatomin yksi yksinäinen pari C-O-sidokseksi.
- Nyt hiiliatomin ja yhden happiatomin välillä on kaksoissidos (yksi C=O-sidos). Nyt hiiliatomin ja kahden muun happiatomin välillä on kaksi yksinkertaista sidosta (kaksi C-O-sidosta).
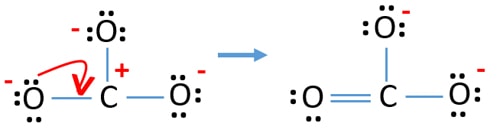
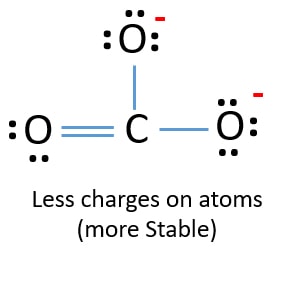
Uudessa rakenteessa atomien varaukset ovat pienemmät kuin edellisessä rakenteessa. Nyt yhdellä happiatomilla ja hiiliatomilla ei ole varauksia. Myös vain kahdella happiatomilla on -1 negatiivinen varaus. Nyt ymmärrät, että tämä CO32- rakenne on vakaampi kuin edellinen rakenne. Tällä rakenteella on siis paremmat mahdollisuudet olla CO32-ionin Lewis-rakenne.
CO32- (karbonaatti)ionin Lewis-rakenne
Kysymyksiä
Kysy kemian kysymyksesi ja löydä vastaukset
karbonaatin Lewis-rakenne ja bikarbonaatin Lewis-rakenne
Karbonaatti-ionissa on kaksi happiatomia, joilla kummallakin on -1 varaus. Toinen näistä happiatomeista ottaa protonin (H+-ioni) ja muodostaa -OH-ryhmän.
Seuraavat opetusohjelmat
Vastaa