- Introducción
- Producción de GMS
- Impurezas encontradas en el glutamato monosódico
- D-Glutamato
- El ácido piroglutámico
- Mono y dicloro propanoles
- MSG en cubos de condimento
- Síndrome del restaurante chino
- Metabolismo del glutamato dietético
- Efectos del glutamato
- Sistema nervioso central (SNC)
- Obesidad
- Sistema reproductor
- Hepatotoxicidad
- Nefrotoxicidad
- Prevención de los efectos tóxicos del GMS
- La ingesta frecuente de vitamina C
- La vitamina E
- El ajo
- Curcuma longa (cúrcuma)
- Jengibre
- Las alubias de la India
- Conclusión
- Conflicto de intereses
- Agradecimientos
Introducción
El glutamato monosódico (GMS) es una sal sódica del ácido glutámico. El agua lo ioniza en iones libres de sodio y ácido glutámico, que es un compuesto orgánico formado por cinco átomos de carbono. Tiene un grupo carboxílico (-COOH) y un grupo amino (-NH2) unidos a un átomo de carbono «alfa» (un átomo de carbono unido directamente al grupo -COOH) (David, 2008). Es un alfaaminoácido. La fórmula molecular del GMS es C3H8NNaO4 y su masa molecular es de 169,11 gmol-1. El GMS tiene la misma estructura básica de los aminoácidos, con un grupo amina (-NH2) y un ion carboxilato en lugar del grupo carboxílico (-COO-). El GMS tiene una estructura casi idéntica a la del glutamato. La diferencia es que un átomo de hidrógeno de la cadena carboxílica ha sido sustituido por un átomo de sodio, de ahí el nombre de glutamato monosódico (Figura 1&2).
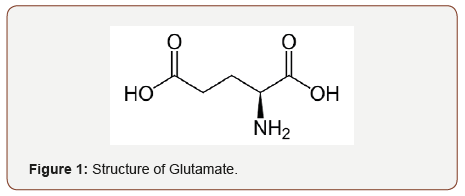
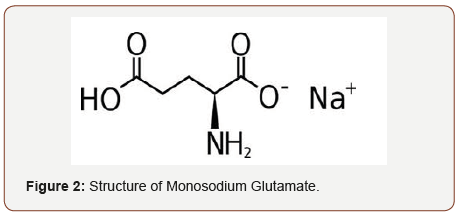
El glutamato monosódico tiene un sabor característico que queda fuera de la región de los cuatro sabores clásicos: dulce, ácido, salado y amargo. Debido a este sabor especial, muchos productores de alimentos utilizan el glutamato para mejorar el sabor de sus productos. Recientemente, Chaudhari et al. identificaron un receptor gustativo específico del glutamato en la lengua. Los científicos japoneses encontraron tres sustancias umami (glutamato, 5-inosinato y 5-guanilato), pero el umami no ha sido reconocido en Europa y América durante mucho tiempo. A finales del siglo XX, el umami fue reconocido internacionalmente como el quinto sabor básico sobre la base de estudios psicofísicos, electrofisiológicos y bioquímicos. Existe un sinergismo entre el glutamato y los 5-nucleótidos. Entre los receptores mencionados, sólo el receptor T1R1+T1R3 muestra el sinergismo. Dado que el glutamato y el 5-inosinato están contenidos en varios alimentos, el sabor umami es inducido por el sinergismo en la alimentación diaria.
La seguridad y la toxicidad del glutamato monosódico se han vuelto controvertidas en los últimos años debido a los informes de reacciones adversas en personas que han consumido alimentos que contienen glutamato monosódico. Muchos estudios han confirmado las reacciones adversas del GMS. Se ha informado de que el GMS causa dolor de cabeza, vómitos, diarrea, síndrome del intestino irritable, ataques de asma en pacientes asmáticos y ataques de pánico. Obuchi et al. estudiaron el efecto de los extractos de ajo en el fibroma inducido por el GMS en ratas wistar e informaron de que el GMS por sí solo aumentaba las proteínas totales, el colesterol y el estradiol (estrógeno), lo que a su vez inducía el fibroma en las ratas. Sin embargo, el tratamiento con extractos de ajo abrogó/mitigó casi por completo cualquier efecto inducido por el GMS.
Egbuonu et al. informaron de un estudio destinado a investigar el potencial de la administración de bajas concentraciones de glutamato monosódico para inducir hepatotoxicidad en ratas albinas macho. En ese estudio, se observó que el tratamiento de ratas con glutamato monosódico a una baja concentración (5mg/kg de peso corporal) podía ser hepatotóxico sin colestasis significativa ni patologías del hueso. Onyema et al. informaron de que el glutamato monosódico a una dosis de 0,6mg/peso corporal inducía el estrés oxidativo y la hepatotoxicidad en ratas y la vitamina E mejoraba el estrés oxidativo y la hepatotoxicidad inducidos por el glutamato. Meraiyebu et al. informaron de que el GMS aumentó el número de plaquetas, el tiempo de sangrado y el tiempo de coagulación en ratas tratadas con GMS. Onyema et al. probaron la hipótesis de que la alteración del metabolismo de la glucosa tras la administración de GMS podría contribuir a los cambios en los marcadores de estrés oxidativo observados en los animales. El patrón de inducción del estrés oxidativo y la alteración de las enzimas del metabolismo de la glucosa en los animales fue una indicación de que el estrés oxidativo inducido por el GMS en los tejidos renales de las ratas podría ser contribuido por el aumento de la concentración de glucosa en los tejidos como resultado de una mayor gluconeogénesis renal. Nwajei et al. informaron de que cuatro condimentos alimentarios seleccionados (etiquetados como IS, KC, SMC y BS) que se consumen habitualmente en Nigeria perturbaron negativamente algunas hormonas sexuales: testosterona, estrógeno y progesterona de ratas albinas wistar debido a la presencia de GMS en estos condimentos. Kolawole investigó el efecto del GMS administrado por vía oral sobre el consumo de alimentos, el peso corporal y algunos parámetros bioquímicos y hematológicos en ratas wistar adultas e informó de que el GMS en dosis de 5-15mg/kg de peso corporal no era peligroso para la salud.
Producción de GMS
Los chinos han utilizado ciertas algas marinas para mejorar el sabor de los alimentos durante unos 2000 años. En 1908, el agente potenciador del sabor fue identificado como ácido glutámico. Poco después, se desarrollaron métodos para extraer el ácido glutámico de las algas marinas. El glutamato se fabrica mediante un proceso de hidrólisis de proteínas, en el que el ácido glutámico se libera de las proteínas a través de la fermentación enzimática o el uso de productos químicos. El glutamato también se fabrica mediante un proceso de fermentación en el que las bacterias se cultivan aeróbicamente en un medio nutritivo líquido. Las bacterias liberan ácido glutámico como subproducto del metabolismo en el medio nutritivo líquido en el que se cultivan. El ácido glutámico se separa del caldo de fermentación por filtración, concentración, acidificación y cristalización y se convierte en su sal sódica.
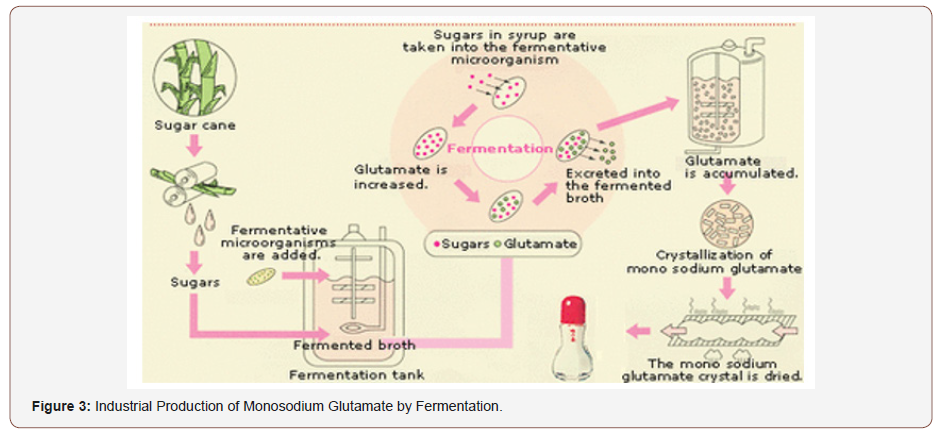
El nombre «glutamato monosódico» se refiere a una combinación de ácido glutámico y sodio con un 99% de pureza. Cada año se producen en el mundo unos 1,9 millones de toneladas de glutamato monosódico mediante la fermentación de Corynebacterium glutamicum o especies afines. Estas bacterias son auxótrofas de biotina y la biotina (vitamina B7) se utiliza como cofactor. Los productores prefieren utilizar azúcares para producir GMS. Algunas fuentes de azúcar utilizadas son, entre otras, la caña de azúcar, los hidrolizados de almidón obtenidos de los tubérculos de maíz o de yuca. El amoníaco y las sales de amonio se añaden como fuente de nitrógeno. Las vitaminas y otros nutrientes se añaden para finalizar el proceso. La acumulación de glutamato en el medio sólo se produce en condiciones de limitación de biotina. Los requisitos de limitación de biotina impidieron el uso de materias primas estándar, como la melaza de azúcar, porque contenían biotina. La adición de penicilina, o el uso de microorganismos auxotróficos para el glicerol o el oleato, permite a las bacterias producir grandes cantidades de glutamato sin limitación de biotina (Figura 3).
Impurezas encontradas en el glutamato monosódico
El glutamato monosódico contiene ácido D-glutámico, piroglutámico y varios otros contaminantes además del ácido L-glutámico.
D-Glutamato
Todos los aminoácidos (excepto la glicina) pueden presentarse en dos formas isoméricas, debido a la posibilidad de formar dosenantiómeros diferentes alrededor del átomo de carbono central. Por convención, se denominan formas L- y D-, análogas a las configuraciones izquierda y derecha. Sólo los L-aminoácidos se fabrican en las células y se incorporan a las proteínas. Algunos aminoácidos D se encuentran en las paredes celulares de las bacterias, pero no en las proteínas bacterianas. El glutamato tiene los enantiómeros D y L y sólo el enantiómero L-glutamato tiene propiedades para mejorar el sabor. El glutamato monosódico manufacturado contiene más del 99,6% de la forma natural predominante de L-glutamato, que es una proporción mayor de los glutamatos libres de los alimentos naturales fermentados. Los productos fermentados, como la salsa de soja, la salsa para bistec y la salsa Worcestershire, tienen niveles de glutamato similares a los de los alimentos con glutamato monosódico añadido, pero el 5% o más del glutamato puede ser el enantiómero D. Los alimentos no fermentados tienen niveles relativos más bajos de D-glutamato que los productos fermentados (Figura 4).
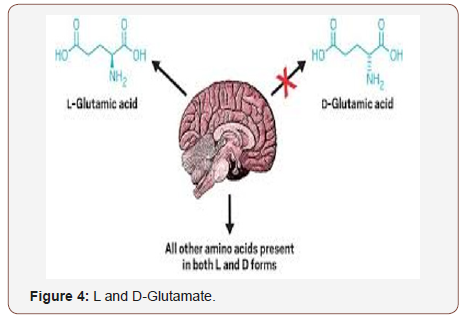
A diferencia de otros D-aminoácidos, el D-glutamato no es oxidado por las oxidasas de los D-aminoácidos; por lo tanto, la vía de desintoxicación no está disponible para manejar el D-glutamato. Asimismo, el D-glutamato, cuando se ingiere, escapa en gran medida a la mayoría de las reacciones de desaminación (a diferencia de su homólogo L). El D-glutamato libre se encuentra en los tejidos de los mamíferos en niveles sorprendentemente altos, representando el D-glutamato el 9% del glutamato total presente en el hígado. El D-glutamato es el inhibidor natural más potente de la síntesis de glutatión identificado hasta la fecha y esto puede explicar su localización en el hígado, ya que el D-glutamato circulante puede alterar la estabilidad redox.
El ácido piroglutámico
El ácido piroglutámico (PCA) también se conoce como 5-oxoprolina, pidolicacid o piroglutamato. Es un derivado natural de los aminoácidos, común pero raramente estudiado, en el que el grupo amino libre del ácido glutámico o de la glutamina se cicla para formar un lactem. Es un metabolito del ciclo del glutatión que se convierte en glutamato mediante la 5-oxoprolinasa. El piroglutamato se encuentra en muchas proteínas, incluida la bacteriodopsina. El ácido glutámico N-terminal y el residuo de glutamina pueden ciclar espontáneamente para convertirse en piroglutamato o ser convertidos enzimáticamente por las glutaminil ciclasas. El piroglutamato es un compuesto aheterocíclico y está presente en el plasma de varias especies, incluida la humana. Sin embargo, las inyecciones cerebrales locales de concentraciones muy elevadas de piroglutamato indujeron lesiones neurotóxicas que parecían ser como las producidas por el ácido cianico (Figura 5).
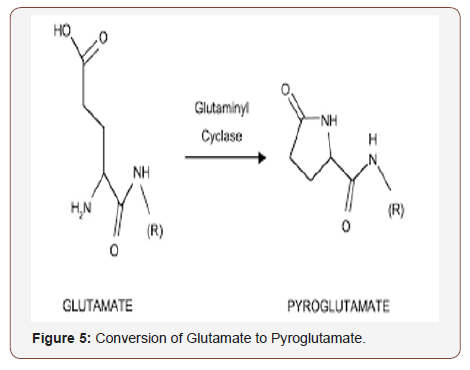
También se ha descubierto que el ácido piroglutámico es producido por el glutamato en presencia de las enzimas γ-GCS, glutamina sintetasa y glutamato-5-quinasa. El glutamato fosforilado unido a la enzima es el intermediario en las tres reacciones enzimáticas. El glutamato activado se transfiere a una molécula aceptora, a saber, cisteína, amoníaco y NADPH, respectivamente. El glutamato fosforilado o activado es muy inestable y propenso a la ciclización espontánea en ácido piroglutámico. Si la molécula aceptora no está presente o no está disponible, la ciclización espontánea del glutamato activado conduce a la generación de ácido piroglutámico. El γ-GCS, que cataliza el primer paso de la glutatión-biosíntesis, activa el glutamato que puede convertirse en ácido piroglutámico en ausencia de cisteína. Del mismo modo, en los metanótrofos, se ha propuesto que en condiciones de estrés y de limitación de nitrógeno se genera ácido piroglutámico a partir de glutamatovia glutamina sintetasa, como se ha encontrado en condiciones in vitro.
Mono y dicloro propanoles
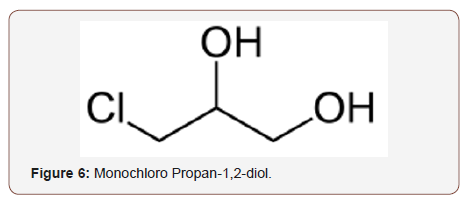
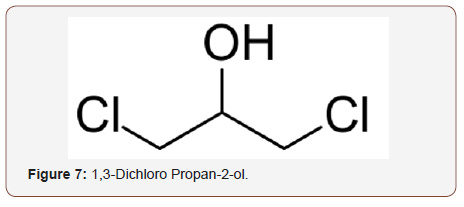
El 3-monocloropropano-1,2-diol (3-MCPD) es un compuesto orgánico-químico que es el miembro más común de los contaminantes químicos de los alimentos conocidos como cloropropanoles. Se sospecha que es cancerígeno para los seres humanos. Se crea principalmente en los alimentos durante la hidrólisis de las proteínas cuando se añade ácido clorhídrico a alta temperatura para acelerar la descomposición de las proteínas en aminoácidos. Como subproducto de este proceso, el cloruro puede reaccionar con la columna vertebral de glicerol de los lípidos para producir 3-MCPD. En el año 2000, el Grupo de Seguridad y Normas Alimentarias del Ministerio de Agricultura, Pesca y Alimentación/Departamento de Sanidad (JFSSG) llevó a cabo un estudio sobre las salsas de soja y productos similares disponibles en el Reino Unido, e informó de que más de la mitad de las muestras recogidas en los puntos de venta contenían diversos niveles de 3-MCPD. En 2001, la Agencia de Normas Alimentarias del Reino Unido (FSA) descubrió en pruebas de varias salsas de ostras y de soja que el 22% de las muestras contenían 3-MCPD a niveles considerablemente superiores a los considerados seguros por la Unión Europea. Alrededor de dos tercios de estas muestras también contenían un segundo cloropropanol llamado 1,3-dicloropropano-2-ol (1,3-DCP) que, según los expertos, no debería estar presente en ningún nivel en los alimentos. Ambas sustancias químicas son potencialmente cancerígenas y la Agencia recomendó que los productos afectados se retiraran de los estantes y se evitaran (Figura 6&7).
MSG en cubos de condimento
Los condimentos alimentarios son sustancias que añaden sabor a los alimentos, por ejemplo, sal, pimientos y otras especias. Las especias son sustancias vegetales de origen autóctono o exótico, aromáticas y de sabor picante, que se utilizan para realzar el sabor de los alimentos o para añadirles el ingrediente estimulante que contienen. Los condimentos también pueden utilizarse para sustituir a la sal común en una gran variedad de alimentos preparados industrialmente, así como en la preparación de alimentos, tanto en restaurantes como en catering, cocina doméstica, etc. Estos condimentos son especialmente adecuados para sopas, carnes y otros alimentos en los que se utilizan condimentos salados y/o especiados. La mezcla de ingredientes y los condimentos, cuando se añaden a varios alimentos, cambian la composición de los mismos.
Hay varias marcas de condimentos para alimentos fácilmente disponibles en los mercados abiertos, en las tiendas de la calle y en los supermercados. Entre ellas se encuentran: Star maggi, knorr, royco, doyin, jumbo (cubos), Onga, Mixpy,Benny, Aluba shrimp seasoning (en polvo), A-one, Vedan, Ajino-moto, Salsa y Tasty (glutamato monosódico). Los informes indican que los principales ingredientes activos de los potenciadores del sabor son la sal (NaCl) y el glutamato monosódico (MSG). Otros ingredientes son: Aceite de palma hidrogenado, caramelo, colorante, granos de soja, algarrobas, maltodextrina, almidón de maíz, grasa de pollo, guanilato disódico, inosilato disódico, proteína vegetal hidrolizada, tomates, especias naturales, etc.
Síndrome del restaurante chino
El «síndrome del restaurante chino» (CRS) se describió por primera vez hace más de 40 años. La descripción original de los síntomas, que aparecían unos 20 minutos después de la comida, incluía adormecimiento o ardor en la nuca, que se irradiaba a ambos brazos y, a veces, al tórax anterior, lo que se asociaba a una sensación de debilidad general y palpitaciones. Posteriormente se describieron los síntomas de rubor, mareo, síncope y presión facial. Los niños pueden reaccionar con fiebre, convulsiones o una ansiedad constante.Se creía ampliamente que el glutamato monosódico estaba asociado al SRC. Sin embargo, las revisiones de los estudios pertinentes han propuesto que los estudios que asociaron el glutamato monosódico con el SRC no tenían un diseño experimental adecuado, los resultados eran inconsistentes y la frecuencia de las respuestas a la ingesta de glutamato monosódico no era lo suficientemente alta como para demostrar que el glutamato monosódico es el desencadenante del SRC. Se dice que el SRC se produce en personas sensibles al GMS.
Esta cuestión sigue siendo controvertida. Dado que el GMS es idéntico al glutamato que contienen naturalmente muchos alimentos, el cuerpo lo absorbe y metaboliza de la misma manera. Por otra parte, se han asociado efectos perjudiciales a la ingesta de GMS, como los relacionados con las enfermedades de Alzheimer y Parkinson. Esto fue descartado por una conferencia de consenso liderada por el profesor Dr. Konrad Beyreuther, ganador del Premio Nobel, porque el glutamato ingerido a través de los alimentos no puede cruzar la barrera hematoencefálica en personas sanas.
Metabolismo del glutamato dietético
El glutamato es el principal constituyente de las proteínas dietéticas y también se consume en muchos alimentos como aditivo en forma de glutamato monosódico. Los estudios realizados en humanos y animales sugieren que el glutamato es un importante combustible oxidativo para el intestino y que el glutamato de la dieta se moviliza ampliamente en el primer paso por el intestino. El glutamato es también un importante precursor de moléculas bioactivas, como el glutatión, y funciona como un neurotransmisor clave. Varios estudios han demostrado que el glutamato se metaboliza ampliamente en el intestino. El glutamato es el principal neurotransmisor excitatorio del cuerpo y se han encontrado múltiples receptores y transportadores de glutamato en el tracto gastrointestinal y el sistema nervioso entérico. Estudios recientes también han demostrado que dos transportadores vesiculares de glutamato (VGLUTs), VGLUTs1 y VGLUTs2, están presentes en el tejido nervioso entérico y pancreático. Se ha puesto de manifiesto que el intestino, especialmente el intestino, es también un lugar importante de catabolismo de varios aminoácidos, principalmente aminoácidos no esenciales como la glutamina, el glutamato y el aspartato.
Sin embargo, hay que hacer una distinción importante: aunque los aminoácidos se catabolizan tanto en el hígado como en los tejidos intestinales, el grado en que se oxidan completamente a dióxido de carbono varía. El glutamato es un aminoácido clave que vincula el catabolismo hepático de aminoácidos y la gluconeogénesis, ya que muchos aminoácidos se catabolizan primero a glutamato por transaminación. Se supone que el metabolismo intestinal del glutamato se produce en gran medida en las células epiteliales que recubren la mucosa, los enterocitos (Figura 8).
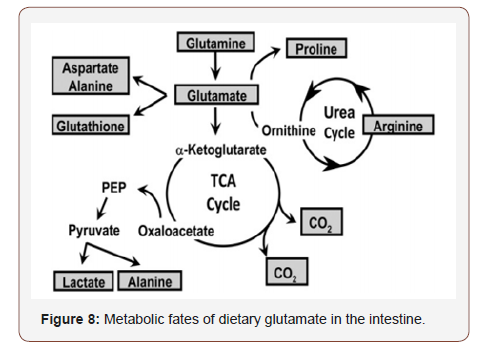
El glutamato es un importante enlace metabólico entre el ciclo del ácido tricarboxílico (TCA) y el ciclo de la urea que interviene en la generación de energía celular y la eliminación de nitrógeno (Figura 9). El GLU y el AKG de la dieta son transportados desde el lumen del intestino hasta el enterocito por los transportadores de aminoácidos excitatorios-1 (EAAC-1) y de Na-dicarboxilato-1 (NaDC-1), respectivamente. Dentro del enterocito, tanto el GLU como el AKG pueden sufrir una transaminación y ser transportados a las mitocondrias para su metabolismo oxidativo en CO2.
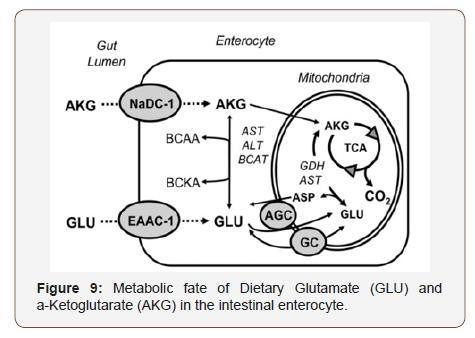
Una preocupación de larga data sobre el consumo de glutamato en la dieta, en particular el glutamato monosódico (GMS), es la evidencia y el riesgo potencial de neurotoxicidad. Algunos han planteado serias preocupaciones sobre el riesgo potencial del GMS dietético, el glutamato parenteral, y sus implicaciones para las enfermedades humanas, como la obesidad. Sin embargo, es muy importante reconocer que las pruebas de neurotoxicidad en varios modelos experimentales sólo se produjeron con cargas extremadamente altas de glutamato enteral y parenteral.
El glutamato, al igual que otros aminoácidos constituyentes ingeridos en las proteínas alimentarias, se absorbe y metaboliza normalmente en el intestino delgado tras la digestión proteolítica. Sin embargo, algunos aminoácidos, especialmente el glutamato dietético, se ingieren en forma libre y, por tanto, pueden metabolizarse de forma diferente cuando se presentan en la mucosa epitelial del estómago.
Efectos del glutamato
Los receptores de glutamato son receptores sinápticos que se localizan en las membranas de las células neuronales. Su prevalencia en el sistema nervioso central se ha relacionado con muchas enfermedades neurodegenerativas, y otras afecciones se han vinculado a mutaciones genéticas del receptor de glutamato o a la actividad de los autoantígenos/anticuerpos del receptor.
La excitotoxicidad es un proceso de sobreestimulación de los receptores de glutamato que puede provocar daños neuronales y neurodegeneración. Las excitotoxinas son aminoácidos como el glutamato, el aspartato y la cisteína que, cuando se aplican a las neuronas, provocan su sobreestimulación y muerte. A diferencia de las proteínas que contienen ácido glutámico en los alimentos, el glutamato se absorbe muy rápidamente en el tracto gastrointestinal (GIT). El glutamato absorbido podría aumentar los niveles de glutamato en el plasma sanguíneo. Sus concentraciones en el plasma son de 50-100μmol/L, en el cerebro entero son de 10.000-12.000μmol/L pero sólo de 0,5-2 μmol/L en los fluidos extracelulares (ECFs). Las bajas concentraciones de ECF, que son esenciales para una función cerebral óptima, son mantenidas por las neuronas, los astrocitos y la barrera hematoencefálica (BBB).
Sistema nervioso central (SNC)
El glutamato es el neurotransmisor excitatorio en el sistema nervioso central (SNC) de los mamíferos y desempeña un papel importante en los procesos tanto fisiológicos como patológicos. Los receptores de glutamato incluyen tres familias de receptores ionotrópicos (N-metil-Daspartato, ácido α-amino-3-hidroxi-5-metil-4-isoxazolpropiónico y kainato) y tres grupos de receptores metabotrópicos (mGluR). Están dispersos por todo el sistema nervioso central, incluyendo la amígdala, el hipocampo y el hipotálamo, donde regulan muchas funciones metabólicas y autonómicas vitales. En el cerebro, el glutamato sirve como neurotransmisor, además de su papel general en el metabolismo de las proteínas y la energía.
Los neurotransmisores se almacenan en las terminaciones nerviosas y son utilizados por las células nerviosas para inhibir o excitar otras células nerviosas o células objetivo, como las células musculares o endocrinas. A finales de la década de los 60 surgió la preocupación de que altas dosis de glutamato monosódico pudieran afectar negativamente a las funciones cerebrales, y también se informó de la posibilidad de que se produjeran lesiones cerebrales inducidas por el glutamato monosódico mediante métodos de inyección o de alimentación forzada en roedores. La altísima concentración de glutamato en el citosol y en las vesículas que contienen glutamato requiere mecanismos homeostáticos estrictos por la siguiente razón. El glutamato es el principal neurotransmisor excitatorio y, sin embargo, los niveles de glutamato en el líquido extracelular deben mantenerse bajos (
Obesidad
Los datos de los estudios en animales, en los que la administración neonatal de MSG proporciona un modelo de obesidad con alteración de la tolerancia a la glucosa y resistencia a la insulina, llevaron a la preocupación por la obesidad en los seres humanos utilizando MSG en los alimentos. Se han propuesto más hipótesis sobre los mecanismos de influencia del GMS en el metabolismo. El vínculo potencial entre el GMS y la obesidad incluye el efecto del GMS en el equilibrio energético al aumentar la palatabilidad de los alimentos y al interrumpir la cadena de señalización hipotalámica de la acción de la leptina.
Se ha informado de que el GMS aumenta la expresión del ARNm de la interleucina-6, el factor de necrosis tumoral alfa, la resistina y la leptina en el tejido adiposo visceral, aumenta los niveles de insulina, resistina y leptina en el suero y también altera la tolerancia a la glucosa. Mediante la estimulación de los receptores orosensoriales y la mejora de la palatabilidad de las comidas, influye en el aumento de peso. El glutamato monosódico (GMS) provoca la reducción de la secreción de las hormonas del crecimiento, lo que conduce a un retraso en el crecimiento y a la irreversibilidad de la obesidad, el exceso de peso, esencialmente debido a la acumulación de un exceso de grasas en el tejido adiposo, derivado de los altos niveles de colesterol que conducen a enfermedades cardiovasculares y a trastornos endocrinológicos (Figura 10).
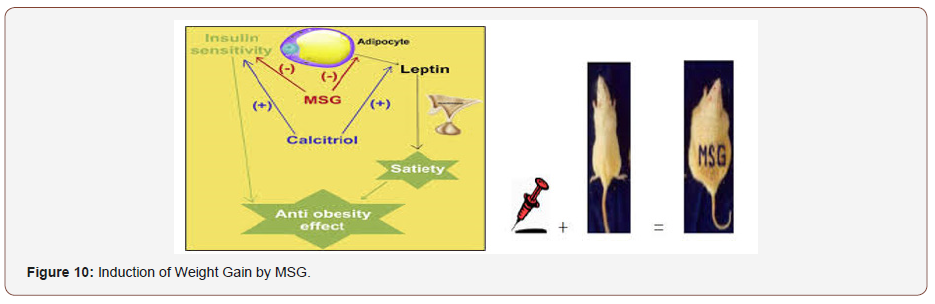
Sistema reproductor
La testosterona es una hormona del grupo de los andrógenos que estimula directamente la espermatogénesis a través de los receptores de andrógenos situados en los testículos. La tasa o el nivel de espermatogénesis también afecta al nivel de testosterona y a otras hormonas reproductivas.La progesterona es una hormona sexual femenina, sintetizada a partir de la pregnenolona, que a su vez deriva del colesterol. Forma parte del grupo de hormonas esteroides denominadas progestágenos. Desempeña un papel central en la ovulación, el embarazo, la implantación y la regulación de las funciones uterinas. Los estrógenos son hormonas esteroides producidas principalmente por los ovarios (las células de la granulosa de los folículos ováricos y los cuerpos lúteos) y la placenta (durante el embarazo). La síntesis ovárica de estrógenos es estimulada por la hormona estimulante del folículo (FSH). El GMS tiene efectos tóxicos en los testículos al causar una oligozoospermia significativa y aumentar la morfología anormal de los espermatozoides de forma dependiente de la dosis en ratas wistar macho. Se ha implicado en la infertilidad masculina al causar hemorragia testicular, degeneración y alteración de la población y morfología de los espermatozoides.
Hepatotoxicidad
El hígado es la mayor glándula del cuerpo de los mamíferos. Los hepatocitos tienen funciones metabólicas que se ocupan de procesos muy esenciales como la desintoxicación, la desaminación, la transaminación, la eliminación de amoníaco en forma de urea, la biosíntesis y la liberación de aminoácidos no esenciales y de proteínas plasmáticas con la excepción de las inmunoglobulinas, la gluconeogénesis, el almacenamiento de glucógeno, la conversión de carbohidratos y proteínas en lípidos, la síntesis de lipoproteínas, fosfolípidos y colesterol, la oxidación de ácidos grasos, el almacenamiento de hierro en forma de ferritina y el almacenamiento de vitaminas A, D y B12. Se han formulado varias pruebas de función para explorar el estado hepático. Se han determinado varias enzimas para explorar el estado hepático, como la alanina aminotransferasa (ALT) y la aspartato aminotransferasa (AST). Además, otras pruebas han incluido la medición de la deshidrogenasa láctica sérica (LDH), la gamma glutamil transpeptidasa (GGT), las fosfatasas alcalinas y las actividades de la 5-nucleotidasa. El uso de esta sustancia como potenciador del sabor a lo largo del tiempo ha sido reportado como behepatotóxico.
Nefrotoxicidad
Estudios en animales sugieren que la ingesta crónica de glutamato monosódico induce daño renal por estrés oxidativo . El estrés oxidativo está causado por la producción excesiva o la disminución de la eliminación de radicales libres en las células, la mayoría de los cuales son radicales de oxígeno y otras especies reactivas de oxígeno (ROS). Sin embargo, los mecanismos subyacentes aún no están claros, a pesar de la creciente evidencia y el consenso de que la α-cetogluterato deshidrogenasa, los receptores de glutamato y el antiportador cisteína-glutamato desempeñan un papel importante en la regulación del estrés oxidativo en la toxicidad inducida por el GMS. El metabolismo nutricional y varios factores extracelulares e intracelulares como las hormonas, las citoquinas y los procesos de desintoxicación contribuyen al estrés oxidativo, por lo que el excesivo metabolismo renal del glutamato en la ingesta crónica de GMS puede ser una fuente de ROS. Se ha demostrado una disminución del nivel de las principales enzimas antioxidantes y un aumento de la peroxidación lipídica en el riñón de las ratas expuestas al GMS de forma crónica. Además, se ha demostrado que altas dosis de glutamato inducen una toxicidad significativa en las células de cultivo renal.
La formación de ROS en el riñón de los animales expuestos al GMS fue uno de los principales factores que contribuyeron a su efecto nefrotóxico, provocando daños celulares y funcionales. Paul et al. encontraron actividades reducidas de superóxido dismutasa, catalasa, glutatión-S-transferasa y glutatión (GSH) en el riñón de los animales tras la administración de GMS. También informaron de que los marcadores de peroxidación lipídica, como el malondialdehído (MDA) y los dienos conjugados, aumentaron en el tejido renal tratado con GMS. Es posible que el GMS provoque una producción excesiva de radicales libres y que los antioxidantes endógenos sean insuficientes para satisfacer la demanda. Por otra parte, algunos estudios han encontrado los efectos de mejora de la vitamina C, E y qiercetina en los riñones tratados con GMS. Los mecanismos por los que estos antioxidantes ejercen tales efectos aún no se han dilucidado por completo. Sin embargo, estos antioxidantes parecen desempeñar un papel clave contra las respuestas inflamatorias renales a través de la disminución de la actividad de las enzimas inflamatorias y la secreción de citoquinas, o mediante la inhibición de la actividad del FNKB.
Prevención de los efectos tóxicos del GMS
Se ha informado de que el consumo de GMS entre 0,3 y 1 gramo diario es seguro. Sin embargo, en estudios con ratones, esto ha variado según el peso. Las agencias de protección del consumidor aconsejan a las personas sanas que eviten el consumo frecuente de GMS. Se ha informado de que lo siguiente minimiza el efecto tóxico del GMS.
La ingesta frecuente de vitamina C
Se ha informado de que el GMS es tóxico, especialmente para los tejidos nerviosos. Provoca la muerte celular a través del estrés oxidativo. Con los beneficios conocidos de la vitamina C, se puede reducir el efecto adverso del MSG. La investigación ha demostrado que la vitamina C es un antioxidante, con la capacidad de limpiar los radicales libres producidos en el cuerpo. La vitamina C puede eliminar el superóxido, el peróxido de hidrógeno y los radicales hidroxilo. Se ha informado de que la vitamina C invierte el impacto del GMS en el hígado al provocar una disminución significativa de las células de crecimiento no saludables y reducir las mutaciones de los genes supresores de tumores. También se ha informado de que tiene un efecto protector en el hígado.
La vitamina E
La vitamina E es un componente importante de la dieta humana. Ejerce efectos protectores contra las enfermedades que pueden atribuirse a su potente propiedad antioxidante. Como antioxidante, protege contra los efectos dañinos de los radicales libres, que pueden contribuir al desarrollo de enfermedades. La investigación ha demostrado que el glutamato induce el estrés oxidativo y la vitamina E reduce significativamente el estrés oxidativo. En los mamíferos, se ha informado de que estabiliza la membrana y elimina los radicales peroxídicos de los lípidos y el oxígeno singlete.
El ajo
El ajo es una especie de la familia de las cebollas llamada Allium sativum. El ajo también contiene enzimas, calcio, cobre, hierro, manganeso, fósforo, potasio y selenio. Las vitaminas del ajo incluyen la vitamina A, la vitamina B1 (tiamina), la vitamina B2 (riboflavina), la vitamina B6 y la vitamina C.
Curcuma longa (cúrcuma)
La cúrcuma longa, comúnmente conocida como cúrcuma, es una planta herbácea perenne arhizomatosa de la familia del jengibre, Zingiberaceae. La cúrcuma longa se ha utilizado en la medicina tradicional para una amplia gama de dolencias, incluyendo la curación de heridas, infecciones del tracto urinario y gastrointestinal, y dolencias del hígado. La curcumina se ha definido como el componente más activo de la Curcuma longa y ha demostrado tener un considerable efecto gastroprotector, antiulcerogénico y terapéutico en la enfermedad gástrica. El informe de Airaodion et al. demostró que la cúrcuma es potente en la prevención de la úlcera péptica debido a la presencia de flavonoides y otros antioxidantes. Debido a su contenido, la cúrcuma tiene la capacidad de anular el efecto del GMS en el cuerpo.
Jengibre
El jengibre (Zingiber officinale) se utiliza como especia en alimentos y bebidas y en la medicina tradicional como carminativo, antipirético y en el tratamiento del dolor, el reumatismo y la bronquitis.Sus extractos se han estudiado ampliamente por su amplia gama de actividades biológicas, como antibacteriana, analgésica y antiinflamatoria, antiangiogénica y antitumoral. También se ha utilizado para el tratamiento de trastornos gastrointestinales, incluida la úlcera gástrica. El jengibre también se ha señalado como potente en la prevención de la úlcera péptica debido a sus propiedades flavonoides y antioxidantes. Con estas actividades biológicas, el jengibre puede minimizar el efecto del glutamato monosódico en la salud humana.
Las alubias de la India
Las alubias de la India (Parkia biglobosa) se utilizan como condimento en la cocina. Es muy popular entre los yoruba de Nigeria, donde se llama «iru». Puede ser fresca o seca. La algarroba seca tiene menos sabor y picor que la fresca. La algarroba tiene un alto contenido en lípidos (29%), proteínas (35%) e hidratos de carbono (16%). Es una buena fuente de calcio y grasa para la población rural. Durante la fermentación, el contenido de azúcares reductores aumenta y el contenido total de aminoácidos libres disminuye inicialmente. Las algarrobas pueden utilizarse convenientemente en lugar de los condimentos que contienen glutamato.
Conclusión
Este estudio demostró que el glutamato monosódico es peligroso para la salud humana, ya que está relacionado con el Síndrome del Restaurante Chino (SRC). La ingesta regular de glutamato monosódico durante un largo periodo de tiempo puede provocar enfermedades como hepatotoxicidad, daños renales, fibromas, obesidad, etc. Debería crearse una mayor concienciación sobre los efectos peligrosos del glutamato monosódico para informar a la población y promover alternativas naturales al glutamato monosódico.
Conflicto de intereses
Sin conflicto de intereses.
Agradecimientos
Ninguno.
Deja una respuesta