La combustión de hidrocarburos se refiere a la reacción química en la que un hidrocarburo reacciona con el oxígeno para crear dióxido de carbono, agua y calor. Los hidrocarburos son moléculas formadas por hidrógeno y carbono. Son más conocidos por ser el componente principal de los combustibles fósiles, es decir, el gas natural, el petróleo y el carbón. Por esta razón, los recursos de combustibles fósiles suelen denominarse recursos de hidrocarburos. La energía se obtiene de los combustibles fósiles mediante la combustión (quema) del combustible. Aunque existen impurezas en los combustibles fósiles, la combustión de hidrocarburos es el proceso principal en la quema de combustibles fósiles. En la figura 1 se ilustra un ejemplo de combustión de hidrocarburos. Vea la simulación al final de la página para ver más ejemplos.
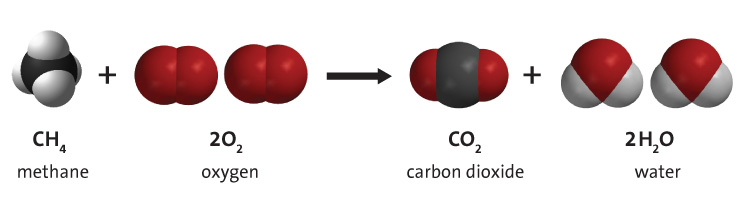
Descripción
Independientemente del tipo de hidrocarburo, la combustión con oxígeno produce 3 productos: dióxido de carbono, agua y calor, tal y como se muestra en la reacción general de abajo. La energía necesaria para romper los enlaces de las moléculas de hidrocarburo es sustancialmente menor que la energía liberada en la formación de los enlaces de las moléculas de CO2 y H2O. Por esta razón, el proceso libera cantidades significativas de energía térmica (calor). Esta energía térmica puede utilizarse directamente (por ejemplo, para calentar una casa) o bien puede convertirse en energía mecánica, utilizando un motor térmico. Sin embargo, esto está sujeto a pérdidas de eficiencia, lo que da lugar a importantes pérdidas de energía necesarias (como calor residual) regidas por la segunda ley de la termodinámica. La energía mecánica útil resultante será mucho menor que la energía térmica inicial proporcionada por la combustión de hidrocarburos.
Ecuación general de la reacción:
- se refiere al número de átomos de carbono en el hidrocarburo
- se refiere al número de átomos de hidrógeno en el hidrocarburo
- se refiere al número de átomos de oxígeno necesarios en la reacción de combustión de hidrocarburos
Combustión de hidrocarburos y combustibles fósiles
Nótese que en la combustión de hidrocarburos siempre se produce CO2; no importa el tipo de molécula de hidrocarburo. La producción de CO2 y H2O es en realidad la forma en que se obtiene la energía útil de los combustibles fósiles. Por esta razón, es importante distinguir entre el dióxido de carbono y otros productos «residuales» que surgen de las impurezas del combustible, como los compuestos de azufre y nitrógeno. Los residuos que surgen de las impurezas pueden eliminarse con la tecnología adecuada; el CO2 no puede eliminarse a menos que los combustibles fósiles no se quemen (utilicen) en primer lugar.
No todos los combustibles fósiles tienen la misma composición. El gas natural está compuesto por más del 90% de metano (CH4), que es la molécula de hidrocarburo más pequeña. El petróleo suele estar compuesto por moléculas de tamaño medio, aunque la composición varía mucho de un grado de crudo a otro. En general, cuanto más denso es el petróleo, más largas son las cadenas de carbono de las moléculas. Por último, el carbón contiene las moléculas de hidrocarburo más grandes y complejas.
Dado que los diferentes hidrocarburos tienen diferentes proporciones de hidrógeno y carbono, producen diferentes proporciones de agua y dióxido de carbono. En general, cuanto más larga y compleja es la molécula, mayor es la relación entre el carbono y el hidrógeno. Por esta razón, la combustión de cantidades iguales de diferentes hidrocarburos producirá diferentes cantidades de dióxido de carbono, dependiendo de la proporción de carbono e hidrógeno en las moléculas de cada uno. Dado que el carbón contiene las moléculas de hidrocarburo más largas y complejas, su combustión libera más CO2 que la quema de la misma masa de petróleo o gas natural. Esto también cambia la densidad energética de cada uno de estos combustibles.
Emisiones de dióxido de carbono
A continuación se muestra un gráfico del CO2 emitido por la producción de 293,1 kWh (1.000.000 BTU) de energía a partir de varios combustibles de hidrocarburos.
| Combustible | kg de emisiones de CO2 |
|---|---|
| Carbón Antracita | 104 |
| Carbón Bituminoso | 93.5 |
| Carbón Lignito | 97,9 |
| Carbón Subbituminoso | 97,4 |
| Diesel | 73.2 |
| Gasolina | 71,5 |
| Propano | 63,2 |
| Gas natural | 53.2 |
Animación de la combustión
Elige un combustible del menú desplegable para ver la reacción neta que se produce durante la combustión.
Para más información
Para más información, consulte las páginas relacionadas más abajo:
- Combustible fósil
- Energía primaria
- Recursos de hidrocarburos
- Carbón
- Petróleo
- Gas natural
- Una página al azar
Deja una respuesta