Nøgleord
CADASIL – slagtilfælde – MRT
Introduktion
Cerebral Autosomal Dominant Arteriopathy with Subcortical Infarcts and Leucoencephalopathy (CADASIL) er en arvelig sygdom i små arterier forårsaget af forskellige patogenetiske mutationer i NOTCH-3-genet. Den er karakteriseret ved at være forbundet med migræne med aura, psykiatriske symptomer, tilbagevendende iskæmiske hændelser i en tidlig alder og kognitiv svækkelse. Dette og dens typiske radiologiske fund er det, der normalt hjælper os til at mistænke sygdommen. Den anses normalt for at være en sygdom hos unge og midaldrende voksne, men tilfælde hos ældre kan være underdiagnosticeret. Vi rapporterer om en mand, der blev diagnosticeret med CADASIL i slutningen af halvfjerdserne takket være en tidligere diagnose hos hans datter.
Cases Reports
Fald 1
Vores patients datter var 50 år gammel, da hun blev sendt til vores hospital fra det neurologiske ambulatorium til yderligere undersøgelse på grund af de radiologiske fund i hendes MRI-scanning af hjernen, som bestod af hvide stofforandringer i begge ydre kapsler, bilaterale periventrikulære områder og venstre temporallap.
Hun kom til førnævnte klinik, fordi hun havde lidt af migræne med visuel aura i 30 år, med nogle episoder, der tydede på visuel aura uden hovedpine. Hun havde ingen andre symptomer. Hun var allergisk over for phosphomycin og havde fået foretaget en tonsillektomi som barn. Hun havde ingen anden sygehistorie. Hendes familiehistorie var bemærkelsesværdig: hendes mor havde migræne og mild demens, og hendes far fik et slagtilfælde i en alder af 75 år; hendes farfar, onkel og tante fra faderen havde haft slagtilfælde, og onklen var blevet diagnosticeret med Alzheimers sygdom, en faderlig fætter havde andetsteds fået diagnosen “ANA+ vaskulitis”, og en anden faderlig fætter var blevet diagnosticeret med multipel sklerose. Hun havde to raske sønner. Den fysiske undersøgelse, herunder en omhyggelig neurologisk udredning, var fuldstændig normal. Den gentagne MR-scanning af hjernen viste multiple hyperintense læsioner i den hvide substans i posterior protuberance, periventrikulære og subkortikale områder, herunder anterior temporallappe, især den venstre, begge centrum semiovale, interne og eksterne kapsler, uden tegn på nylige eller tidligere mikroblødninger (figur 1). Alle de øvrige undersøgelser, herunder hæmogram, glukæmi, lever- og nyrefunktion, erytrocytsedimentationshastighed, serumskjoldbruskkirtelhormoner, screening for hyperkoagulabilitet, vaskulitis-screening, EKG, røntgen af brystet, syfilis- og HIV-serologier og supraaortastammernes ultralydsundersøgelse med Doppler, var normale bortset fra en kolesterolemi på 220 mg/dl med et LDL-kolesterol på 152 mg/dl. Hudbiopsien var også normal. Der blev fundet en Arg169Cys-mutation (cytosin til thymin-substitution i kodon 505) i fjerde exon af NOTCH 3-genet, som vides at være patogenetisk, så hun fik stillet diagnosen CADASIL. Med denne diagnose blev begge forældre evalueret i vores klinik.
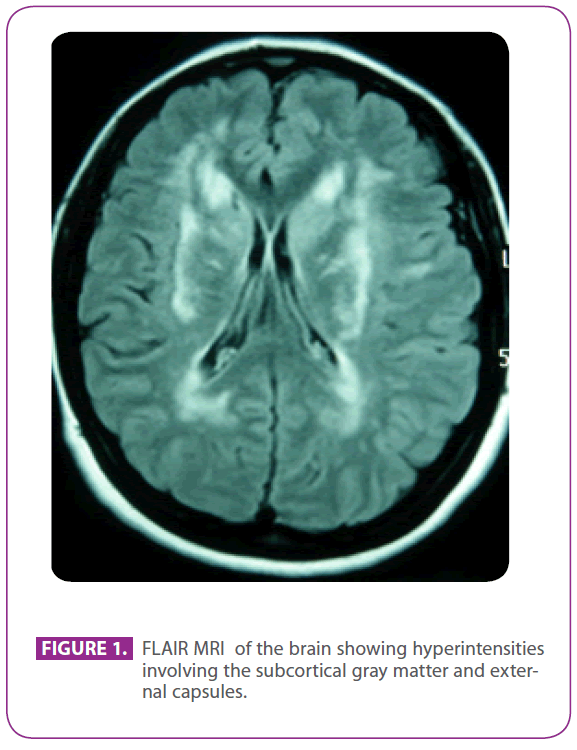
Figur 1: FLAIR-MRI af hjernen, der viser hyperintensiviteter, der involverer den subkortikale grå substans og de ydre kapsler.
Fald 2
Hendes mor var 78 år gammel. Hun havde en lang historie med migræne uden aura og havde i de sidste to år udviklet en mild demens med symmetrisk parkinsonisme, fluktuationer og REM-søvnadfærdsforstyrrelser, der tydede på demens med Lewy-kroppe. Hjerne-MRI udelukkede relevant sygdom i den hvide substans.
Hendes far var en 79-årig mand med flere vaskulære risikofaktorer: diabetes mellitus type 2, dyslipidæmi og 50 års rygning med et akkumuleret indeks på 15 pakkeår, selv om han var stoppet for 3 år siden. Han havde iskæmisk hjertesygdom med et posteroinferior myokardieinfarkt i 1991. I de sidste 8 år havde han haft tre forbigående iskæmiske ulykker og et lacunært slagtilfælde svarende til forskellige arterielle territorier, med progressiv gangforstyrrelse, og i de sidste 6 måneder var han blevet lidt tilbagetrukket og apatisk. Han havde ingen anamnese på migræne. Han var i behandling med metformin, clopidogrel, atenolol og atorvastatin. Ved fysisk undersøgelse var han ved bevidsthed og orienteret, men lidt uopmærksom, sprog og fjern- og nyere hukommelse var normale, han viste ideomotorisk apraxi, ændret ligheds- og ordfortolkning, uden frontale udløsningsreflekser. Han udviste også global hyperrefleksi med bilaterale flexor plantar reflekser og en gang med korte skridt og reducerede armbevægelser. En CT-scanning udført to år tidligere, efter et af hans forbigående iskæmiske anfald, viste omfattende sygdom i den hvide substans, især fremtrædende i den ydre kapsel og temporallapperne (figur 2).
Sammenfattende havde patienten tilbagevendende iskæmiske slagtilfælde, mild subkortikal kognitiv svækkelse og leukoencefalopati, stærkt mistænkelig for CADASIL i betragtning af hans datters diagnose. Der blev foretaget en genetisk test, som viste den samme NOTCH 3-mutation som datteren og bekræftede diagnosen.
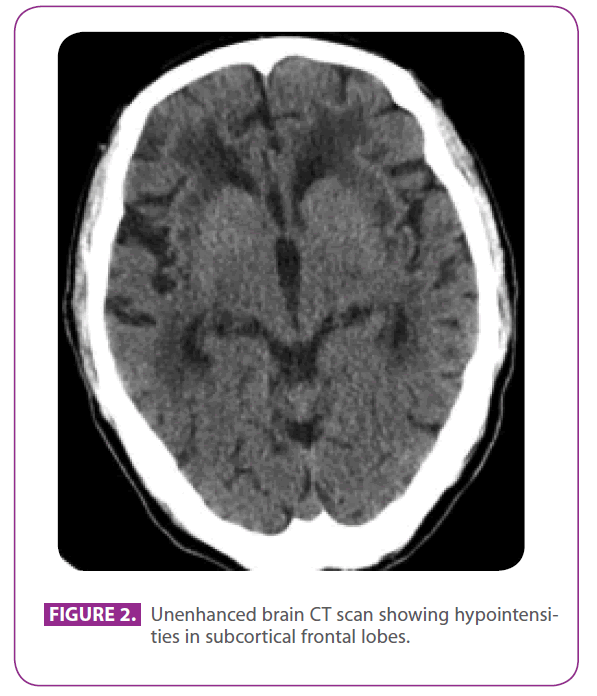
Figur 2: Unenhanced brain CT-scanning viser hypointensiteter i subkortikale frontallapper.
Diskussion
CADASIL er den mest almindelige arvelige sygdom med små kar. Den kan dog også være sporadisk, da de novo-mutationer er blevet beskrevet. Den skyldes forskellige patogene mutationer i NOTCH-3-genet, der er placeret på kromosom 19, locus 19p13.2-p13.1, og som består af 33 exoner, der koder for et protein med 2321 aminosyrer (1). Dette protein er en enkeltpasset transmembranreceptor på celleoverfladen, der udtrykkes i systemiske arterielle glatte muskelceller, med et ekstracellulært reguleringsdomæne og et intracellulært transduktordomæne. Der er til dato rapporteret om mere end 190 mutationer, der kan føre til CADASIL, og de forekommer alle i exon 2 til 24 af NOTCH 3-genet, som koder for de 34 epidermal grow factor-lignende gentagelser i den ekstracellulære del af NOTCH 3. Screening af disse 23 exoner har derfor 100 % følsomhed og næsten samme specificitet (2). Af disse mutationer er mere end 180 missense-mutationer, mindst 6 deletioner, en insertion, en frameshift og 2 duplikationer. De fleste af de patogenetiske NOTCH3-mutationer forekommer i exon 3 og 4 (3).
Alle mutationer resulterer i en tilføjelse eller et tab af en cysteinrest i en EGF-lignende gentagelse og dermed et ulige antal cysteinrester, der giver dannelse af unormale disulfidbroer. Mutanten NOTCH3 forårsager degeneration af vaskulære glatte celler i små arterier og arterioler og ophobning af det unormale protein i væggen af disse kar, hvilket fører til stenose af lumen (1). I hjernen påvirker den penetrerende cerebrale og leptomeningeale arterier, hvilket fremkalder disse kar til at være ude af stand til at autoregulere og hypoperfusion af de områder, der vandes af dem, og derfor infarkter i den hvide substans.
Det første symptom ved CADASIL er normalt migræne med aura, med en gennemsnitlig debutalder på 30 år. Det optræder hos 20 til 40 % af patienterne (4). De fleste anfald er typiske med visuel eller sensorisk aura, men halvdelen af patienterne har også atypiske anfald med basilær, hemiplegisk eller langvarig aura.
Subkortikale iskæmiske hændelser, forbigående anfald eller slagtilfælde, forekommer hos 60 til 85 % af patienterne, det første i en gennemsnitsalder på 50 år, selv om det kan forekomme så tidligt som i det andet årti. For det meste er der ingen konventionelle vaskulære risikofaktorer, eller de er ikke særlig vigtige. Hos to tredjedele af patienterne viser de iskæmiske hændelser sig klinisk og radiologisk som lacunar syndromer. De fleste af patienterne får flere slagtilfælde, normalt 2 til 5, som i løbet af flere år fører til gangbesvær, urin- og afføringsinkontinens, demens og pseudobulbar lammelse (1). Kognitiv svækkelse er den næsthyppigste kliniske manifestation. Det tidligste tegn er normalt svækkelse af de eksekutive evner og behandlingshastighed, som er til stede hos de fleste patienter over 35 år, men som kan forekomme allerede i det første årti af livet (5). Denne kognitive svækkelse er progressiv og forværres normalt ved tilbagevendende slagtilfælde, hvortil kommer svækkelse af instrumentelle aktiviteter, hukommelse, sprog, ræsonnement og visuospatiale evner. Over 70 % af patienterne er demente i det sjette årti af deres liv. Alvorlig afasi, apraksi eller agnosi er sjældne i CADASIL.
Psykiatriske lidelser, hovedsagelig humørforstyrrelser, forekommer hos 20 % af patienterne, generelt i form af alvorlige depressive episoder. Apati er til stede hos 40 % af patienterne og er ikke relateret til depression Andre mindre almindelige kliniske manifestationer er akut reversibel encephalopati (6) (hos 10 % af patienterne), hvoraf de fleste opstår efter en migræne med aura, kramper (hos 5 til 10 % af patienterne), døvhed, parkinsonisme, hjerneblødninger (oftest hos patienter med højt blodtryk) og myokardieinfarkt.
På trods af den fuldstændige penetrering har CADASIL en betydelig inter- og intrafamiliær klinisk udtryksvariabilitet. Den samme NOTCH-3-mutation har et bredt klinisk spektrum, uden klare forskelle mellem homozygote og heterozygote patienter. Faktisk er der ingen korrelation mellem genotype og klinisk fænotype (4). Årsagen til disse forskelle kendes ikke, men der er beskrevet nogle mulige fænotypemodifikatorer af CADASIL, som f.eks. nuværende rygning for risiko for slagtilfælde og alder for første slagtilfælde, højt blodtryk for risiko for slagtilfælde eller homocysteinniveauer for alder for debut af migræne (3,4). Disse og andre faktorer kan påvirke sygdommens kliniske udtryk ved at ændre genekspressionen eller ved at påvirke andre fysiopatologiske ruter, der kan føre til de samme kliniske manifestationer.
Radiologiske ændringer forekommer hos alle personer med en CADASIL-mutation før 35-årsalderen og øges med tiden. De tidligste og hyppigste træk er hyperintense ikke-forstærkende punktformede områder i cerebral hvid substans og subkortikale strukturer i T2-vægtede og væske-attenuerede inversion recovery-billeder af MRI. Involvering af ydre kapsler og den forreste del af temporallapperne er typisk for denne sygdom og et fingerpeg for diagnosen, da de hjælper i differentialdiagnosen med andre tilstande som f.eks. småkarsygdomme (1).
CADASIL anses almindeligvis for at være en sygdom hos unge og midaldrende voksne, men antallet af ældre patienter kan være underdiagnosticeret (7,8). Vores andet tilfælde kan tjene som et eksempel: en 79-årig patient med vaskulære risikofaktorer og tilbagevendende slagtilfælde med sygdom i den hvide substans, som af flere neurologer blev betragtet som sekundær til småkarsygdom. Diagnosen blev først stillet, efter at man fik kendskab til hans dattermutation. I tilfælde uden klar familiehistorie kan et åbent sind og omhyggelig opmærksomhed på suggestive radiologiske fund som f.eks. involvering af den ydre kapsel eller de forreste temporallapper være den eneste ledetråd til en korrekt diagnose.
- Chabriat H, Joutel A, Dichgans M, Tournier-Lasserve E, Bousser MG. Cadasil. Lancet Neurol 2009; 8:643-53.
- Vazquez do Campo R, Morales-Vidal S, Randolph C, Chadwick L, Biller J. CADASIL: en case-serie på 11 patienter. Rev Neurol. 2011; 52:202-10.
- Adib-Samii P, Brice G, Martin RJ, Markus HS. Klinisk spektrum af CADASIL og virkningen af kardiovaskulære risikofaktorer på fænotypen: undersøgelse af 200 konsekutivt rekrutterede personer. Stroke 2010; 4:630-4.
- Singhal S, Bevan S, Barrick T, Rich P, Markus HS. Indflydelse af genetiske og kardiovaskulære risikofaktorer på CADASIL-fænototypen. Brain. 2004; 127:2031-8.
- Dichgans M, Markus HS, Salloway S, Verkkoniemi A, Moline M, Wang Q, Posner H, Chabriat HS. Donepezil hos patienter med subkortikal vaskulær kognitiv svækkelse: et randomiseret dobbeltblindforsøg i CADASIL. Lancet Neurol. 2008;7:310-8.
- Schon F, Martin RJ, Prevett M, Clough C, Enevoldson TP, Markus HS. “CADASIL coma”: en underdiagnosticeret akut encephalopati. J Neurol Neurosurg Psychiatry. 2003;74:249-52.
- Liem MK, Lesnik Oberstein SA, Vollebregt MJ, Middelkoop HA, van der Grond J, Helderman-van den Enden AT. Homozygositet for en NOTCH3-mutation hos en 65-årig CADASIL-patient med milde symptomer: en familirapport. J Neurol. 2008 ;255:1978-80.
- Lee YC, Yang AH, Yang AH, Soong BW. Den bemærkelsesværdigt variable ekspressivitet af CADASIL: rapport om en minimalt symptomatisk mand i en fremskreden alder. J Neurol. 2009;256:1026-7
Skriv et svar