Gruppe 13-elementerne omfatter metaller efter overgangen.
Udtrykket metaller efter overgangen refererer til de elementer, der er metaller efter overgangsmetallerne. Som med metalloid-begrebet er der ikke universel konsensus om, hvad der præcist er et postovergangsmetal. Heldigvis er det i praksis mindre vigtigt at definere præcist, hvad der er og ikke er et post-overgangsmetal, end at forstå årsagen til, at det kan være nyttigt at klassificere elementer som post-overgangsmetal.
De vigtigste kendetegn ved postovergangsmetallerne er, at de er relativt elektronrige og elektronegative sammenlignet med det, man klassisk opfatter som et metal. Groft sagt udmønter dette sig i relativt lavere smeltepunkter (da flere antibindingsniveauer i båndstrukturen har tendens til at være besat), øget præference for kovalens og større sprødhed end andre metaller (på grund af den resulterende retningsbestemte binding). Deres elektronrigdom betyder, at de har en tendens til at danne bløde kationer.
Der anvendes flere systemer til at klassificere grundstoffer som tilhørende postovergangsmetallerne. De vigtigste omfatter:
- Metaller, der følger d-blokken. Ifølge denne definition er det kun metaller i gruppe 13 og højere og række 3 og højere, som danner relativt bløde og elektronrige kationer og udviser betydelig kovalens i deres bindinger, der er omfattet. Hvis dette skema vedtages for strengt, er Al imidlertid udelukket, da det teknisk set ikke følger d-blokken (og har en uudfyldt (n-1)d-underskal), og metalloiderne er udelukket, selv om mange af dem også danner relativt bløde og elektronrige kationer med fyldte (n-1)d-underskaller. En anden ulempe ved dette system er, at det sammenfiltrer spørgsmålet om, hvilke grundstoffer der skal klassificeres som post-overgangsmetaller, med det torne spørgsmål om, hvilke grundstoffer der skal klassificeres som metaller vs. metalloider.
- Metaller og metalloider i p-blokken. Dette system har den fordel, at det fremhæver de interessante og unikke egenskaber ved metaller og metalloider i p-blokken samt kontinuiteterne i disse egenskaber gennem p-blokken. Derfor vil det blive anvendt i de følgende afsnit. Det har imidlertid den ulempe, at det udelukker metaller som Zn, Cd og Hg, der danner mange forbindelser, hvori metallet har en (n-1)d10-konfiguration.
- Metaller, der følger overgangselementerne i den forstand, at de danner ioner med en fuldstændig fuld (n-1)d-valensskal, er nogle gange sammen med Al og metalloiderne i p-blokken. Denne definition tilføjer Zn, Cd og Hg (og undertiden Cu, Ag og Au), da de danner ioner med en (n-1)d 10-valenselektronkonfiguration som f.eks. Zn2+, Cd2+ og Hg2+(og Cu+, Ag+ og Au+). Da dette kapitel kun betragter p-blokelementerne for de i dette kapitel er dette system funktionelt identisk med system 2.
Hvilket klassifikationsskema man end bruger, er det ofte mere nyttigt at tænke på klassifikationen af grundstoffer som post-transitonmetaller som en måde at fremhæve ligheder i de kemiske egenskaber hos et sæt grundstoffer end som en måde at fremhæve, hvordan post-transitonmetaller adskiller sig fra andre metaller. Efterovergangsmetallerne er ikke de eneste, der danner bløde kationer eller forbindelser, der bedre kan beskrives som værende holdt sammen af kovalente bindinger. Som det fremgik af de foregående afsnit, danner selv alkalimetaller anioner under de rette omstændigheder, og mange forbindelser af metaller kan bedre beskrives ved hjælp af kovalente end ioniske vekselvirkninger. Dette var allerede tydeligt i kemien af de alkaliske jordarmetaller Be og Mg, som blev diskuteret i det foregående afsnit. I de efterfølgende kapitler vil bindinger og reaktivitet i koordinationskomplekser og organometalliske forbindelser i vid udstrækning blive beskrevet i kovalente termer.
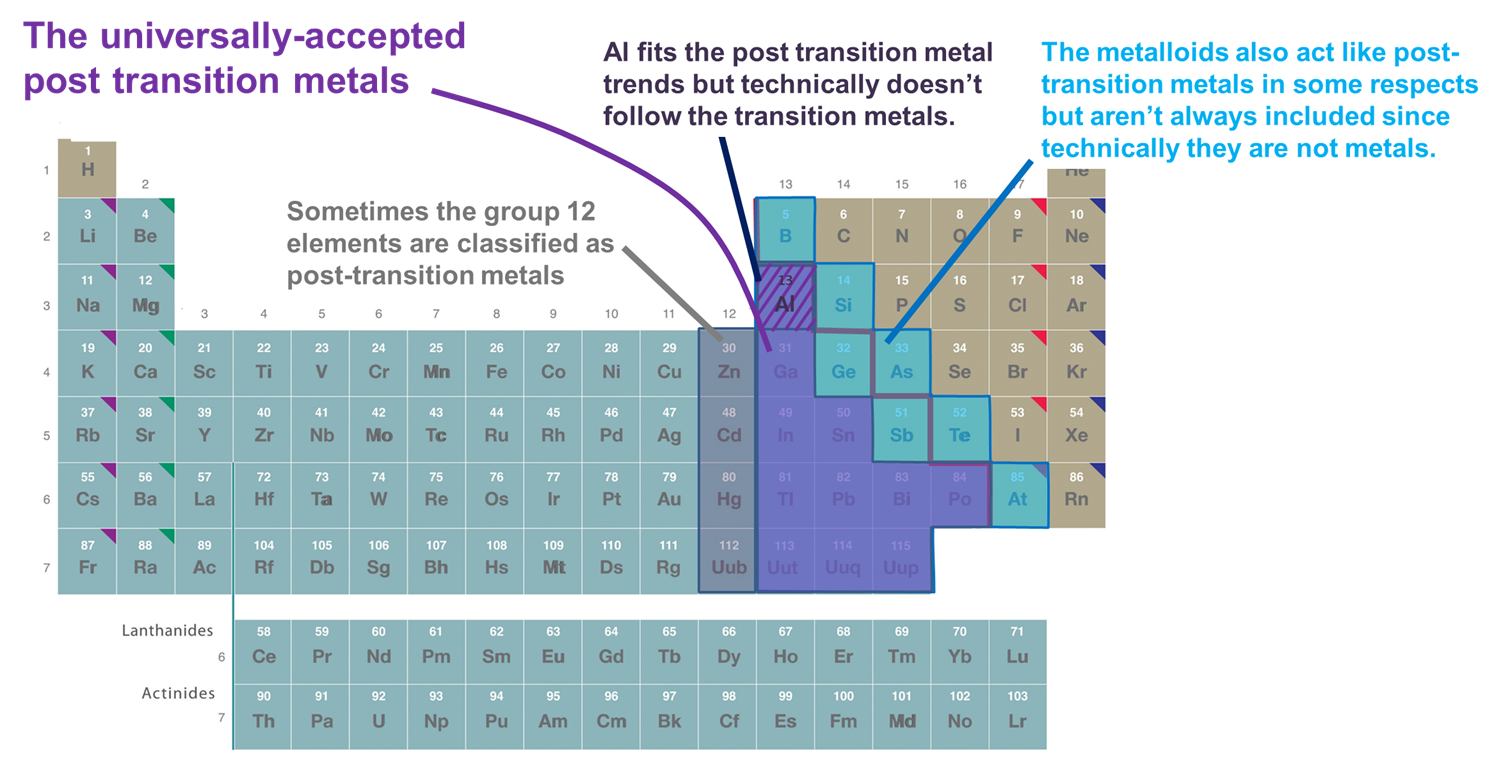
Figur \(\sf{{\PageIndex{2}}}\). Nogle af de grundstoffer, der klassificeres som efterovergangsmetaller. De, der er vist med lilla, accepteres almindeligvis, da de er metaller og klart følger overgangsmetallerne, mens metallerne i gruppe 12 (og nogle gange 11), Al og metalloiderne alle nogle gange er med, da de opfører sig som de andre efterovergangsmetaller i vigtige henseender. Det periodiske system er tilpasset fra det på https://chem.libretexts.org/Bookshelves/General_Chemistry/Map%3A_Chemistry_-_The_Central_Science_(Brown_et_al.)/02._Atoms%2C_Molecules%2C_and_Ions/2.5%3A_The_Periodic_Table.
Skriv et svar